
| A. | Ba( NO3-)2=Ba2++( NO3-) 2 | B. | NaHSO4=Na++H++SO42- | ||
| C. | H2SO4=2H++SO42- | D. | KClO3=K++ClO3- |
分析 A.硝酸鋇完全電離生成鋇離子和2個硝酸根離子;
B.硫酸氫鈉完全電離生成鈉離子、氫離子和硫酸根離子;
C.硫酸完全電離生成氫離子和硫酸根離子;
D.氯酸鉀完全電離生成鉀離子和氯酸根離子.
解答 解:A.硝酸鋇完全電離生成鋇離子和2個硝酸根離子,電離方程式為Ba( NO3)2=Ba2++2 NO3-,故A錯誤;
B.硫酸氫鈉完全電離生成鈉離子、氫離子和硫酸根離子,電離方程式為NaHSO4=Na++H++SO42-,故B正確;
C.硫酸完全電離生成氫離子和硫酸根離子,電離方程式為H2SO4=2H++SO42-,故C正確;
D.氯酸鉀完全電離生成鉀離子和氯酸根離子,電離方程式為KClO3=K++ClO3-,故D正確;
故選A.
點評 本題考查電離方程式的書寫,側重考查學生分析判斷能力,明確電解質強弱及電離出的離子是解本題關鍵,注意硫酸氫鈉在水溶液中和熔融狀態下電離方式的不同點,題目難度不大.


 輕松奪冠全能掌控卷系列答案
輕松奪冠全能掌控卷系列答案科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 若三種溶液中c(H+)分別為a1 mol•L-1、a2 mol•L-1、a3 mol•L-1,則它們的大小關系為$\frac{1}{2}$a2=a1=a3 | |
| B. | 等體積的以上三種酸分別與過量的NaOH溶液反應,若生成的鹽的物質的量依次為b1 mol、b2 mol、b3 mol,則它們的大小關系為b1=b2<b3 | |
| C. | 分別用以上三種酸中和一定量的NaOH溶液生成正鹽,若需要酸的體積分別為V1、V2、V3,其大小關系為V1=V2=V3 | |
| D. | 分別與Zn反應,開始時生成H2的速率分別為v1、v2、v3,其大小關系為v2>v1>v3 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H2CO3?2H++CO32- | B. | NaHSO4?Na++HSO4- | ||
| C. | H2S+H2O?HS-+H3O+ | D. | Ca(OH)2?Ca2++2OH- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
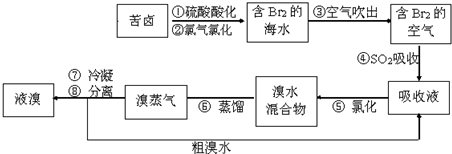
| A. | 步驟④⑤是為了富集溴 | |
| B. | 步驟③說明溴具有揮發性 | |
| C. | 步驟④的離子方程式為Br2+SO2+H2O═2H++2Br-+SO32- | |
| D. | 步驟⑧中溴蒸氣冷凝后得到液溴與溴水的混合物可用分液漏斗分離 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 活性炭/mol | NO/mol | A/mol | B/mol | p/MPa | |
| 200℃ | 2.00 | 0.0400 | 0.0300 | 0.0300 | 3.93 |
| 335℃ | 2.005 | 0.050 | 0.0250 | 0.0250 | p |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com