
| A. | 碳酸氫鈉在水中的電離:NaHCO3═Na++H++CO32- | |
| B. | 鈉與水的反應:2Na+2H2O═2Na++2OH-+H2↑ | |
| C. | 氯氣和水的反應:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 鋁和燒堿溶液的反應:Al+2OH-═AlO-2+H2↑ |
分析 A.碳酸氫鈉電離出鈉離子和碳酸氫根離子,碳酸氫根離子不能拆開;
B.鈉與水反應生成氫氧化鈉和氫氣;
C.次氯酸為弱酸,離子方程式中拆開不能拆開,應該保留分子式;
D.2mol鋁完全反應生成3mol氫氣,該反應不滿足電子守恒、電荷守恒.
解答 解:A.碳酸氫根離子不能拆開,正確的離子方程式為:NaHCO3=Na++HCO3-,故A錯誤;
B.鈉與水的反應生成氫氧化鈉和氫氣,反應的離子方程式為:2Na+2H2O═2Na++2OH-+H2↑,故B正確;
C.氯氣和水反應生成的次氯酸是弱酸,應該用化學式表示,正確的離子方程式為:Cl2+H2O═H++Cl-+HClO,故C錯誤;
D.鋁與氫氧化鈉溶液反應生成偏鋁酸鈉和氫氣,正確的離子方程式為:2Al+2OH-+2H2O=2AlO2-+3H2↑,故D錯誤;
故選B.
點評 本題考查了離子方程式的書寫判斷,為高考的高頻題,題目難度中等,注意掌握離子方程式的書寫原則,明確離子方程式正誤判斷常用方法:檢查反應物、生成物是否正確,檢查各物質拆分是否正確,如難溶物、弱電解質等需要保留化學式,檢查是否符合守恒關系(如:質量守恒和電荷守恒等)等.


科目:高中化學 來源: 題型:選擇題
| A. | C4H8O2的酯有4種結構 | |
| B. | 淀粉和纖維素互為同分異構體 | |
| C. | 乙醇和葡萄糖均能發生酯化反應 | |
| D. | 用氫氧化鈉溶液可以鑒別地溝油和礦物油 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
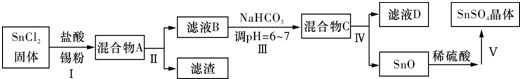
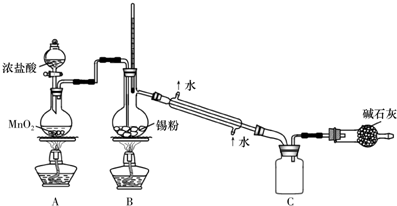
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1.7g OH- 所含電子數為0.9NA | |
| B. | 標準狀況下,11.2 L HCl 所含質子數為18NA | |
| C. | 常溫下,11.2 L Cl2 氣所含原子數為NA | |
| D. | 0.5 mol D2O 中所含質子數為5NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H+、SO42-、NO3-、Ba2+ | B. | K+、Cl-、CO32-、Na+ | ||
| C. | Cu2+、NO3-、OH-、Na+ | D. | K+、SO42-、HCO3-、H+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 做“鈉與水的反應”實驗時,切取綠豆粒大小的金屬鈉,用濾紙吸干表面的煤油,放入燒杯中,滴入兩滴酚酞溶液,再加入少量水,然后觀察并記錄實驗現象 | |
| B. | 用蒸餾法提純物質時,如果把溫度計水銀球位于蒸餾燒瓶支管口下方,會使收集的產品中混有低沸點的雜質 | |
| C. | 制備乙酸乙酯時,向乙醇中緩慢加入濃硫酸和冰醋酸,加熱3~5min,將導氣管插入飽和Na2CO3溶液中以便于除去乙醇和乙酸 | |
| D. | 為檢驗皂化反應進行程度,取幾滴反應液,滴入裝有熱水的試管中,振蕩,若有油滴浮在液面上,說明油脂已完全反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A. | 反應在前50s 的平均速率 (PCl3)=0.0032mol•L-1•s-1 | |
| B. | 保持其他條件不變,升高溫度,平衡時 (PCl3)=0.11mol•L-1,則反應的△H<0 | |
| C. | 相同溫度下,起始時向容器中充入1.0mol PCl5、0.20mol PCl3和0.20mol Cl2,反應達到平衡前 (正)>(逆) | |
| D. | 相同溫度下,起始時向容器中充入2.0mol PCl3和2.0mol Cl2,達到平衡時,PCl3的轉化率小于80% |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
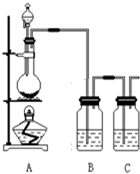 為了驗證氯元素的非金屬性比碘元素的非金屬性強,某化學實驗小組利用題中所給試劑設計了如下實驗,請回答下列問題:
為了驗證氯元素的非金屬性比碘元素的非金屬性強,某化學實驗小組利用題中所給試劑設計了如下實驗,請回答下列問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com