
【題目】某NaAlO2、Na2CO3的混合溶液中逐滴加入 1mol·L-1的鹽酸,測得溶液中的CO32-、HCO3-、AlO2-、Al3+的物質的量與加入鹽酸溶液的體積變化關系如圖所示。(已知:H2CO3的電離平衡常數K1=4.3×10-7,K2=5.6×10-11;Al(OH)3的酸式電離平衡常數K=6.3×10-13)則下列說法正確的是
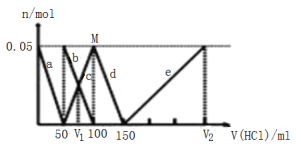
A.V1:V2=1:4
B.M點時生成的CO2為0.05mol
C.原混合溶液中的CO32-與AlO2-的物質的量之比為1:3
D.a曲線表示的離子方程式為:AlO2-+4H+=Al3++2H2O
【答案】A
【解析】
Na2CO3、NaAlO2的混合溶液中逐滴加入1molL-1的鹽酸后,首先發生反應:![]() ,a曲線表示AlO2-,由圖可知AlO2-反應完畢,加入鹽酸50mL,根據方程式可知:n(AlO2-)=n(H+)=0.05mol×1mol/L=0.05mol;
,a曲線表示AlO2-,由圖可知AlO2-反應完畢,加入鹽酸50mL,根據方程式可知:n(AlO2-)=n(H+)=0.05mol×1mol/L=0.05mol;
AlO2-反應完畢,發生反應:![]() ,b曲線表示CO32-,c曲線表示HCO3-,由圖可知CO32-反應完畢,該階段加入鹽酸100mL-50mL=50mL,根據方程式可知:n(CO32-)=n(H+)=0.05mol×1mol/L=0.05mol;
,b曲線表示CO32-,c曲線表示HCO3-,由圖可知CO32-反應完畢,該階段加入鹽酸100mL-50mL=50mL,根據方程式可知:n(CO32-)=n(H+)=0.05mol×1mol/L=0.05mol;
CO32-反應完畢,發生反應![]() ,d曲線表示HCO3-,由圖可知HCO3-反應完畢,該階段加入鹽酸150mL-100mL=50mL,根據方程式可知n(HCO3-)=n(H+);
,d曲線表示HCO3-,由圖可知HCO3-反應完畢,該階段加入鹽酸150mL-100mL=50mL,根據方程式可知n(HCO3-)=n(H+);
發生反應![]() ,e曲線表示Al3+,由圖可知Al(OH)3反應完畢,根據方程式可知n(H+)=3n[Al(OH)3]=3×0.05mol=0.15mol,進而求出消耗鹽酸的體積。
,e曲線表示Al3+,由圖可知Al(OH)3反應完畢,根據方程式可知n(H+)=3n[Al(OH)3]=3×0.05mol=0.15mol,進而求出消耗鹽酸的體積。
Na2CO3、NaAlO2的混合溶液中逐滴加入1molL-1的鹽酸后,首先發生反應:![]() ,a曲線表示AlO2-,由圖可知AlO2-反應完畢,加入鹽酸50mL,根據方程式可知:n(AlO2-)=n(H+)=0.05mol×1mol/L=0.05mol;
,a曲線表示AlO2-,由圖可知AlO2-反應完畢,加入鹽酸50mL,根據方程式可知:n(AlO2-)=n(H+)=0.05mol×1mol/L=0.05mol;
AlO2-反應完畢,發生反應:![]() ,b曲線表示CO32-,c曲線表示HCO3-,由圖可知CO32-反應完畢,該階段加入鹽酸100mL-50mL=50mL,根據方程式可知:n(CO32-)=n(H+)=0.05mol×1mol/L=0.05mol;
,b曲線表示CO32-,c曲線表示HCO3-,由圖可知CO32-反應完畢,該階段加入鹽酸100mL-50mL=50mL,根據方程式可知:n(CO32-)=n(H+)=0.05mol×1mol/L=0.05mol;
CO32-反應完畢,發生反應![]() ,d曲線表示HCO3-,由圖可知HCO3-反應完畢,該階段加入鹽酸150mL-100mL=50mL,根據方程式可知n(HCO3-)=n(H+);
,d曲線表示HCO3-,由圖可知HCO3-反應完畢,該階段加入鹽酸150mL-100mL=50mL,根據方程式可知n(HCO3-)=n(H+);
發生反應![]() ,e曲線表示Al3+,由圖可知Al(OH)3反應完畢,根據方程式可知n(H+)=3n[Al(OH)3]=3×0.05mol=0.15mol,該階段加入鹽酸體積為:
,e曲線表示Al3+,由圖可知Al(OH)3反應完畢,根據方程式可知n(H+)=3n[Al(OH)3]=3×0.05mol=0.15mol,該階段加入鹽酸體積為:![]() 。
。
A. 原溶液中n(CO32-)=0.05mol,V1時溶液中碳酸氫根離子等于碳酸根離子為0.025ml,由反應![]() 可知,需要鹽酸為0.025mol,鹽酸的體積為25mL,故V1=50mL+25mL=75mL,由上述分析可知,V2=150mL+150mL=300mL,故V1:V2=75mL:300mL=l:4,故A正確;
可知,需要鹽酸為0.025mol,鹽酸的體積為25mL,故V1=50mL+25mL=75mL,由上述分析可知,V2=150mL+150mL=300mL,故V1:V2=75mL:300mL=l:4,故A正確;
B. 根據述分析可知,M點時溶液中CO32-完全轉化為HCO3-,沒有CO2生成,故B錯誤;
C. 由上述分析可知,原混合溶液中的CO32-與AlO2-的物質的量之比為:0.05mol:0.05mol=1:1span>,故C錯誤;
D. 由上述分析可知,a曲線表示的離子方程式為:![]() ,故D錯誤;
,故D錯誤;
故答案選:A。


科目:高中化學 來源: 題型:
【題目】H2O2分解速率受多種因素影響。實驗測得 70 ℃時不同條件下H2O2濃度隨時間的變化如圖所示。下列說法正確的是
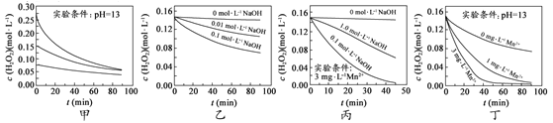
A.圖甲表明,其他條件相同時,H2O2濃度越小,其分解速率越快
B.圖乙表明,其他條件相同時,溶液pH越小,H2O2分解速率越快
C.圖丙表明,少量Mn 2+存在時,溶液堿性越強,H2O2分解速率越快
D.圖丙和圖丁表明,堿性溶液中,Mn2+對H2O2分解速率的影響大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】關于下列裝置的說法正確的是
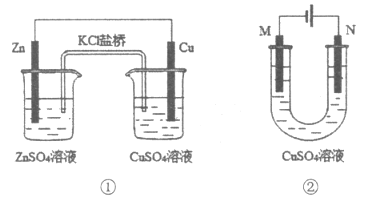
A.裝置①中Cu為正極,電極上大量氣泡產生
B.裝置①中e-的遷移方向是:Zn→導線→Cu→鹽橋→Zn
C.若裝置②用于鐵棒鍍銅,則N極為銅棒
D.若裝置②用于電解精煉銅,則電解前后溶液中的Cu2+濃度保持不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】N2O、NO和NO2等氮氧化物是空氣污染物,含有氮氧化物的尾氣需處理后才能排放。
(1)N2O的處理。N2O是硝酸生產中氨催化氧化的副產物,用特種催化劑能使N2O分解。NH3與O2在加熱和催化劑作用下生成N2O的化學方程式為________。
(2)NO和NO2的處理。已除去N2O的硝酸尾氣可用NaOH溶液吸收,主要反應為
NO+NO2+2OH![]() 2
2![]() +H2O
+H2O
2NO2+2OH![]()
![]() +
+![]() +H2O
+H2O
①下列措施能提高尾氣中NO和NO2去除率的有________(填字母)。
A.加快通入尾氣的速率
B.采用氣、液逆流的方式吸收尾氣
C.吸收尾氣過程中定期補加適量NaOH溶液
②吸收后的溶液經濃縮、結晶、過濾,得到NaNO2晶體,該晶體中的主要雜質是________(填化學式);吸收后排放的尾氣中含量較高的氮氧化物是________(填化學式)。
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾氣,可提高尾氣中NO的去除率。其他條件相同,NO轉化為![]() 的轉化率隨NaClO溶液初始pH(用稀鹽酸調節)的變化如圖所示。
的轉化率隨NaClO溶液初始pH(用稀鹽酸調節)的變化如圖所示。
①在酸性NaClO溶液中,HClO氧化NO生成Cl和![]() ,其離子方程式為________。
,其離子方程式為________。
②NaClO溶液的初始pH越小,NO轉化率越高。其原因是________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗操作或裝置能達到目的的是( )
A | B | C | D |
|
|
|
|
混合濃硫酸和乙醇 | 配制一定濃度的溶液 | 收集 | 證明乙炔可使溴水褪色 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(題文)化合物N具有鎮痛、消炎等藥理作用,其合成路線如下:

(1)A的系統命名為____________,E中官能團的名稱為____________。
(2)A→B的反應類型為____________,從反應所得液態有機混合物中提純B的常用方法為____________。
(3)C→D的化學方程式為________________________。
(4)C的同分異構體W(不考慮手性異構)可發生銀鏡反應:且1 mol W最多與2 mol NaOH發生反應,產物之一可被氧化成二元醛。滿足上述條件的W有____________種,若W的核磁共振氫譜具有四組峰,則其結構簡式為____________。
(5)F與G的關系為(填序號)____________。
a.碳鏈異構 b.官能團異構 c.順反異構 d.位置異構
(6)M的結構簡式為____________。
(7)參照上述合成路線,以![]() 為原料,采用如下方法制備醫藥中間體
為原料,采用如下方法制備醫藥中間體![]() 。
。

該路線中試劑與條件1為____________,X的結構簡式為____________;
試劑與條件2為____________,Y的結構簡式為____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知某二元酸H2MO4在水中電離分以下兩步:H2MO4H++HMO4-,HMO4-H++MO42-。常溫下向20 mL0.1mol/L NaHMO4溶液中滴入cmol/LNaOH溶液,溶液溫度與滴入NaOH溶液體積關系如圖。下列說法正確的是
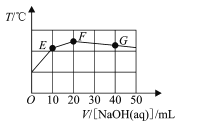
A.該氫氧化鈉溶液pH=12
B.圖像中F點對應的溶液中c(OH-)>c(HMO4-)
C.滴入NaOH溶液過程中水的電離程度一直增大
D.圖像中G點對應的溶液中c(Na+)=c(HMO4-)+2c(MO42-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】重鉻酸鉀(K2Cr2O7)是一種重要的化工原料,以FeO·Cr2O3為原料制備K2Cr2O7的流程如下:

已知:2FeO·Cr2O3+4Na2CO3+7NaNO3![]() 4Na2CrO4+Fe2O3+4CO2↑+7NaNO2
4Na2CrO4+Fe2O3+4CO2↑+7NaNO2
回答下列問題:
(1)寫出濾渣的一種用途:___________________。
(2)“調節pH”可實現CrO42-和Cr2O72-在溶液中相互轉化。室溫下,若初始濃度為1.0 mol·L-1的Na2CrO4溶液中c(Cr2O72-)隨c(H+)的變化如圖所示:

①由圖可知,溶液酸性增大,CrO42-的平衡轉化率________(填“增大”“減小”或“不變”)。
②根據A點數據,計算出該轉化反應的平衡常數為_________。
(3)流程中的“轉化”過程中發生的反應屬于_________(填基本反應類型)。
(4)在化學分析中采用K2CrO4為指示劑,以AgNO3標準溶液滴定溶液中的Cl-,利用Ag+與CrO42-生成磚紅色沉淀,指示到達滴定終點。當溶液中Cl-恰好完全沉淀(濃度等于1.0×10-5 mol·L-1)時,溶液中c(Ag+)為_______mol·L-1,此時溶液中c(CrO42-)等于________mol·L-1。(已知Ag2CrO4、AgCl的Ksp分別為2.0×10-12和2.0×10-10)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CuCl為白色粉末,微溶于水,不溶于乙醇,潮濕的CuCl在空氣中被氧化為Cu2(OH)3Cl。
(1)一種由海綿銅(Cu)為原料制備CuCl的工藝流程如下:

①“溶解”步驟發生反應的離子方程式為_________________________________;
②潮濕的CuCl在空氣中被氧化的化學反應方程式為_________________________________;
③已知常溫下Cu(OH)2溶度積常數Ksp=2×10-20要使c(Cu2+)=0.2 mol·L-1的硫酸銅溶液中的銅離子沉淀比較完全(使銅離子濃度變為原來的千分之一)則應調節溶液pH為___________以上。
(2)次磷酸(H3PO2)是一元中強酸,可用于作金屬表面處理劑。
①向Ba(H2PO2)2溶液中加入硫酸可以制取H3PO2,寫出反應的化學方程式:_____________;
②H3PO2可將溶液中的Ag+還原為銀,從而用于化學鍍銀,反應同時生成P元素最高價氧化物對應的水化物。在該過程中,氧化劑與還原劑的物質的量之比為:___________;
③NaH2PO2的水溶液呈弱堿性,用離子方程式說明原因:______________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com