
在一定條件下,已達平衡的可逆反應:2A(g)+B(g)  2C(g),下列說法中正確的是 ( )
2C(g),下列說法中正確的是 ( )
A.平衡時,此反應的平衡常數K與各物質的濃度有如下關系:K=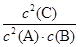 |
| B.改變條件后,該反應的平衡常數K一定不變 |
| C.如果改變壓強并加入催化劑,平衡常數會隨之變化 |
| D.若平衡時增加A和B的濃度,則平衡常數會減小 |
A
解析試題分析:對于在一定條件下進行的可逆反應來說,當反應達到化學平衡時,各生成物的濃度冪指數的乘積與各反應物的濃度冪指數乘積的比是個常數。這個常數就是化學平衡常數。化學平衡常數只與溫度有關。而與濃度、壓強等無關。根據化學平衡常數的定義可知A.平衡時,此反應的平衡常數K與各物質的濃度有如下關系:K=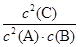 是正確的。B.如果改變的條件溫度,則該反應的平衡常數K改變,若改變的是其它條件,則平衡常數K不變。錯誤。C.如果改變壓強并加入催化劑,溫度沒變,平衡常數也不會隨之變化。錯誤。D.若平衡時只是增加A和B的濃度,并未改變溫度,平衡常數不變。錯誤。
是正確的。B.如果改變的條件溫度,則該反應的平衡常數K改變,若改變的是其它條件,則平衡常數K不變。錯誤。C.如果改變壓強并加入催化劑,溫度沒變,平衡常數也不會隨之變化。錯誤。D.若平衡時只是增加A和B的濃度,并未改變溫度,平衡常數不變。錯誤。
考點:考查外界因素與化學平衡常數的關系的知識。


 金牌教輔培優優選卷期末沖刺100分系列答案
金牌教輔培優優選卷期末沖刺100分系列答案科目:高中化學 來源: 題型:單選題
對于反應:H2(g)+I2(g) 2HI(g),在一恒定壓強的容器中進行,下列可以判斷此反應達到平衡狀態的是( )
2HI(g),在一恒定壓強的容器中進行,下列可以判斷此反應達到平衡狀態的是( )
| A.混合氣體的體積保持不變 | B.混合氣體的密度保持不變 |
| C.混合氣體平均相對分子質量保持不變 | D.混合氣體顏色保持不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在密閉容器中發生下列反應aA(g) cC(g)+dD(g),反應達到平衡后,將氣體體積壓縮到原來的一半,當再次達到平衡時,C的濃度為原平衡的1.6倍,下列敘述正確的是
cC(g)+dD(g),反應達到平衡后,將氣體體積壓縮到原來的一半,當再次達到平衡時,C的濃度為原平衡的1.6倍,下列敘述正確的是
| A.A的轉化率變大 | B.平衡向正反應方向移動 |
| C.D的質量分數變大 | D.a<c+d |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
對于A2+3B2 2C的反應來說,以下化學反應速率的表示中,反應速率最快的是
2C的反應來說,以下化學反應速率的表示中,反應速率最快的是
A.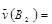 0.8mol·L-1·s-1 0.8mol·L-1·s-1 | B. 0.7mol·L-1·s-1 0.7mol·L-1·s-1 |
C. 0.4mol·L-1·s-1 0.4mol·L-1·s-1 | D.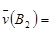 54mol·L-1·min-1 54mol·L-1·min-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
反應4NH3+5O2 4NO+6H2O(g),在5L的密閉容器中進行半分鐘后,NO的物質的量增加了0.3mol,則此反應的平均速率υ(x)(表示反應物的消耗速率或生成物的生成速率)為 ( )
4NO+6H2O(g),在5L的密閉容器中進行半分鐘后,NO的物質的量增加了0.3mol,則此反應的平均速率υ(x)(表示反應物的消耗速率或生成物的生成速率)為 ( )
| A.υ(O2)="0.001" mol·L-1·s-1 | B.υ(NO)="0.06" mol·L-1·s-1 |
| C.υ(H2O) ="0.003" mol·L-1·s-1 | D.υ(NH3)="0.001" mol·L-1·s-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
硫代硫酸鈉與稀鹽酸的反應Na2S2O3+2HCl→2NaCl+S↓+SO2↑+H2O在加熱條件下反應速度加快,原因主要是
| A.該反應是吸熱反應,且可逆,加熱使平衡向正向移動 |
| B.加熱促使SO2逸出,使平衡向正向移動 |
| C.加熱促進S2O32-與H+的碰撞,使反應加速 |
| D.加熱促進Na+與Cl-的碰撞,使反應加速 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
已知A(s)+2B(g)  2C(g)+D(g) △H<0 在一密閉容器中反應的υ-t圖。t1時,改變了一個條件,下列敘述正確的是
2C(g)+D(g) △H<0 在一密閉容器中反應的υ-t圖。t1時,改變了一個條件,下列敘述正確的是
| A.t1時,一定是升高了反應的溫度 |
| B.t1時,可能是向容器中通入了一定量的C氣體 |
| C.t1時,可能是向容器中加入了催化劑 |
| D.t1時改變外界條件后,該反應的平衡常數可能減小,也可能不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
化學反應C(s)+H2O(g) CO(g)+H2(g);△H>0達到平衡,下列敘述正確的是
CO(g)+H2(g);△H>0達到平衡,下列敘述正確的是
| A.升高溫度,正反應速率增大,逆反應速率減小,平衡向正反應方向移動 |
| B.加入固體碳,平衡向正反應方向移動 |
| C.加入水蒸氣使容器壓強增大,平衡向逆反應方向移動動 |
| D.減小壓強,平衡向正反應方向移 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
對于可逆反應2HI(g)  I2(g)+H2(g),下列敘述能夠說明已達到平衡狀態的是
I2(g)+H2(g),下列敘述能夠說明已達到平衡狀態的是
| A.各物質的量的濃度比2 : 1: 1 |
| B.容器內的總壓不隨時間變化 |
| C.生成2 mol H-I鍵的同時生成1 mol I-I鍵 |
| D.混合氣體的顏色不再變化時 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com