
���� ��1������(j��)NԪ���غ㣬��֪n��NO2��+n��NO��=n������Һ��HNO3��-n��������Һ��NO3-������NO2��NO�����|(zh��)�����քe��xmol��ymol����������D(zhu��n)���غ㡢���ߵ����|(zh��)����֮���з���Ӌ�㣮
��2���������NaNO2��NaNO3�����Һ������(j��)NԪ���غ��֪��n��NaNO2��+n��NaNO3��=n��NO2��+n��NO��������(j��)�cԪ���غ��֪��n��NaOH��=n��NaNO2��+n��NaNO3�����ٸ���(j��)V=$\frac{n}{c}$Ӌ�㣮
��� �⣺��1��6.4g Cu�����|(zh��)����=$\frac{6.4g}{64g/mol}$=0.1mol��������Һn��Cu2+��=n��Cu��=0.1mol������(j��)NԪ���غ㣬��֪n��NO2��+n��NO��=n������Һ��HNO3��-n��������Һ��NO3-��=0.05L��9mol/L=0.45mol-0.1L��3mol/L=0.15mol��
��NO2��NO�����|(zh��)�����քe��xmol��ymol���t��
$\left\{\begin{array}{l}{x+y=0.15}\\{x+y=0.15\\;x+3y=0.1��2}\end{array}\right.$��
���x=0.125��y=0.025��
�ʴ𰸞飺0.125��
��2���������NaNO2��NaNO3�����Һ������(j��)NԪ���غ��֪��n��NaNO2��+n��NaNO3��=n��NO2��+n��NO��=0.15mol������(j��)�cԪ���غ��֪��n��NaOH��=n��NaNO2��+n��NaNO3��=0.15mol��NaOH��Һ���w�e��$\frac{0.15mol}{1mol/L}$=0.15L=150mL��
�ʴ𰸞飺150��
�c�u ���}����������߀ԭ���������P(gu��n)Ӌ�㣬����(j��)ԭ���غ㡢늺��غ����������y���еȣ�



| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
| A�� | 4g D2������O2����������D2O 2NA�� | |
| B�� | 98g H3PO4��H2SO4�Ļ�����к���ԭ��2.5NA�� | |
| C�� | 6.02��1023�������Ƿ��Ӽs���u��6NA�� | |
| D�� | 1molNa��ȫȼ�����D(zhu��n)�����NA�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�����}
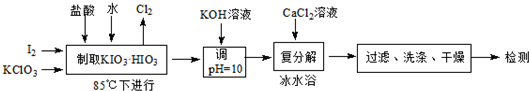
| �ض�/�� | 0 | 10 | 20 | 40 | 60 | 80 |
| KIO3 | 4.60 | 6.27 | 8.08 | 12.6 | 18.3 | 24.8 |
| KCl | 28.1 | 31.2 | 34.2 | 40.1 | 45.8 | 51.3 |
| Ca��IO3��2 | 0.119 | 0.195 | 0.3071 | 0.520 | 0.621 | 0.669 |
| �����}�����ΑB(t��i) | �oˮ�} | һˮ���� | ��ˮ���� |
| ��(w��n)���r�Ĝضȅ^(q��)�� | ��57.5�� | 32-57.5�� | ��32�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
| A�� | �ɴ˿ɴ_����Ԫ�ص�����ԭ���|(zh��)����131 | |
| B�� | $\stackrel{131}{53}$I�ǵ�Ԫ�ص�һ�Nͬλ�� | |
| C�� | $\stackrel{131}{53}$I�����к����Ӕ�(sh��)��53 | |
| D�� | $\stackrel{131}{53}$I2��Ħ���|(zh��)����262 g |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�����}
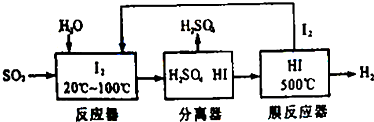
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�����}
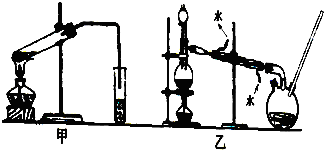
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
| A�� | Cu | B�� | Si | C�� | SiO2 | D�� | Al2O3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
| A�� | ��������ɭ�� | B�� | ����ȼ��ú��ʯ�͵Ȼ�ʯȼ�� | ||
| C�� | ˮ����ʧ | D�� | ��܇�ŷ�β�℡�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
 T��r����6mol CO2��8mol H2����2L���]���������У��l(f��)��������CO2��g��+3H2��g��?CH3OH��g��+H2O��g����������H2�����|(zh��)�����S�r�g׃����D�Ќ�����ʾ���D��̓����ʾ�H��׃ijһ�����l���r��H2�����|(zh��)�����S�r�g��׃���������f�����_���ǣ�������
T��r����6mol CO2��8mol H2����2L���]���������У��l(f��)��������CO2��g��+3H2��g��?CH3OH��g��+H2O��g����������H2�����|(zh��)�����S�r�g׃����D�Ќ�����ʾ���D��̓����ʾ�H��׃ijһ�����l���r��H2�����|(zh��)�����S�r�g��׃���������f�����_���ǣ�������| A�� | �����_ʼ��a�c�rv��H2��=2 mol/��L•min�� | |
| B�� | ���������ėl����׃�����أ��tԓ�����şᷴ�� | |
| C�� | ������?q��)����ėl����׃�ǽ��͉��� | |
| D�� | ������?q��)����ėl����׃�Ǽ������ |
�鿴�𰸺ͽ���>>
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com