
分析 (1)根據質量守恒定律,生成氧氣的質量=反應前物質質量總和-反應后物質質量總和;
(2)利用氯酸鉀受熱分解的化學方程式和生成氧氣的質量,列出比例式,就可計算出參與反應的氯酸鉀質量;
(3)利用氯酸鉀受熱分解的化學方程式和生成氧氣的質量,列出比例式,就可計算出剩余固體中氯化鉀的質量.
解答 解:(1)生成氧氣的質量=60g-40.8g=19.2g;答:生成氧氣的質量19.2g;
(2)原來固體中氯酸鉀的質量為x,剩余固體中氯化鉀的質量為y
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 149 96
x y 19.2g
$\frac{245}{x}=\frac{96}{19.2g}$x=49g,答:原混合物中氯酸鉀的質量49g;
(3)$\frac{149}{y}=\frac{96}{19.2g}$,解得:y=29.8g,剩余固體中氯化鉀的質量分數$\frac{29.8g}{40.8g}$×100%≈73%,
答:剩余固體中氯化鉀的質量分數73%.
點評 本題主要考查學生利用化學方程式和質量守恒定律解答問題的能力.解題的關鍵是根據質量守恒定律求出生成氧氣的質量是解題的關鍵.


科目:高中化學 來源: 題型:選擇題
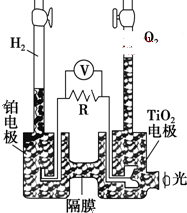 TiO2在光照射下可使水分解:2H2O$\frac{\underline{\;TiO_{2}\;}}{光}$2H2↑+O2↑,該過程類似植物的光合作用.下圖是光照射下TiO2分解水的裝置示意圖.下列敘述正確的是( )
TiO2在光照射下可使水分解:2H2O$\frac{\underline{\;TiO_{2}\;}}{光}$2H2↑+O2↑,該過程類似植物的光合作用.下圖是光照射下TiO2分解水的裝置示意圖.下列敘述正確的是( )| A. | TiO2電極上發生的反應為:2H++2e-═H2↑ | |
| B. | 該裝置工作時,TiO2電極附近溶液的pH變大 | |
| C. | 該裝置工作時,電流由TiO2電極經R流向鉑電極 | |
| D. | 該裝置可以將光能轉化為電能,同時也能將其轉化為化學能 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 18ml | B. | 大于18ml | C. | 小于18ml | D. | 無法判斷 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 能被銀氨溶液氧化 | |
| B. | 能使KMnO4酸性溶液褪色 | |
| C. | 1mol該有機物只能與1mol H2發生加成反應 | |
| D. | 1mol該有機物只能與1mol Br2發生加成反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鈉和冷水反應:Na+2H2O═Na++OH-+H2↑ | |
| B. | 金屬鋁溶于氫氧化鈉:Al+2OH-═AlO2-+H2↑ | |
| C. | 金屬鋁溶于鹽酸中2Al+6H+═2Al3++3H2↑ | |
| D. | 鐵跟稀鹽酸反應:Fe+2H+═Fe3++H2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 上述弱酸溶液的pH=4 | |
| B. | 加入NaOH溶液后,弱酸的電離平衡向右移動,K值增大 | |
| C. | 加入等體積0.01 mol•L-1 NaOH溶液后,所得溶液的pH=7 | |
| D. | 加入等體積0.01 mol•L-1 NaOH溶液后,所得溶液的pH<7 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
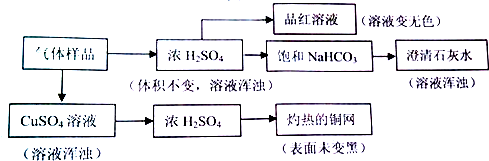
| A. | 能使品紅溶液褪色,說明原氣體樣品中至少含有Cl2或SO2 | |
| B. | 灼熱的銅網未變黑,說明原氣體樣品中一定不含有O2 | |
| C. | 澄清石灰水變渾濁,說明原氣體樣品中含有SO2,不能確定是否含有CO2 | |
| D. | 經過硫酸銅溶液,溶液變渾濁,說明原氣體樣品中含有H2S,則可排除SO2、Cl2的存在 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com