
 ,并推測1molNH4BF4(氟硼酸銨)中含有2NA個配位鍵.
,并推測1molNH4BF4(氟硼酸銨)中含有2NA個配位鍵.
分析 (1)由圖及元素守恒可寫出由B2O3制備BF3的方程式;根據價層電子對互斥理論確定構型和雜化方式;
(2)同一周期元素,元素的第一電離能隨著原子序數增大而增大,但第IIA族、第VA族元素第一電離能大于其相鄰元素,據此判斷第一電離能大小順序;
(3)在[Al(OH)4]-中Al采取sp3雜化,用最外層的四個空軌道接受O提供的孤對電子形成配合物,一個NH4BF4中N原子和其中一個H原子之間存在配位鍵、B原子和其中一個F原子之間存在一個配位鍵,所以含有2個配位鍵,據此計算;
(4)在硼原子組成的正二十面體結構中,每5個面共用一個頂點,每個等邊三角形擁有的頂點為:$\frac{1}{5}$×3=$\frac{3}{5}$,20個等邊三角形擁有的頂點為:$\frac{3}{5}$×20=12,每2個面共用一個B-B鍵;
(5)①a.由圖可知立方相氮化硼是立體網狀結構,為原子晶體;
b.非金屬元素之間易形成共價鍵;
c.六方相氮化硼為層狀結構,層間為分子間作用力,作用力小;
d.立方相氮化硼含有σ鍵不存在π鍵;
②六方相氮化硼晶體層內一個硼原子與相鄰氮原子形成3個共價單鍵,該物質的層狀結構中不存在自由移動的電子;
③氮化硼與碳元素的單質相似,結合金剛石的結構進行判斷,立方相氮化硼晶體中,每個硼原子連接12個六元環,在地殼內部,離地面越深,其壓強越大、溫度越高.
解答 解:(1)B2O3與CaF2和H2SO4反應即生成BF3,同時還應該產生硫酸鈣和水,方程式為:B2O3+3CaF2+3H2SO4=2BF3↑+3CaSO4+3H2O,BF3分子的中心原子B原子上含有3個σ 鍵,中心原子上的孤電子對數=$\frac{1}{2}$(a-xb)=$\frac{1}{2}$(0-3×1)=0,中心原子B原子的價層電子對數為3,屬于sp2雜化,中心原子上沒有孤對電子,所以其空間構型就是平面三角形,鍵角是120°,BF3分子為平面三角形,
故答案為:B2O3+3CaF2+3H2SO4=2BF3↑+3CaSO4+3H2O;sp2;平面正三角形;
(2)同一周期元素,元素的第一電離能隨著原子序數增大而增大,但第IIA族、第VA族元素第一電離能大于其相鄰元素,B、N、O、F元素處于同一周期且原子序數逐漸增大,N處于第VA族,所以第一電離能N>O,B的第一電離能最小,第一電離能由大到小的順序是:F>N>O>B,
故答案為:F>N>O>B;
(3)在[Al(OH)4]-中Al采取sp3雜化,用最外層的四個空軌道接受O提供的孤對電子形成配合物,其結構式為 ,一個NH4BF4中N原子和其中一個H原子之間存在配位鍵、B原子和其中一個F原子之間存在一個配位鍵,所以含有2個配位鍵,則1mol NH4BF4含有2mol配位鍵,即2NA個配位鍵,
,一個NH4BF4中N原子和其中一個H原子之間存在配位鍵、B原子和其中一個F原子之間存在一個配位鍵,所以含有2個配位鍵,則1mol NH4BF4含有2mol配位鍵,即2NA個配位鍵,
故答案為: ;2NA;
;2NA;
(4)在硼原子組成的正二十面體結構中,每5個面共用一個頂點,每個面擁有這個頂點的:$\frac{1}{5}$×3=$\frac{3}{5}$,20個等邊三角形擁有的頂點為:$\frac{3}{5}$×20=12,每2個面共用一個B-B鍵,每個面擁有這個B-B鍵的$\frac{1}{2}$,每個等邊三角形占有的B-B鍵為:$\frac{1}{2}$×3=$\frac{3}{2}$,20個等邊三角形擁有的B-B鍵為:$\frac{3}{2}$×20=30,
故答案為:30;
(5)①(2)a.立方相氮化硼為空間網狀結構,不存在分子,為原子晶體,故a錯誤;
b.非金屬元素之間易形成共價鍵,所以N原子和B原子之間存在共價鍵,故b正確;
c.六方相氮化硼層間為層狀結構,分子間作用力,作用力小,導致其質地軟,故c正確;
d.立方相氮化硼N原子和B原子之間存在共價單鍵,所以該化合物中含有σ鍵不存在π鍵,故d錯誤;
故選ad;
②六方相氮化硼晶體層內一個硼原子與相鄰氮原子形成3個共價單鍵,六方相氮化硼晶體內B-N鍵數與硼原子數之比為3:1,該物質的層狀結構中不存在自由移動的電子,所以不導電,
故答案為:3:1;立方氮化硼晶體內無自由移動的電子;
③氮化硼與金剛石的結構相似,立方相氮化硼晶體中,每個硼原子連接12個六元環,在地殼內部,離地面越深,其壓強越大、溫度越高,根據題干知,實驗室由六方相氮化硼合成立方相氮化硼需要的條件應是高溫高壓,
故答案為:12;高溫、高壓.
點評 本題考查了物質結構和性質,涉及第一電離能、原子的雜化方式、晶體的計算等知識點,側重于學生的分析能力和計算能力的考查,這些知識點都是高考熱點,注意價層電子對互斥理論確定原子雜化方式及分子空間構型、晶胞的計算,題目難度中等.


 學練快車道快樂假期暑假作業新疆人民出版社系列答案
學練快車道快樂假期暑假作業新疆人民出版社系列答案 浙大優學小學年級銜接導與練浙江大學出版社系列答案
浙大優學小學年級銜接導與練浙江大學出版社系列答案 小學暑假作業東南大學出版社系列答案
小學暑假作業東南大學出版社系列答案 津橋教育暑假拔高銜接廣東人民出版社系列答案
津橋教育暑假拔高銜接廣東人民出版社系列答案 波波熊暑假作業江西人民出版社系列答案
波波熊暑假作業江西人民出版社系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | X極為負極,Y極為正極 | |
| B. | 工作一段時間后,KOH的物質的量不變 | |
| C. | 電池工作時甲烷一極附近溶液的pH減小 | |
| D. | 該在標準狀況下通入5.6 L O2完全反應,則有1.0mol電子發生轉移 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 我國2015年玉月1日正式實施的《環境保護法》被稱為“史上最嚴”環保法,為保護好環境,工業生產應從源頭上減少或盡量消除生產對環境的污染 | |
| B. | 在某爆炸事故救援現場,消防員發現存放金屬鈉、電石、甲苯二異氰酸酯 等化學品的倉庫起火,應立即用泡沫滅火器將火撲滅 | |
| C. | 世界衛生組織認為青蒿素(結構如右圖所示)聯合療法是當下治療瘧疾最 有效的手段,已經拯救了上百萬生命,靑蒿素屬于烴類物質 | |
| D. | 某品牌化妝品在廣告中反復強調:“十年專注自然護膚”,該產品中不含任何化學成分 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 可用作熒光燈內壁保護層的氧化鋁納米材料屬于膠體 | |
| B. | 高分子材料可能導電,如聚乙炔 | |
| C. | 鋼化玻璃、有機玻璃、防彈玻璃均屬于硅酸鹽材料 | |
| D. | 人造剛玉的主要成分是MgO,熔點很高,可用作高級耐火材料 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 實驗操作 | 現象 | 結論 |
| A | SO2通入足量的稀Fe(NO3)3溶液 | 溶液由棕黃色變為淺綠色,但立即又變成棕黃色 | 氧化性:HNO3>稀硫酸>Fe3+ |
| B | 相同條件下,測定等濃度的Na2CO3和Na2SO3溶液的pH | 前者pH比后者的大 | 非金屬性:S>C |
| C | 將表面氧化的銅絲從酒精燈的外焰慢慢移向內焰 | 黑色的銅絲變紅色 | 氧化銅被酒精燈內焰的乙醇蒸汽還原 |
| D | 取適量NH4Al(SO4)2樣品置于試管中加水溶解,滴加少量稀NaOH溶液 | 濕潤的紅色石蕊試紙靠近試管口,試紙變藍 | NH4Al(SO4)2溶液中存在NH4+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗操作 | 實驗現象 |
| 向2mL 0.1mol/LBaCl2 溶液(填化學式)中通入SO2 | 試管內有白色沉淀產生 |
| 實驗操作 | 實驗數據 |
| 向燒杯中加入煮沸了的0.1mol/L的BaCl2溶液25mL,再加入25mL植物油,冷卻至室溫,用pH傳感器測定溶液pH隨時間(t)的變化曲線 | 圖1:向BaCl2(無氧)溶液中通入SO2 |
| 向燒杯中分別加入25mL 0.1mol/L的BaCl2溶液、Ba(NO3)2溶液,通入SO2,用pH傳感器分別測定溶液pH隨時間(t)變化的曲線. | 圖2:分別向BaCl2、Ba(NO3)2溶液中通入SO2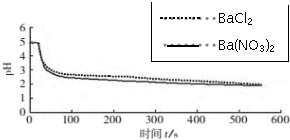 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | “霾塵積聚難見路人”,霧霾所形成的氣溶膠有丁達爾效應 | |
| B. | “熬膽礬鐵釜,久之亦化為銅”,該過程發生了置換反應 | |
| C. | “青蒿一握,以水二升漬,絞取汁”,屠呦呦對青蒿素的提取屬于化學變化 | |
| D. | 古劍“沈盧”“以劑鋼為刃,柔鐵為莖干,不爾則多斷折”,劑鋼指的是鐵的合金 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 碳碳鍵鍵長:乙烯>苯 | B. | 密度:一氯乙烷>一氯丁烷 | ||
| C. | 熱穩定性:NaHCO3>Na2CO3>H2CO3 | D. | 沸點:H2O>H2S>H2Se |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com