
| A. | 等物質的量的硫蒸氣和硫固體分別完全燃燒,后者放出熱量多 | |
| B. | 由C(石墨)=C(金剛石);△H=+1.90 kJ•mol-1可知,金剛石比石墨穩定 | |
| C. | 在稀溶液中,H+(aq)+OH-(aq)=H2O(l);△H=-57.3 kJ•mol-1,若將含0.5 mol H2SO4的濃硫酸與含1 mol NaOH的溶液混合,放出的熱大于57.3 kJ | |
| D. | 在101 kPa時,2 g H2 完全燃燒生成液態水,放出285.8 kJ熱量,氫氣燃燒的熱化學方程式表示為:2H2(g)+O2(g)=2H2O(l);△H=-285.8 kJ•mol-1 |
分析 A.硫蒸氣具有能量較高,則前者放出熱量較多;
B.物質具有能量越高,其穩定性越弱,結合該反應為放熱反應分析;
C.濃硫酸溶于水放熱,導致放出熱量增大;
D.2g氫氣的物質的量為1mol,則2mol放出的熱量為285.8×2 kJ.
解答 解:A.氣態硫的能量高于固態硫的,所以等物質的量的硫蒸氣和硫固體分別完全燃燒,前者放出熱量多,故A錯誤;
B.該反應為吸熱反應,生成物的能量高,所以石墨比金剛石穩定,故B錯誤;
C.濃硫酸溶于水放熱,含0.5 mol H2SO4的濃硫酸與含1 mol NaOH的溶液混合,放出的熱大于57.3 kJ,故C正確;
D.2g氫氣的物質的量為:$\frac{2g}{2g/mol}$=1mol,焓變與化學計量數成正比,該反應熱的數值錯誤,故D錯誤;
故選C.
點評 本題考查了熱化學方程式的書寫及應用,題目難度不大,明確物質穩定性與具有能量的關系為解答關鍵,注意熟練掌握熱化學方程式的書寫原則,試題培養了學生的靈活應用能力.


 導學全程練創優訓練系列答案
導學全程練創優訓練系列答案科目:高中化學 來源: 題型:解答題
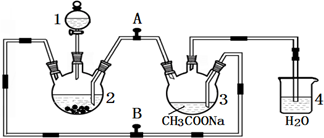 醋酸亞鉻水合物
醋酸亞鉻水合物查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 化石能源物質內部蘊涵著大量的能量 | |
| B. | 綠色植物進行光合作用時,將太陽能轉化為化學能“貯存”起來 | |
| C. | 吸熱反應中由于反應物總能量小于生成物總能量,因而沒有利用價值 | |
| D. | 物質的化學能可以在一定條件下轉化為熱能.電能為人類所利用 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
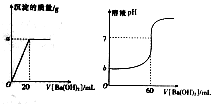 室溫下,某同學為測量硫酸和鹽酸混合溶液中溶質的濃度進行如下實驗:取混合酸20mL放入錐形瓶中,逐滴滴人0.05mol•L-1的Ba(OH)2溶液,實驗記錄如下:(1g3=0.5)
室溫下,某同學為測量硫酸和鹽酸混合溶液中溶質的濃度進行如下實驗:取混合酸20mL放入錐形瓶中,逐滴滴人0.05mol•L-1的Ba(OH)2溶液,實驗記錄如下:(1g3=0.5)查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 容器 編號 | c(H2O)/mol•L-1 | c(CO)/mol•L-1 | c(H2)/mol•L-1 | ν正、ν逆比較 |
| I | 0.06 | 0.60 | 0.10 | ν正=ν逆 |
| Ⅱ | 0.12 | 0.20 | 0.60 | ν正=ν逆 |
| Ⅲ | 0.10 | 0.20 | 0.40 | ν正>ν逆 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
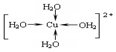 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
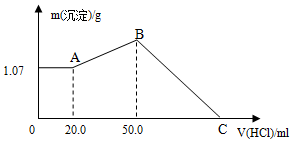 把NaOH、FeCl3、AlCl3三種固體組成的混合物溶于足量水后,產生1.07g白色沉淀,再向所得懸濁液中逐滴加入1mol/L HCl溶液,加入HCl溶液的體積與生成沉淀的關系如圖所示.試回答:
把NaOH、FeCl3、AlCl3三種固體組成的混合物溶于足量水后,產生1.07g白色沉淀,再向所得懸濁液中逐滴加入1mol/L HCl溶液,加入HCl溶液的體積與生成沉淀的關系如圖所示.試回答:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
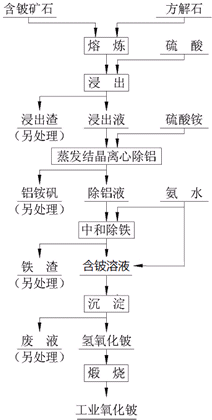 硫酸法是現代氧化鈹或氫氧化鈹生產中廣泛應用的方法之一,其原理是利用預焙燒破壞鈹礦物(綠柱石-3BeO•Al2O3•6SiO2及少量FeO等)的結構與晶型,再采用硫酸酸解含鈹礦物,使鈹、鋁、鐵等酸溶性金屬進入溶液相,與硅等脈石礦物初步分離,然后將含鈹溶液進行凈化、除雜,最終得到合格的氧化鈹( 或氫氧化鈹) 產品,其工藝流程如圖.
硫酸法是現代氧化鈹或氫氧化鈹生產中廣泛應用的方法之一,其原理是利用預焙燒破壞鈹礦物(綠柱石-3BeO•Al2O3•6SiO2及少量FeO等)的結構與晶型,再采用硫酸酸解含鈹礦物,使鈹、鋁、鐵等酸溶性金屬進入溶液相,與硅等脈石礦物初步分離,然后將含鈹溶液進行凈化、除雜,最終得到合格的氧化鈹( 或氫氧化鈹) 產品,其工藝流程如圖.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com