
| A | B | C | D | |
| 用品 |  |  |  |  |
| 主要成分 | Fe | NaHCO3 | Si | Fe2O3 |
| 用途 | 可運輸濃硫酸 | 發酵 | 光導纖維 | 涂料 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.常溫下濃硫酸和Fe發生鈍化現象;
B.NaHCO3是發酵粉的主要成分之一,主要是利用其受熱易分解的性質;
C.光導纖維的主要成分是二氧化硅;
D.Fe2O3是紅棕色固體,能作涂料等.
解答 解:A.常溫下濃硫酸和Fe發生氧化還原反應生成一層致密的氧化物薄膜而阻止進一步被氧化,該現象為鈍化現象,所以常溫下可以用鐵制容器運輸濃硫酸,故A正確;
B.NaHCO3是發酵粉的主要成分之一,主要是利用其受熱易分解的性質,碳酸氫鈉受熱分解生成碳酸鈉、二氧化碳和水,故B正確;
C.光導纖維的主要成分是二氧化硅,Si能作太陽能電池、硅芯片、半導體材料等,故C錯誤;
D.Fe2O3是紅棕色固體,能作涂料、油漆等,故D正確;
故選C.
點評 本題考查物質用途,明確物質性質是解本題關鍵,性質決定用途,用途體現性質,知道常見物質性質,題目難度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 烯烴各同系物中碳的質量分數相等 | |
| B. | C2H4和C4H8一定是同系物 | |
| C. | 分子量相同的兩種物質不一定是同分異構體 | |
| D. | C2H6和C4H10一定是同系物 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
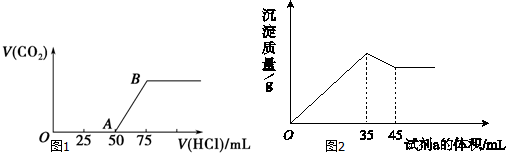
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
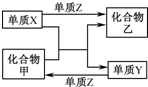 X、Y、Z是三種常見的單質,甲、乙是兩種常見的化合物.下表各組物質之間通過一步反應不能實現如圖所示轉化的是( )
X、Y、Z是三種常見的單質,甲、乙是兩種常見的化合物.下表各組物質之間通過一步反應不能實現如圖所示轉化的是( )| 選項 | X | Y | Z | 甲 | 乙 |
| A | Fe | H2 | O2 | H2O | Fe3O4 |
| B | Mg | C | O2 | CO2 | MgO |
| C | Zn | Fe | Cl2 | FeCl2 | ZnCl2 |
| D | Cl2 | N2 | H2 | NH3 | HCl |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
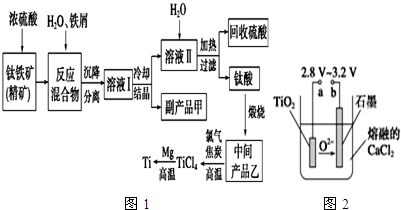
| 氫氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
| Ksp | 8.0×10-16 | 1.0×10-29 | 1.8×10-11 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na+、Ca2+、Cl-、AlO2- | B. | Ba2+、K+、OH-、NO3- | ||
| C. | Al3+、Cu2+、SO42-、Cl- | D. | NH4+.、Mg2+、SO42-、Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.2L | B. | 0.5L | C. | 0.65L | D. | 0.8L |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com