
| A. | 電解精煉銅時,若轉移了NA個電子,則陰極析出32 g銅 | |
| B. | 標準標況下,33.6 L三氧化硫中含有1.5NA個三氧化硫分子 | |
| C. | 1 mol Cl2與過量的鐵反應,轉移3NA個電子 | |
| D. | 1 mol FeCl3跟水反應,完全轉化為氫氧化鐵膠體后,其中膠體粒子的數目為NA |
分析 A、電解精煉銅時,陰極反應為:Cu2++2e-=Cu;
B、標況下三氧化硫為固體;
C、氯氣和鐵反應后變為-1價;
D、一個氫氧化鐵膠粒是多個氫氧化鐵的聚集體.
解答 解:A、電解精煉銅時陽極電極反應:Cu-2e-═Cu2+,Fe-2e-═Fe2+,Zn-2e-═Zn2+,Ni-2e-═Ni2+,陰極電極反應為Cu2++2e-═Cu,若陰極得到電子數為NA個,依據電子守恒,則陰極析出32 g銅,故A正確;
B、標準狀況下,三氧化硫不再是氣體,不能用氣體摩爾體積計算,故B錯誤;
C、1 mol Cl2與過量的鐵反應后變為-1價,故1mol氯氣轉移2NA個電子,故C錯誤;
D、氫氧化鐵膠體粒子是氫氧化鐵形成的集合體,故膠粒數一定小于NA,故D錯誤.
故選A.
點評 本題考查了阿伏伽德羅常數的有關計算,熟練掌握公式的使用和物質的結構是解題關鍵,難度不大.


科目:高中化學 來源: 題型:解答題


 +HO-NO2$→_{△}^{濃H_{2}SO_{4}}$
+HO-NO2$→_{△}^{濃H_{2}SO_{4}}$ +H2O.
+H2O. .
. (寫出其中一種的結構簡式).
(寫出其中一種的結構簡式).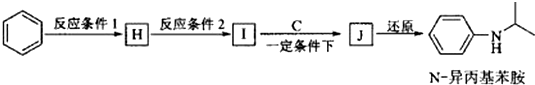
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 純凈物 | B. | 混合物 | C. | 化合物 | D. | 單質 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題

| A. | 羥氨芐青霉素在空氣中不能很穩定地存在 | |
| B. | 每個羥氨芐青霉素分子中含有3個手性碳原子 | |
| C. | 羥氨芐青霉素既能與鹽酸反應,又能與碳酸氫鈉溶液反應 | |
| D. | 羥氨芐青霉素可以與FeCl3發生顯色反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鋁和氫氧化鈉溶液反應生成Al(OH)3和Na | |
| B. | 鈉在空氣中燃燒生成淡黃色的NaO2 | |
| C. | 鐵在高溫下與水蒸氣反應生成Fe3O4和H2 | |
| D. | 用碳酸鈉和氫氧化鈣反應制NaHCO3 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com