
【題目】氟及其化合物用途非常廣泛。回答下列問題:
(1)聚四氟乙烯商品名稱為“特氟龍”,可做不粘鍋涂層。它是一種準晶體,該晶體是一種無平移周期序、但有嚴格準周期位置序的獨特晶體。可通過____方法區分晶體、準晶體和非晶體。
(2)基態銻(Sb)原子價電子排布的軌道式為____。[H2F]+[SbF6]-(氟酸銻)是一種超強酸,存在[H2F]+,該離子的空間構型為______,依次寫出一種與[H2F]+具有相同空間構型和鍵合形式的分子和陰離子分別是_______、_________。
(3)硼酸(H3BO3)和四氟硼酸銨(NH4BF4)都有著重要的化工用途。
①H3BO3和NH4BF4涉及的四種元素中第二周期元素的第一電離能由大到小的順序_____(填元素符號)。
②H3BO3本身不能電離出H+,在水中易結合一個OH﹣生成[B(OH)4]﹣,而體現弱酸性。[B(OH)4]﹣中B原子的雜化類型為_____。
③NH4BF4(四氟硼酸銨)可用作鋁或銅焊接助熔劑、能腐蝕玻璃等。四氟硼酸銨中存在_______(填序號):
A.離子鍵 B.σ鍵 C.π鍵 D.配位鍵 E.范德華力
(4)某砷鎳合金的晶胞如圖所示,設阿伏加德羅常數的值為NA,該晶體的密度ρ=____g/cm3。

【答案】X-射線衍射 ![]() V型 H2O NH2- F>N>O>B sp3 ABD
V型 H2O NH2- F>N>O>B sp3 ABD ![]()
【解析】
(1)晶體對X射線發生衍射,非晶體不發生衍射,準晶體介于二者之間;
(2)Sb的價電子為5s能級上2個電子、5p能級上3個電子;
[H2F]+與H2O、NH2-等互為等電子體,結構相似;
(3)①涉及的第二周期元素有B、N、O、F元素,第二周期元素第一電離能隨著原子序數增大而呈增大趨勢,但第IIA族、第VA族元素第一電離能大于相鄰元素;
②[B(OH)4]-中B原子價層電子對個數是4,根據價層電子對互斥理論判斷B原子雜化類型;
③NH4BF4中陰陽離子之間存在離子鍵,N原子和H原子之間存在共價鍵且其中一個是配位鍵,B原子和F原子之間存在共價鍵且其中一個是配位鍵,共價單鍵為σ鍵;
(4)先根據均攤方法確定晶胞中含有的As、Ni原子個數,在計算晶胞的體積,最后根據![]() 計算。
計算。
(1)從外觀無法區分三者,但用X光照射會發現:晶體對X射線發生衍射,非晶體不發生衍射,準晶體介于二者之間,因此通過有無X射線衍射現象即可確定;
(2)Sb的價電子為5s能級上2個電子、5p能級上3個電子,所以其價電子軌道式為![]() ;
;
[H2F]+與H2O、NH2-等互為等電子體,結構相似,為V形;
(3)①涉及的第二周期元素有B、N、O、F元素,第二周期元素第一電離能隨著原子序數增大而呈增大趨勢,但第IIA族元素的原子核外處于其軌道的全充滿穩定狀態、第VA族元素原子核外電子處于其軌道的半充滿的穩定狀態,因此它們的第一電離能大于相鄰元素,B、N、O、F分別位于第IIIA族、第VA族、第VIA族、第VIIA族,所以第一電離能大小順序為F>N>O>B;
②[B(OH)4]-中B原子價層電子對個數是4,根據價層電子對互斥理論判斷B原子雜化類型為sp3雜化;
③NH4BF4中陰、陽離子之間存在離子鍵,N原子和H原子之間存在共價鍵結合且其中有一個是配位鍵,B原子和F原子之間存在共價鍵且其中一個是配位鍵,共價單鍵為σ鍵,所以四氟硼酸銨中存在離子鍵、σ鍵、配位鍵,故合理選項是ABD;
(4)根據砷鎳合金的晶胞示意圖可知該晶胞中As原子個數是2、Ni原子個數=4×![]() +4×
+4×![]() +2×
+2×![]() +2×
+2×![]() =2,其體積=(a×10-10cm×a×10-10cm×
=2,其體積=(a×10-10cm×a×10-10cm×![]() )×c×10-10 cm=
)×c×10-10 cm=![]() a2c×10-30cm3,晶胞密度ρ=
a2c×10-30cm3,晶胞密度ρ= g/cm3=
g/cm3=![]() g/cm3。
g/cm3。


 通城學典默寫能手系列答案
通城學典默寫能手系列答案科目:高中化學 來源: 題型:
【題目】0.2 mol某烴A在氧氣中充分燃燒后,生成化合物B、C各1.2 mol。試回答:
(1)烴A的分子式為________。
(2)若烴A不能使溴水褪色,但在一定條件下,能與氯氣發生取代反應,其一氯代物只有一種,則烴A的結構簡為_____________。
(3)若烴A能使溴水褪色,在催化劑作用下,與H2加成,其加成產物經測定分子中含有4個甲基,烴A可能有的結構簡式為______________。
(4)比烯烴A少2個碳原子的同系物有________種同分異構體(不考慮順反異構),其中能和H2發生加成反應生成2-甲基丙烷的烯烴的名稱是________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關圖像的說法正確的是
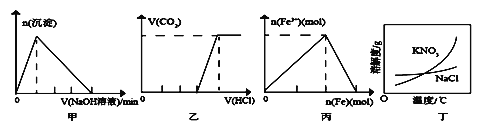
A. 圖甲表示:向某明礬溶液中逐滴加入NaOH溶液至過量,生成沉淀的物質的量與滴加NaOH溶液體積的關系
B. 圖乙表示:向含等物質的量的NaOH和Na2CO3的混合溶液中逐滴加入稀鹽酸至過量,生成氣體的體積與滴加HCl溶液體積的關系
C. 圖丙表示:在稀硝酸溶液中逐漸加入鐵粉至過量,溶液中Fe3+物質的量與逐漸加入鐵粉物質的量的變化關系
D. 除去混在硝酸鉀中少量的氯化鈉可用“蒸發濃縮、趁熱過濾”的方法
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】廢易拉罐的成分比較復雜,據查,鋁易拉罐各部分成分及含量(質量百分含量)見表:
Si | Fe | Cu | Mn | Mg | Cr | Zn | Ti | Al | |
罐身/% | 0.3 | 0.7 | 0.25 | 0.25 | 1.0~1.5 | - | - | - | 其余 |
罐蓋/% | 0.2 | 0.35 | 0.15 | 0.2~0.5 | 4.0~5.0 | - | 0.1 | 0.25 | 其余 |
拉環/% | 0.2 | 0.35 | 0.15 | 0.2~0.5 | 3.0~4.0 | 0.1 | 0.25 | 0.1 | 其余 |
為了驗證罐身的組成成分,進行了如下實驗:
(實驗儀器與藥品)
儀器:酒精燈、燒杯、試管、試管夾、漏斗、濾紙、鐵圈、玻璃棒、砂紙、剪刀
藥品:易拉罐、去污粉、NaOH溶液、KSCN溶液、鹽酸、鎂試劑、高碘酸(H5IO6,弱酸)
(實驗方案)
實驗預處理。將剪好的易拉罐片用砂紙打磨,除去表面的涂料層,直到光亮后用去污粉清洗干凈備用。
(實驗過程)分別向試管a、b中加入少量上述易拉罐片,進行如下操作:

請填寫下列空白:
(1)圖中操作①②所用到的玻璃儀器有______________________________。
(2)沉淀A的成分為________。
(3)操作③觀察到的現象為_____________________________________;反應的離子方程式為____________________________________________。
(4)若試管a、b中取樣量相等,則分別加入過量的NaOH溶液、稀鹽酸后,相同條件下理論上產生的氣體體積V(a)________V(b)(填“<”、“>”或“=”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某小組設計如圖裝置(部分夾持裝置已略去),以探究潮濕的Cl2與Na2CO3反應得到固體物質的成分。

(1)試劑X的化學式________。A中制取Cl2的離子方程式____________________。
(2)試劑Y的名稱為______________。
(3)通入一定量潮濕的Cl2反應后,經檢測,D中只有Cl2O一種氣體,C中除含一種氯鹽外,同時含有NaHCO3等,某同學對C中所得固體殘渣的成分進行探究。
①提出合理假設。
假設1:存在兩種成分:NaHCO3和____________________________;
假設2:存在三種成分:NaHCO3和__________________________。
②設計方案,進行實驗。寫出實驗步驟以及預期現象和結論。_______
限選實驗試劑和儀器:蒸餾水、稀硝酸、BaCl2溶液、澄清石灰水、AgNO3溶液、試管、小燒杯。

(4)已知Cl2O與水反應生成次氯酸,則D中Cl2O進入E反應的化學方程式為____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2005年諾貝爾化學獎授予了研究烯烴復分解反應的科學家,以表彰他們作出的卓越貢獻。烯烴復分解反應原理如下:C2H5CH=CHCH3+CH2=CH2![]() C2H5CH=CH2+CH2=CHCH3
C2H5CH=CH2+CH2=CHCH3
現以烯烴C5H10為原料,合成有機物M和N,合成路線如下:

(1)按系統命名法,有機物A的名稱是_______。
(2)B的結構簡式是__________。
(3)C![]() D的反應類型是___________。
D的反應類型是___________。
(4)寫出D![]() M的化學方程式________。
M的化學方程式________。
(5)已知X的苯環上只有一個取代基,且取代基無甲基,則N的結構簡式為_______。
(6)滿足下列條件的X的同分異構體共有_______種,寫出任意一種的結構簡式_________。
①遇FeCl3溶液顯紫色 ②苯環上的一氯取代物只有兩種
(7)寫出E![]() F合成路線(用結構簡式表示有機物,箭頭上注明試劑和反應條件)。______
F合成路線(用結構簡式表示有機物,箭頭上注明試劑和反應條件)。______
![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定條件下可實現圖所示的物質之間的變化:

據此回答下列問題:
(1)I、II、III、IV四步操作采取的分離方法是___。
(2)根據上述框圖反應關系,寫出下列B、C、E所含物質的化學式
沉淀固體B___;C___;E___
(3)寫出①、④四個反應方程式(是離子反應的寫離子方程式)
①___;④___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫,下列各組離子一定能在指定溶液中大量共存的是( )
A.![]() =10-12的溶液中:
=10-12的溶液中:![]() 、Cu2+、
、Cu2+、![]() 、
、![]()
B.滴加KSCN溶液顯紅色的溶液中:![]() 、K+、Cl-、I-
、K+、Cl-、I-
C.0.1mol·L-1的NaHCO3溶液中:Fe3+、K+、Cl-、![]()
D.水電離產生的c(OH-)=10-12mol·L-1的溶液中:Na+、Al3+、Cl-、![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硅是信息產業、太陽能電池光電轉化的基礎材料。鋅還原四氯化硅是一種有著良好應用前景的制備硅的方法,該制備過程示意如下:

(1)焦炭在過程Ⅰ中作______劑。
(2)過程Ⅱ中的Cl2用電解飽和食鹽水制備,制備Cl2的化學方程式是____。
(3)整個制備過程必須嚴格控制無水。
①SiCl4遇水劇烈水解生成SiO2和一種酸,反應的化學方程式是_____。
②干燥Cl2時,從有利于充分干燥和操作安全的角度考慮,需將約90℃的潮濕氯氣先冷卻至12℃,然后再通入到濃H2SO4中。冷卻的作用是____。
(4)Zn還原SiCl4的反應如下:
反應1: 400℃~756℃ ,SiCl4(g) + 2Zn(l)![]() Si(s) + 2ZnCl2(l) ΔH1<0
Si(s) + 2ZnCl2(l) ΔH1<0
反應2: 756℃~907℃ ,SiCl4(g) + 2Zn(l)![]() Si(s) + 2ZnCl2(g) ΔH2<0
Si(s) + 2ZnCl2(g) ΔH2<0
反應3: 907℃~1410℃,SiCl4(g) + 2Zn(g)![]() Si(s) + 2ZnCl2(g) ΔH3<0
Si(s) + 2ZnCl2(g) ΔH3<0
① 對于上述三個反應,下列說法合理的是_____。
a.升高溫度會提高SiCl4的轉化率 b.還原過程需在無氧的氣氛中進行
c.增大壓強能提高反應的速率 d.Na、Mg可以代替Zn還原SiCl4
② 實際制備過程選擇“反應3”,選擇的理由是____。
③ 已知Zn(l)=Zn(g) ΔH = +116 KJ/mol 。若SiCl4的轉化率均為90%,每投入1mol SiCl4,“反應3”比“反應2”多放出_____kJ的熱量。
(5)用硅制作太陽能電池時,為減弱光在硅表面的反射,采用化學腐蝕法在其表面形成粗糙的多孔硅層。腐蝕劑常用稀HNO3和HF的混合液。硅表面首先形成SiO2,最后轉化為H2SiF6。用化學方程式表示SiO2轉化為H2SiF6的過程_____。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com