
分析 根據價層電子對互斥理論確定中心原子雜化方式,價層電子對個數(n)=配原子個數+孤電子對個數.
根據n值判斷雜化類型:一般有如下規律:當n=2,sp雜化;n=3,sp2雜化;n=4,sp3雜化;sp3雜化是四面體構型,sp2雜化,分子呈平面三角形.
解答 解:甲醛中C原子形成3個σ鍵,為sp2雜化,是平面三角形結構,鍵角為120°,甲醇分子內碳原子形成4個σ鍵,無孤電子對,雜化方式為sp3雜化,是四面體結構,O-C-H鍵角約為109°28′,鍵角小于120°,所以甲醇分子內O-C-H鍵角比甲醛分子內O-C-H鍵角小,
故答案為:sp3;小于.
點評 本題考查了原子的雜化方式,題目難度不大,注意把握價層電子對數的判斷方法.


 一本好題口算題卡系列答案
一本好題口算題卡系列答案科目:高中化學 來源: 題型:選擇題
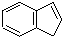 .下列關于茚的說法中不正確的是( )
.下列關于茚的說法中不正確的是( )| A. | 茚能使酸性高錳酸鉀溶液褪色 | |
| B. | 茚能使溴的四氯化碳溶液褪色 | |
| C. | 1 mol茚只含有1 mol碳碳雙鍵 | |
| D. | 茚中所有的原子均可能處在同一平面上 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.80g | B. | 0.02g | C. | 0.23g | D. | 0.46g |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| A | 完全燃燒的產物中n(CO2):n(H2O)=2:1 28<Mr(A)<60 不能使溴的四氯化碳溶液褪色 一氯代物只有1種結構 |
| B | 飽和鏈烴,通常情況下呈氣態 二溴代物有3種 |
 ;
;查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 化合物:干冰、冰水共存物、燒堿、小蘇打 | |
| B. | 非電解質:乙醇、四氯化碳、氯氣、葡萄糖 | |
| C. | 同素異形體:活性炭、C60、石墨烯、金剛石 | |
| D. | 混合物:鋁熱劑、純凈礦泉水、分析純鹽酸、漂白粉 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com