
分析 (1)電解質是指:在水溶液中或熔融狀態下能夠導電的化合物.電解質水溶液中或熔融狀態下能夠導電,是因電解質自身可以離解成自由移動的離子;
強電解質是在水溶液中或熔融狀態下能完全電離的電解質,包括強酸、強堿、活潑金屬氧化物和大部分鹽;
弱電解質是在水溶液中不能完全電離的電解質,包括弱酸、弱堿、水等;
非電解質是指:在水溶液里和熔融狀態下都不導電的化合物,非金屬氧化物、大多數的有機物(如蔗糖、乙醇等),單質,混合物既不是電解質也不是非電解質;
(2)酸性溶液的pH<7、中性溶液的pH=7、堿性溶液的pH>7,且酸性越強,溶液的pH越小,堿性越強,溶液的pH越大;先根據溶液酸堿性對各物質進行分類,然后判斷溶液pH大小;
(3)在Na2S溶液中,硫離子是多元弱酸陰離子,水解分步進行以第一步為主;當向H2S溶液中加入NaOH固體時,OH-與H+反應,硫化氫的電離平衡正移.
解答 解:(1)①石墨是非金屬單質,但它既不是電解質也不是非電解質;
②三氧化硫在水溶液中與水反應生成亞硫酸酸,亞硫酸酸電離出自由移動的離子導電,三氧化硫自身不能電離,三氧化硫是非電解質;
③氯氣是單質,它既不是電解質也不是非電解質;
④熔融的硫酸鉀中有自由移動的離子,硫酸鉀在水溶液中能完全電離出自由移動的陰陽離子而使其導電,所以熔融的硫酸鉀是強電解質;
⑤食鹽在水溶液中能完全電離出自由移動的陰陽離子而使其導電,所以食鹽是強電解質;
⑥硫酸溶液是混合物,既不是電解質也不是非電解質;
⑧乙醇是化合物,其水溶液只以乙醇分子存在,不導電,乙醇屬于非電解質;
⑨冰醋酸為醋酸(CH3COOH),在水溶液中能部分電離出自由移動的陰陽離子而使其導電,所以冰醋酸是弱電解質;
⑩一水合氨是化合物,無自由移動的離子不導電;但在水溶液中,NH3•H2O?NH4++OH-,屬于弱電解質;
故答案為:④⑤;⑨⑩;②⑧;
(2)溶液的物質的量濃度均為0.1mol•L-1①HCl ②NaOH③CH3COOH④KCl,①為強酸,其溶液pH最小;②為強堿,其溶液的pH最大;③為弱酸,其溶液的pH僅大于HCl;④為中性溶液,則按pH由小到大的排列順序為:①③④②,
故答案為:①③④②;
(3)H2S是二元弱酸,屬弱電解質,分兩步電離,第一步電離出氫離子和硫氫根離子,第二步電離為硫氫根離子電離出硫離子和氫離子;
H2S溶液中存在著H2S=H++HS-、HS-=H++S2-的平衡當向H2S溶液中加入NaOH固體時,OH-與H+反應,減少生成物的濃度,平衡向右移動,
故答案為:H2S?H++HS-、HS-?H++S2-;右.
點評 本題考查了弱電解質的電離平衡及其影響、電解質與電解質、強電解質與弱電解質的判斷、溶液pH大小比較等知識,題目難度中等,明確電解質與非電解質、強電解質與弱電解質的概念為解答關鍵,注意掌握電離平衡及其影響,試題培養了學生的靈活應用能力.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:解答題
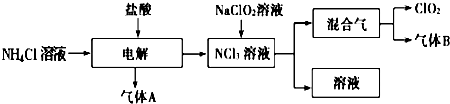
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
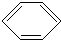 +Cl2
+Cl2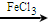
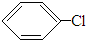 +HCl
+HCl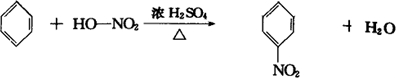
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
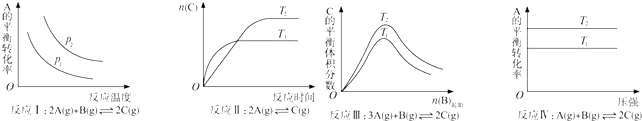
| A. | 反應Ⅰ:△H>0,P2>P1 | B. | 反應Ⅱ:△H<0,T1>T2 | ||
| C. | 反應Ⅲ:△H>0,T2<T1;或△H<0,T2>T1 | D. | 反應Ⅳ:△H<0,T2>T1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
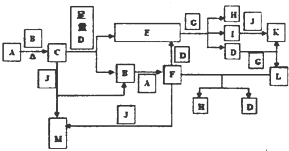
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com