
【題目】工業上常將鉻鍍在其他金屬表面,同鐵、鎳組成各種性質的不銹鋼,在下圖裝置中,觀察到圖1裝置銅電極上產生大量的無色氣泡,而圖2裝置中銅電極上無氣體產生,鉻電極上產生大量有色氣體,則下列敘述正確的是( )
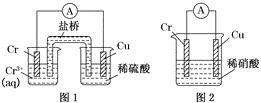
A. 圖1為原電池裝置,Cu電極上產生的是O2
B. 圖2裝置中Cu電極上發生的電極反應式為:Cu-2e-=Cu2+
C. 由實驗現象可知:金屬活動性Cu>Cr
D. 兩個裝置中,電子均由Cr電極流向Cu電極
科目:高中化學 來源: 題型:
【題目】以廢舊鋅錳電池初步處理分選出的含錳廢料(MnO2、MnOOH、MnO及少量Fe、Pb等)為原料制備高純MnCl2·xH2O,實現錳的再生利用。其工作流程如下:
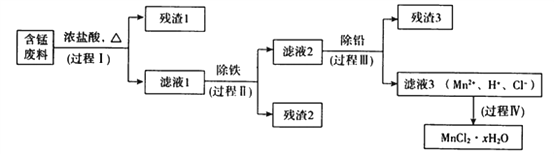
資料a.Mn的金屬活動性強于Fe;Mn2+在酸性條件下比較穩定,pH高于5.5時易被O2氧化。
資料b.生成氫氧化物沉淀的pH
Mn(OH)2 | Pb(OH)2 | Fe(OH)3 | |
開始沉淀時 | 8.1 | 6.5 | 1.9 |
完全沉淀時 | 10.1 | 8.5 | 3.2 |
注:金屬離子的起始濃度為0.1 mol·L-1
(1)過程Ⅰ的目的是浸出錳。經檢驗濾液1中含有的陽離子為Mn2+、Fe3+、Pb2+和H+。
①MnOOH與濃鹽酸反應的離子方程式是_______________________________。
②檢驗濾液1中只含Fe3+不含Fe2+的操作和現象是:_________________________________________。
③Fe3+由Fe2+轉化而成,可能發生的反應有:
a.2Fe2++Cl2=2Fe3+2Cl-
b.4Fe2++O2+4H+=2Fe3++2H2O
c.……
寫出c的離子方程式:____________________。
(2)過程Ⅱ的目的是除鐵。有如下兩種方法,
ⅰ.氨水法:將濾液1先稀釋,再加適量10%的氨水,過濾。
ⅱ.焙燒法:將濾液1濃縮得到的固體于290℃焙燒,冷卻,取焙燒物,加水溶解,過濾,再加鹽酸酸化至pH小于5.5。
已知:焙燒中發生的主要反應為2FeCl3+3O2=2Fe2O3+3Cl2,MnCl2和PbCl2不發生變化。
①氨水法除鐵時,溶液pH應控制在_____________之間。
②兩種方法比較,氨水法除鐵的缺點是____________。
(3)過程Ⅲ的目的是除鉛。加入的試劑是____________。
(4)過程Ⅳ所得固體中的x的測定如下,取m1g樣品,置于氯化氫氛圍中加熱至失去全部結晶水時,質量變為m2g。則x=____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2019年9月12日11時26分,我國在太原衛星發射中心用長征四號乙運載火箭,成功將資源一號02D衛星發射升空。資源一號02D衛星將為國家自然資源資產管理和生態監理工作提供穩定的數據保障,同時兼顧防災減災、環境保護、城鄉建設、交通運輸、應急管理等相關領域應用需求。
(1)衛星改變運行的路線時需要噴火消耗燃料,其燃料一般是肼(N2H4)。肼中N的化合價是___,肼在空氣中燃燒的化學方程式如下,請用雙線橋法標出該反應中電子轉移的方向和數目___。
N2H4+O2![]() N2+2H2O
N2+2H2O
該反應中的氧化劑是___,被氧化的元素是___,每生成1molH2O轉移電子___mol。
(2)近幾年來,太原市在環境保護方面采取了一系列措施,其中的噴霧車、灑水車都是為了降低空氣中的粉塵。含有粉塵的空氣是否屬于膠體___(填“是”或“否”),證明的方法是___,觀察到的現象是___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】加碘食鹽是含KIO3的食鹽,其中KIO3可由反應KI+3Cl2+3H2O=KIO3+6HCl制取。市面上銷售的加碘食鹽中的碘元素含量為20~50mg/kg。請計算:制取1000kg含碘元素25.4mg/kg的加碘食鹽,需要消耗Cl2的體積是多少___?(標準狀況)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是工業利用菱鎂礦(主要含MgCO3,還含有Al2O3、FeCO3雜質)制取氯化鎂的工藝流程。
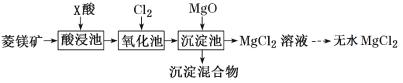
下列說法不正確的是
A.酸浸池中加入的X酸是硝酸
B.氧化池中通入氯氣的目的是將Fe2+氧化為Fe3+
C.生成的沉淀物為Fe(OH)3和Al(OH)3
D.在工業上常利用電解熔融氯化鎂的方法制取金屬鎂
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某一反應體系中有反應物和生成物共5種物質:H2S+HNO3→S+NO+H2O;下列說法中正確的是( )
A.該反應中的還原產物是S
B.若反應過程中轉移了0.3 mol 電子,則氧化產物的質量9.6g
C.氧化劑與還原劑的物質的量之比為2∶3
D.反應后溶液的酸性明顯增強
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用CaSO4代替O2與燃料CO反應,既可以提高燃燒效率,又能得到高純CO2,是一種高效、清潔、經濟的新型燃燒技術,反應①為主反應,反應②和③為副反應。
①1/4CaSO4(s)+CO(g) ![]() 1/4CaS(s)+CO2(g) △H1=-47.3kJ/mol
1/4CaS(s)+CO2(g) △H1=-47.3kJ/mol
②CaSO4(s)+CO(g) ![]() CaO(s)+ CO2(g)+ SO2(g) △H2=+210.5kJ/mol
CaO(s)+ CO2(g)+ SO2(g) △H2=+210.5kJ/mol
③CO(g)![]() 1/2C(s)+1/2CO2(g) △H3=-86.2kJ/mol
1/2C(s)+1/2CO2(g) △H3=-86.2kJ/mol
(1)反應2 CaSO4(s)+7CO(g) ![]() CaS(s)+CaO(s)+C(s)+6CO2(g)+SO2(g)的△H=_______________(用△H1、△H2和△H3表示)。
CaS(s)+CaO(s)+C(s)+6CO2(g)+SO2(g)的△H=_______________(用△H1、△H2和△H3表示)。
(2)為減少副產物,獲得更純凈的CO2,可在初始燃料中適量加入__________________。
(3)以反應①中生成的CaS為原料,在一定條件下經原子利用率100%的高溫反應,可再生成CaSO4,該反應的化學方程式為___________;在一定條件下CO2可與對二甲苯反應,在其苯環上引入一個羧基,產物的結構簡式為_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】含有11.2 g KOH的稀溶液與1 L 0.1 molL﹣1的H2SO4溶液反應,放出11.46 kJ的熱量,下列熱化學方程式正確的是
A. KOH(aq)+![]() H2SO4(aq) ===
H2SO4(aq) === ![]() K2SO4(aq)+H2O(l) ΔH =-11.46 kJmol﹣1
K2SO4(aq)+H2O(l) ΔH =-11.46 kJmol﹣1
B. 2KOH(aq)+H2SO4(aq) === K2SO4(aq)+2H2O(l) ΔH =-11.46 kJmol﹣1
C. 2KOH(aq)+H2SO4(aq) === K2SO4(aq)+2H2O(l) ΔH =+114.6 kJmol﹣1
D. KOH(aq)+![]() H2SO4(aq) ===
H2SO4(aq) === ![]() K2SO4(aq)+H2O(l) ΔH =-57.3 kJmol﹣1
K2SO4(aq)+H2O(l) ΔH =-57.3 kJmol﹣1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究和開發CO、CO2的應用及水體污染的治理是化學工作者研究的重要課題。
(1)水體常見污染物之一的氨氮主要指游離氨或銨鹽,可以通入一定量的氯氣,利用產生的HClO除去。已知: NH4++HClO=NH2Cl+H++H2O;ΔH=a kJ·mol-1
NH4++4HClO=NO3- +6H++4Cl-+H2O;ΔH=b kJ·mol-1。
2NH2Cl+HClO=N2+H2O+3H++3Cl-;ΔH=c kJ·mol-1
則2NH4++3HClO=N2+3H2O+5H++3Cl-;ΔH=_____ kJ·mol-1
(2)將CO2與金屬鈉組合設計成Na-CO2電池,很容易實現可逆的充、放電反應,該電池反應為4Na+3CO2![]() 2Na2CO3+C。放電時當電路中轉移1mol電子時被還原的CO2的質量為_____;充電時,陽極的反應式為________
2Na2CO3+C。放電時當電路中轉移1mol電子時被還原的CO2的質量為_____;充電時,陽極的反應式為________
(3)廢水中重金屬離子常用沉淀法除去,已知Ksp(NiS)=1.1×10-21,Ksp(CuS)=1.3×10-36,國家規定的排放標準:鎳低于1.1×10-5 mol·L-1,銅低于7.8×10-5 mol·L-1。則需要控制溶液中S2-的濃度不低于_____________mol·L-1。
(4)NO易被O2氧化為NO2。其他條件不變時,NO的氧化率α(NO)與溫度、壓強的關系如圖1所示(p1線在p2的上方)則p1__p2(填“>”、“<”或“=”);溫度高于800℃時,α(NO)幾乎為0的原因是____
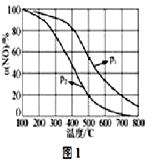
(5)環境中的有害物質常通過轉化為CO2來降低污染,TiO2是一種性能優良的半導體光催化劑,能有效地將有機污染物轉化為CO2等小分子物質。下圖2為在TiO2的催化下,O3降解CH3CHO的示意圖,則該反應的化學方程式為_____。
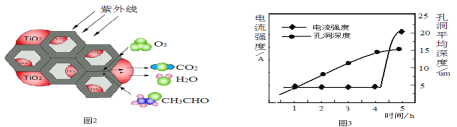
(6)用新型鈦基納米PbO2作電極可將苯、酚類等降解為CO2 和H2O。該電極可通過下面過程制備:將鈦基板用丙酮浸泡后再用水沖洗,在鈦板上鍍上一層鋁膜。用它做陽極在草酸溶液中電解,一段時間后,鋁被氧化為氧化鋁并同時形成孔洞。再用Pb(NO3)2溶液處理得納米PbO2,除去多余的氧化鋁,獲得鈦基納米PbO2電極。電解時,電流強度和基板孔洞深度隨時間變化如上圖3所示,氧化的終點電流強度突然增加,其可能的原因是____。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com