
【題目】NA為阿伏加德羅常數(shù),下列說法正確的是( )
A.14g乙烯、丙烯、丁烯的混合氣體中所含原子數(shù)為3NA
B.28g乙烯所含共用電子對數(shù)目為4NA
C.標準狀況下,11.2L氯仿所含分子數(shù)為0.5NA
D.32g甲醇中含有C—H鍵數(shù)目為4NA
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】標準狀況下,向2mol·L-1的NaOH溶液100mL中緩緩通入4.48LCO2氣體,充分反應后溶液中離子濃度大小排列順序正確的是
A.c(Na+)>c(![]() )>c(OH-)>c(H+)B.c(Na+)+ c(H+)=c(
)>c(OH-)>c(H+)B.c(Na+)+ c(H+)=c(![]() )+ c(OH-)
)+ c(OH-)
C.c(Na+)>c(![]() )>c(H+)>c(OH-)D.c(Na+)=c(
)>c(H+)>c(OH-)D.c(Na+)=c(![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,將2 mol A和1 mol B放入一密閉容器中,發(fā)生反應:A(g)+B(g)![]() 2C(s)+2D(g),5 min后反應達到平衡,測得生成C為0.8 mol,下列相關表述正確的是
2C(s)+2D(g),5 min后反應達到平衡,測得生成C為0.8 mol,下列相關表述正確的是
A.該反應的化學平衡常數(shù)表達式是K=![]()
B.該條件下B的平衡轉(zhuǎn)化率是40%
C.增大該體系的壓強,A的轉(zhuǎn)化率增大
D.若向平衡體系中加入少量生成物C,則正、逆反應速率均增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】近幾年,節(jié)能減排、提高原料利用率來提高經(jīng)濟效益成為人們關注的焦點。某化工廠利用甲烷與氯氣反應得到的副產(chǎn)品來制取鹽酸實現(xiàn)了變廢為寶的夢想,其生產(chǎn)原理可在實驗室中模擬如圖,請根據(jù)要求填空:

(1)B裝置有三種功能:①控制氣流速度;②均勻混合氣體;③__________。
(2)設![]() =x,若理論上欲獲得最多的氯化氫,則x值應_________。
=x,若理論上欲獲得最多的氯化氫,則x值應_________。
(3)在C裝置中,經(jīng)過一段時間的強光照射后,發(fā)現(xiàn)硬質(zhì)玻璃管內(nèi)壁附著有油珠,生成的油狀液滴中的氯仿可作局部麻醉劑,常因保存不慎而被空氣氧化,產(chǎn)生劇毒氣體——光氣,反應化學方程式為2CHCl3+O2![]() 2COCl2+2HCl,上述反應__________ (填選項符號,下同)。
2COCl2+2HCl,上述反應__________ (填選項符號,下同)。
A.屬于取代反應 B.不屬于取代反應
為防止事故發(fā)生,在使用前檢驗氯仿是否變質(zhì)可選用的試劑是____________。
A.氫氧化鈉溶液 B.硝酸銀溶液
C.稀鹽酸 D.水
E.濕潤的藍色石蕊試紙 F.濕潤的無色酚酞試紙
(4)D裝置的石棉中均勻混有KI粉末,其作用是___________。
(5)E裝置的作用是____________ (填編號)。
A.收集氣體 B.吸收氯氣
C.防止倒吸 D.吸收氯化氫
(6)E裝置除生成鹽酸外,還含有有機物,從E中分離出鹽酸的最佳方法為_____________;該裝置還有缺陷,原因是沒有進行尾氣處理,其尾氣主要成分為_____ (填編號)。
①CH4 ②CH3Cl ③CH2Cl2 ④CHCl3 ⑤CCl4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯化亞銅是一種重要的化工原料,一種利用低品位銅礦![]() 主要含有Cu2S、CuS、FeO、Fe2O3、SiO2等
主要含有Cu2S、CuS、FeO、Fe2O3、SiO2等![]() 為原料制取CuCl的工藝流程如下:
為原料制取CuCl的工藝流程如下:

(1)反應Ⅰ“浸取”前需將銅礦粉碎的目的是___________________________;
(2)濾渣Ⅰ的成分除S和![]() 外還含有___________,反應 Ⅰ中
外還含有___________,反應 Ⅰ中![]() 的作用為_______________
的作用為_______________
(3)已知生成氫氧化物的pH如下表,則反應Ⅱ“中和”時,用氨水調(diào)pH的范圍是______________。
物質(zhì) |
|
|
|
開始沉淀pH |
|
|
|
完全沉淀pH |
|
|
|
(4)檢驗濾液Ⅱ中是否含有![]() 所需要的試劑是:______________
所需要的試劑是:______________
(5)①反應Ⅲ中生成難溶![]() 的離子方程式:______________
的離子方程式:______________
②反應Ⅳ所對應的化學方程式:______________________________
(6) CuCl的定量分析
步驟1.取樣品0.7500g和30.0mL 1.0mol·L-1過量的FeCl3溶液置于250mL的錐形瓶中,不斷搖動。
步驟2.待樣品溶解后,平均分為3份,用0.1000mol·L-1 Ce(SO4)2標準溶液進行滴定。
三次實驗測得數(shù)據(jù)如下表
序號 | 1 | 2 | 3 |
起始讀數(shù) |
|
|
|
終點讀數(shù) |
|
|
|
已知:![]() ;
;![]() 。
。
①數(shù)據(jù)處理:計算得CuCl的純度為_________![]()
②誤差下列操作會使測定結果偏高的是______________
A.錐形瓶中有少量蒸餾水
B.滴定終點讀數(shù)時仰視滴定管刻度線
C.0.1000mol·L-1硫酸鈰溶液久置后濃度變小
D.滴定前滴定管尖嘴無氣泡,滴定后產(chǎn)生氣泡
E.用量筒取10.0mL 1.0mol·L-1的![]() 溶液時仰視刻度線
溶液時仰視刻度線
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學興趣小組的同學用如下圖所示裝置研究有關電化學的問題。當閉合K時,觀察到電流表的指針發(fā)生了偏移。
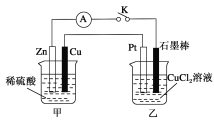
請回答下列問題:
(1)乙裝置的名稱是________;Zn為________極。
(2)寫出電極反應:Cu極:______________________;石墨棒極:______________________。
(3)當甲中產(chǎn)生0.1mol氣體時,乙中產(chǎn)生的氣體在標準狀況下的體積應為________________。
(4)若乙中溶液不變,將其電極都換成銅電極,閉合K一段時間后,乙中溶液的顏色________(填“變深”、“變淺”或“無變化”)。
(5)若乙中電極不變,將其溶液換成NaCl溶液,閉合K一段時間后,甲中溶液的pH將________(填“增大”、“減小”或“不變”,下同);乙中溶液的pH將________。
(6)若乙中電極不變,將其溶液換成飽和Na2SO4溶液,閉合K一段時間,當陰極上有a mol氣體生成時,同時有w g Na2SO4·10H2O析出,假設溫度不變,剩余溶液中溶質(zhì)的質(zhì)量分數(shù)應為________(用含w、a的表達式表示,不必化簡)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某興趣小組以廢鐵屑制得硫酸亞鐵銨后,按下列流程制備二水合草酸亞鐵(FeC2O4·2H2O),進一步制備高純度還原鐵粉。
已知:FeC2O4·2H2O難溶于水,150℃開始失結晶水;常溫下H2C2O4為晶體,易溶于水,溶解度隨溫度升高而增大。

請回答:
(1)步驟②,發(fā)生反應的離子方程式____________________________;該步驟H2C2O4稍過量主要是為了_________________。
(2)下列操作或描述正確的是_______________。
A.步驟①,酸化主要是為了抑制Fe2+水解
B.步驟③,如果采用冷水洗滌可提高除雜效果
C.步驟③,如果在常壓下快速干燥,溫度可選擇略高于100℃
(3)稱取一定量的FeC2O4·2H2O試樣,用硫酸溶解,采用KMnO4滴定法測定,折算結果如下:
n(Fe2+)/mol | n(C2O42-)·mol-1 | 試樣中FeC2O4·2H2O的質(zhì)量分數(shù) |
9.80×10-4 | 9.80×10-4 | 0.98 |
由表中數(shù)據(jù)推測試樣中最主要的雜質(zhì)是_________________。
(4)實現(xiàn)步驟④必須用到的兩種儀器是_________(供選儀器如下)
a.坩堝;b.燒杯;c.蒸餾燒瓶;d.錐形瓶;e.表面皿:f.高溫爐
該步驟的化學方程式是______________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】罌粟堿是一種異喹啉型生物堿,其鹽酸鹽可用于治療腦血栓、肢端動脈痙攣等。罌粟堿的合成方法如下:

(1)D分子中的官能團有___和___(填名稱)。
(2)B→C的轉(zhuǎn)化屬于___反應(填反應類型)。
(3)E和F發(fā)生取代反應生成G的同時有HCl生成,則F的結構簡式是___。
(4)E的同分異構體有多種,寫出兩種符合下列要求的異構體X的結構簡式:___。
Ⅰ.含氧官能團種類與D相同。
Ⅱ.核磁共振氫譜圖中有4個吸收峰。
Ⅲ.屬于芳香族化合物,苯環(huán)上一取代物有兩種。
(5) 已知: (R、R’為烴基)。根據(jù)已有知識并結合相關信息,寫出以乙醇為原料制備
(R、R’為烴基)。根據(jù)已有知識并結合相關信息,寫出以乙醇為原料制備![]() 的合成路線流程圖(無機試劑任用)___。
的合成路線流程圖(無機試劑任用)___。
合成路線流程圖示例如下:CH3CH2OH![]() H2C=CH2
H2C=CH2![]()
![]() 。
。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A.常溫下,向0.1 mol·L1 CH3COONa中加入少量水,溶液中![]() 比值減小
比值減小
B.用0.1 mol·L1 NaOH溶液分別中和等體積等pH的鹽酸和醋酸,鹽酸消耗NaOH溶液的體積大
C.常溫下,pH=10的氨水中,由水電離出的OH-濃度為1×10-4mol·L1
D.常溫下,向10 mL pH=2的鹽酸中分別加入V1 mL的水和V2 mL pH=12的NaOH溶液,所得溶液的pH均為3,忽略混合時溶液體積的變化,則V1∶V2=11∶1
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com