

分析 水溶后,VOSO4、硫酸鉀可溶于水,二氧化硅不溶于水,過濾得到濾渣為二氧化硅,濾液加入有機萃取劑,萃取得到含VO2+有機層,反萃取除掉有機萃取劑,加入KClO3使VO2+氧化為VO3-,焙燒得到V2O5.
(1)二氧化硅不溶于水,過濾得到濾渣為二氧化硅;二氧化硅與氫氧化鈉溶液反應生成了硅酸鈉和水,反應的離子方程式為:SiO2+2OH-=SiO32-+H2O;
(2)步驟②、③是萃取、分液,使用的主要儀器是分液漏斗;②中萃取時必須加入適量堿,會和平衡中的氫離子反應促進平衡正向進行;
(3)③中反萃取時加入的X試劑是抑制平衡正向進行;步驟④加入KClO3使VO2+氧化為VO3-,則本身被還原為Cl-;
(4)分析流程圖,物質參加反應,反應過程中又生成可以循環利用.
解答 解:水溶后,VOSO4、硫酸鉀可溶于水,二氧化硅不溶于水,過濾得到濾渣為二氧化硅,濾液加入有機萃取劑,萃取得到含VO2+有機層,反萃取除掉有機萃取劑,加入KClO3使VO2+氧化為VO3-,焙燒得到V2O5.
(1)水溶后,VOSO4、硫酸鉀可溶于水,二氧化硅不溶于水,過濾得到濾渣為二氧化硅,二氧化硅與氫氧化鈉溶液反應生成了硅酸鈉和水,反應的離子方程式為:SiO2+2OH-=SiO32-+H2O,
故答案為:SiO2+2OH-=SiO32-+H2O;
(2)①實驗室中步驟②、③是萃取、分液,使用的主要儀器是分液漏斗,故答案為:分液漏斗;
②分析平衡,Rn+(水層)+nHA(有機層)?RAn(有機層)+nH+(水層),加入的堿會中和氫離子促進平衡正向進行,提高了釩的萃取率;
故答案為:加入的堿會中和氫離子促進平衡正向進行,提高了釩的萃取率;
(3)③中反萃取時加入的X試劑是抑制平衡正向進行,可以加入硫酸抑制平衡正向進行;步驟④加入KClO3使VO2+氧化為VO3-,則本身被還原為Cl-,配平得離子方程式為ClO3-+6VO2++9H2O=Cl-+6VO3-+18H+,
故答案為:硫酸;ClO3-+6VO2++9H2O=Cl-+6VO3-+18H+;
(4)分析流程圖,物質參加反應,反應過程中又生成的物質,或重復利用的物質可以循環利用,流程中有機萃取劑、氨氣可以循環利用,
故答案為:有機萃取劑;氨氣.
點評 本題考查了流程分析判斷,物質性質和實驗設計的方法應用,題干信息分析判斷能力,掌握基礎是關鍵,題目難度中等.


科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
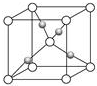 Al、Ti、Fe、Cu是幾種常見的重要金屬.根據要求回答下列問題:
Al、Ti、Fe、Cu是幾種常見的重要金屬.根據要求回答下列問題:| 元素 | A | B | |
| 電離能(kJ/mol) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加入水時,溶液中$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$增大 | |
| B. | 降低溫度,溶液中c(NH4+)增大 | |
| C. | 加入少量NaOH固體,平衡向左移動,電離平衡常數減小 | |
| D. | 加入少量0.1 mol•L-1 鹽酸,溶液中c(OH-)增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①④⑤ | B. | ①②③④ | C. | ①②③④⑤ | D. | 全部 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 反應時間/min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
| A. | 反應在t1min內的平均速率為v(H2)=$\frac{0.40}{t_1}$mol/(L•min) | |
| B. | 保持其他條件不變,起始時向容器中充入0.60molCO和1.20molH2O,到達平衡時n(CO2)=0.40 mol | |
| C. | 保持其他條件不變,向平衡體系中再通入0.20molH2O,與原平衡相比,達到新平衡時CO轉化率增大,H2O的體積分數減小 | |
| D. | 溫度升至1000℃,上述反應平衡常數為1.6,則正反應為放熱反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
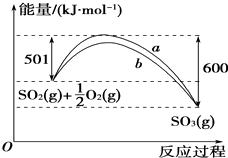 根據下列敘述寫出相應的熱化學方程式:
根據下列敘述寫出相應的熱化學方程式:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
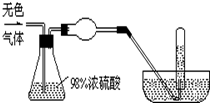 有一無色氣體(可能由O2、N2、CO2、HCl、NH3、H2、NO、NO2中的一種或幾種組成),體積為100mL.如圖示通過濃硫酸的洗氣瓶,發現氣體體積減少到一半;通過球形干燥管后氣體呈紅棕色,再將該氣體完全通入盛滿水且倒立于水槽的試管內,發現倒立于水槽的試管內的水位下降后又緩慢上升,最后試管內全部充滿液體,由此判斷:
有一無色氣體(可能由O2、N2、CO2、HCl、NH3、H2、NO、NO2中的一種或幾種組成),體積為100mL.如圖示通過濃硫酸的洗氣瓶,發現氣體體積減少到一半;通過球形干燥管后氣體呈紅棕色,再將該氣體完全通入盛滿水且倒立于水槽的試管內,發現倒立于水槽的試管內的水位下降后又緩慢上升,最后試管內全部充滿液體,由此判斷:查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com