
分析 2min末生成0.2mol W,v(W)=$\frac{\frac{0.2mol}{2L}}{2min}$=0.05mol/(L•min),若測得以Z的物質的量濃度變化表示的平均反應速率為0.1mol/(L•min),由速率之比等于化學計量數之比可知n=4,則
3X(g)+Y(g)=4Z(g)+2W(g)
開始 1 0.5 0 0
轉化 0.3 0.1 0.4 0.2
2min 0.7 0.4 0.4 0.2
結合v=$\frac{△c}{△t}$、轉化率=$\frac{轉化的量}{開始的量}$×100%計算.
解答 解:2min末生成0.2mol W,v(W)=$\frac{\frac{0.2mol}{2L}}{2min}$=0.05mol/(L•min),若測得以Z的物質的量濃度變化表示的平均反應速率為0.1mol/(L•min),由速率之比等于化學計量數之比可知n=4,則
3X(g)+Y(g)=4Z(g)+2W(g)
開始 1 0.5 0 0
轉化 0.3 0.1 0.4 0.2
2min 0.7 0.4 0.4 0.2
(1)2 min末生成0.2 mol W,轉化的X為0.3mol,v(X)=$\frac{\frac{0.3mol}{2L}}{2min}$=0.075 mol/(L•min),
答:前2min內,用X表示的平均反應速率為0.075 mol/(L•min);
(2)2min末時Y的轉化率α(Y)=$\frac{0.1mol}{0.5mol}$×100%=20%,
答:2min末時Y的轉化率為20%;
(3)由上述分析可知n=4,
答:化學方程式中Z的化學計量數n為4.
點評 本題考查化學平衡的計算,為高頻考點,把握化學平衡三段法、各物質的量的關系等為解答的關鍵,側重分析與計算能力的考查,注意速率與化學計量數的關系確定n,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 僅有實驗①可推出肯定含有SO42-,不含Cl- | |
| B. | 該無色溶液肯定含有NH4+、K+、Al3+、SO42- | |
| C. | 該無色溶液中肯定不含K+、Mg2+、HCO3-、Cl-、MnO4-、I- | |
| D. | 不能確定該無色溶液是否含有K+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 32g O2 | B. | 0.2mol N2 | ||
| C. | 3.01×1023個CO2分子 | D. | 標準狀況下11.2L H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
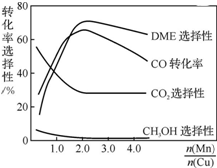 采用一種新型的催化劑(主要成分是Cu-Mn的合金),利用CO和H2制備二甲醚(DME).觀察上右圖回答問題:催化劑中$\frac{n(Mn)}{n(Cu)}$約為2.0時最有利于二甲醚的合成.
采用一種新型的催化劑(主要成分是Cu-Mn的合金),利用CO和H2制備二甲醚(DME).觀察上右圖回答問題:催化劑中$\frac{n(Mn)}{n(Cu)}$約為2.0時最有利于二甲醚的合成.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
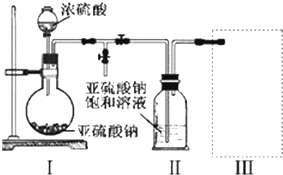
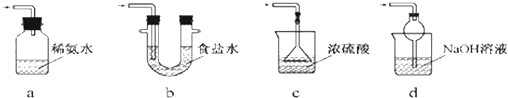

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| t/(℃) | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 漂白粉被氧化了 | |
| B. | 有色布條被空氣中的氧氣氧化了 | |
| C. | 漂白粉跟空氣中的 CO2反應充分,生成了較多量的 HClO | |
| D. | 漂白粉溶液蒸發掉部分水,其濃度增大 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com