
【題目】鑭系金屬元素鈰(Ce)常見有+3、+4兩種價態,鈰的合金耐高溫,可以用來制造噴氣推進器零件。鈰元素在自然界中主要以氟碳鈰礦形式存在,其主要化學成分為CeFCO3。工業上利用氟碳鈰礦提取CeCl3的一種工藝流程如下:

(1)為了提高焙燒效率可以采取的措施有______________。(回答兩條即可)
(2)假設參與酸浸反應的CeO2和CeF4的物質的量之比為3∶1,試寫出相應的化學方程式: ______。有同學認為酸浸過程中用稀硫酸和H2O2替換鹽酸更好,其理由是:___________。
(3)常溫下,當溶液中的某離子濃度≤1.0×10-5 mol·L-1時,可認為該離子沉淀完全。據此,在生成Ce(OH)3的反應中,加入NaOH溶液至pH至少達到________時,即可視為Ce3+已完全沉淀。{Ksp[Ce(OH)3]=1.0×10-20}。
(4)向Ce(BF4)3中加入KCl溶液,該反應能發生的原因是____________________。
(5)霧霾中含有的污染物NO可以被含Ce4+的溶液吸收,生成NO2-、NO3-,用電解的方法可將上述吸收液中的NO2-轉化為穩定的無毒氣體,同時將Ce3+再生為Ce4+,其原理如圖所示。

①NO2-從電解槽的________(填字母序號)口進入。
②每生成標準狀況下11.2 L無毒氣體,同時可再生Ce4+________ mol。
【答案】粉碎、逆流、增大空氣量 9CeO2+3CeF4+45HCl+3H3BO3=Ce(BF4)3↓+11CeCl3+6Cl2↑+27H2O 不釋放氯氣,減少對環境的污染 9 KBF4的溶解性比Ce(BF4)3 的溶解性更小 d 3
【解析】
利用氟碳鈰礦(主要成分CeFCO3)提取CeCl3的一種工藝流程為,CeFCO3焙燒得CeO2、CeF4,用鹽酸和硼酸酸浸,過濾得沉淀Ce(BF)4和CeCl3濾液,Ce(BF)4與氯化鉀溶液反應得到CeCl3和KBF4,CeCl3與前面濾液中CeCl3的合并再加氫氧化鈉,得Ce(OH)3沉淀,Ce(OH)3沉淀與鹽酸反應可得CeCl36H2O,加熱CeCl36H2O和NH4Cl的固體混合物可得到無水CeCl3;據此解答。
(1)根據外界條件對反應速率的影響可知為了提高焙燒效率可以采取的措施有粉碎、逆流、增大空氣量等。
(2)假設參與酸浸反應的CeO2和CeF4的物質的量之比為3∶1,根據流程可知反應物還有HCl、H3BO3,生成物有Ce(BF4)3沉淀、CeCl3,根據化合價的變化,因元素Ce由+4價變為+3價,化合價降低,由氧化還原反應原理可知,應有元素化合價升高,則應有Cl2生成,結合原子守恒可知相應的化學方程式為9CeO2+3CeF4+45HCl+3H3BO3=Ce(BF4)3↓+11CeCl3+6Cl2↑+27H2O。由于有氯氣生成,會污染空氣,所以酸浸過程中用稀硫酸和H2O2替換鹽酸更好的理由是不釋放氯氣,減少對環境的污染。
(3)常溫下,當溶液中的某離子濃度≤1.0×10-5 mol·L-1時,可認為該離子沉淀完全。根據Ksp[Ce(OH)3]=1.0×10-20可知溶液中氫氧根濃度是![]() =10-5mol/L,因此在生成Ce(OH)3的反應中,加入NaOH溶液至pH至少達到9時,即可視為Ce3+已完全沉淀。
=10-5mol/L,因此在生成Ce(OH)3的反應中,加入NaOH溶液至pH至少達到9時,即可視為Ce3+已完全沉淀。
(4)由于KBF4的溶解性比Ce(BF4)3的溶解性更小,因此向Ce(BF4)3中加入KCl溶液,該反應能發生。
(5)①根據氫離子的移動方向可知左側電極是陽極,右側電極是陰極,NO2-得到電子轉化為穩定的無毒氣體氮氣,所以NO2-從電解槽的d口進入。
②每生成標準狀況下11.2 L無毒氣體,氮氣的物質的量是0.5mol,轉移0.5mol×6=3.0mol電子,根據電子得失守恒可知同時可再生3.0molCe4+。


科目:高中化學 來源: 題型:
【題目】下圖是部分短周期元素原子半徑與原子序數的關系如圖,則下列說法正確的是( )
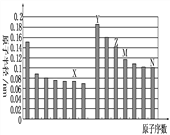
A . Z、N兩種元素形成的化合物熔融狀態下可以導電
B.X、N兩種元素的氣態氫化物的沸點相比,前者較低
C.Z的氧化物能分別溶解于Y的氫氧化物和N的氫化物的水溶液中
D.由X與M兩種元素組成的化合物能與水反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述不正確的是( )
A. CCl4可由CH4制得,可萃取碘水中的碘
B. 乙烯和甲苯分子中所有原子都在同一個平面上
C. 煤油可由石油分餾獲得,可用作燃料和保存少量金屬鈉
D. ![]() 和CH3-CH=CH2互為同分異構體
和CH3-CH=CH2互為同分異構體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】維拉帕米(又名異搏定)是治療心絞痛和原發性高血壓的藥物,合成路線中某一步驟如圖所示。
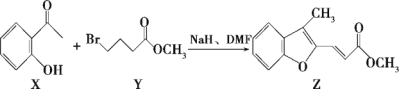
下列說法中正確的是
A.X中所有原子可能在同一平面上B.含苯環和羧基的X的同分異構體有3種
C.Z的分子式為C13H10O3D.1 mol Z最多可與2 mol Br2發生加成反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】前四周期元素A、B、C、D、E原子序數依次增大。已知:A、C同主族,A的原子最外層電子數是次外層的3倍,B的氧化物既能溶于強酸,又能溶于強堿,D的原子半徑是第3周期中最小的,E是形成骨骼和牙齒的主要元素,且E單質能和水反應。則下列分析錯誤的是
A.A和 B形成的化合物可作為耐火材料
B.A和C的氫化物的沸點:C>A
C.簡單離子半徑:E<D<C
D.E和D形成的化合物的電子式:![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某芳香烴A,分子式為C8H10;某烴類衍生物X,分子式為C15H14O3,能使FeCl3溶液顯紫色;J分子內有兩個互為對位的取代基.在一定條件下有如下的轉化關系:(無機物略去)
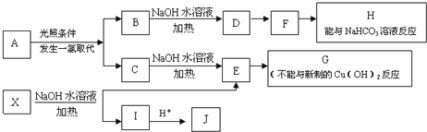
(1)屬于芳香烴類的A的同分異構體中,其沸點的大小關系為______;(不包括A,用結構簡式表示)
(2)J中所含的含氧官能團的名稱為______;
(3)E與H反應的化學方程式是________;反應類型是_______;
(4)B、C的混合物在NaOH乙醇溶液中加熱可以生成同一種有機物I,以I為單體合成的高分子化合物的名稱是______;
(5)已知J有多種同分異構體,寫出一種符合下列性質的J的同分異構體的結構簡式_______;
①與FeCl3溶液作用顯紫色
②與新制Cu(OH)2懸濁液作用產生紅色沉淀
③苯環上的一鹵代物有2種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知硫酸鈉晶體(![]() )的物質的量為1.5mol,請計算填空:
)的物質的量為1.5mol,請計算填空:
(1)所含鈉離子的物質的量是________,鈉離子的數目是________。
(2)所含硫酸根離子的物質的量是________,所含氧原子的數目是________。
(3)硫酸鈉晶體(![]() )是_______________________(填“純凈物”或“混合物”)
)是_______________________(填“純凈物”或“混合物”)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫酸是一種重要的化工產品,硫酸的消耗量常被視為一個國家工業發展水平的一種標志。目前的重要生產方法是“接觸法”,有關接觸氧化反應2SO2+O2![]() 2SO3的說法不正確的是
2SO3的說法不正確的是
A.該反應為可逆反應,故在一定條件下二氧化硫和氧氣不可能全部轉化為三氧化硫
B.達到平衡后,反應就停止了,故此時正、逆反應速率相等且均為零
C.一定條件下,向某密閉容器中加入2 mol SO2和1 mol O2,則從反應開始到達到平衡的過程中,正反應速率不斷減小,逆反應速率不斷增大,某一時刻,正、逆反應速率相等
D.在利用上述反應生產三氧化硫時,要同時考慮反應所能達到的限度和化學反應速率兩方面的問題
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學設計如下實驗方案,以分離KCl和BaCl2兩種固體混合物,試回答下列問題:
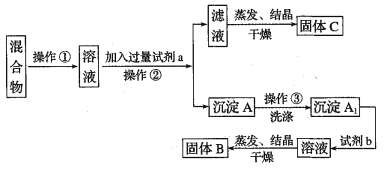
供選試劑:Na2SO4溶液、K2CO3溶液、K2SO4溶液、鹽酸
(1)操作②的名稱是______________,試劑a的溶質是_______________(填化學式)。
(2)加入試劑b所發生反應的化學方程式為_____________________________。
(3)該方案有不足之處,請你把它找出來并改進:_______________________________。
(4)操作③為什么要洗滌沉淀A:_____________________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com