
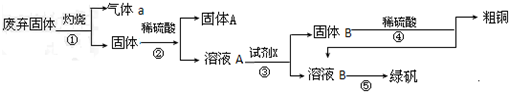
分析 廢棄固體主要成分Cu2S和Fe2O3、SiO2等,灼燒廢氣固體發生反應Cu2S+2O2$\frac{\underline{\;高溫\;}}{\;}$SO2+2CuO,所以氣體a是SO2,固體A是CuO和Fe2O3、SiO2,固體和稀硫酸混合,發生的反應為CuO+H2SO4=CuSO4+H2O、Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,所以溶液A中成分為CuSO4、Fe2(SO4)3,而二氧化硅與稀硫酸不反應,則固體A為SiO2,向溶液A中加入過量Fe屑,發生反應CuSO4+Fe=FeSO4+Cu、2Fe2(SO4)3+Fe=3FeSO4,所以固體B成分是Fe、Cu,濾液B成分為FeSO4,固體B和稀硫酸混合,Fe和稀硫酸反應生成FeSO4,Cu和稀硫酸不反應,過濾得到固體粗銅,以此解答該題.
解答 解:廢棄固體主要成分Cu2S和Fe2O3、SiO2等,灼燒廢氣固體發生反應Cu2S+2O2$\frac{\underline{\;高溫\;}}{\;}$SO2+2CuO,所以氣體a是SO2,固體A是CuO和Fe2O3、SiO2,固體和稀硫酸混合,發生的反應為CuO+H2SO4=CuSO4+H2O、Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,所以溶液A中成分為CuSO4、Fe2(SO4)3,而二氧化硅與稀硫酸不反應,則固體A為SiO2,向溶液A中加入過量Fe屑,發生反應CuSO4+Fe=FeSO4+Cu、2Fe2(SO4)3+Fe=3FeSO4,所以固體B成分是Fe、Cu,濾液B成分為FeSO4,固體B和稀硫酸混合,Fe和稀硫酸反應生成FeSO4,Cu和稀硫酸不反應,過濾得到固體粗銅,
(1)由以上分析可知,二氧化硅和稀硫酸不反應,固體A為SiO2,故答案為:SiO2;
(2)加入試劑X,用于置換出銅并生成硫酸亞鐵,則X應為Fe,發生的離子反應為2 Fe3++Fe=3Fe2+、Fe+Cu2+=Fe2++Cu,
故答案為:Fe;2 Fe3++Fe=3Fe2+、Fe+Cu2+=Fe2++Cu;
(3)溶液B獲得綠礬的實驗操作是蒸發濃縮、冷卻結晶、過濾、洗滌、干燥,故答案為:冷卻結晶;過濾.
點評 本題考查混合物的分離和提純和制備,側重考查學生分析問題、實驗操作、思維縝密性等能力,明確物質的性質是解本題關鍵,能從整體上分析各個步驟發生的反應,能正確書寫相應的化學方程式和離子方程式,題目難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 4種 | B. | 5種 | C. | 6種 | D. | 7種 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在水中通入氯氣:Cl2+H2O=Cl-+2H++ClO- | |
| B. | 二氧化硅與燒堿溶液反應:SiO2+2OH-=SiO32-+H2O | |
| C. | 往氯化鋁溶液中滴加過量的氨水:Al3++4NH3•H2O=[Al(OH)4]-+4NH4+ | |
| D. | 往氯化鐵溶液中加入銅:Fe3++Cu=Cu2++Fe2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
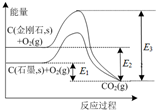
| A. | 石墨與O2生成CO2的反應是吸熱反應 | |
| B. | 等量金剛石和石墨完全燃燒,金剛石放出熱量更多 | |
| C. | 從能量角度看,金剛石比石墨更穩定 | |
| D. | 金剛石轉化為石墨需要吸收的能量為E3-E2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .該物質合成線路如圖示:
.該物質合成線路如圖示: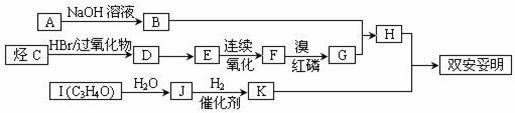
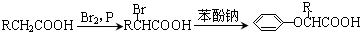
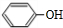 ,CC(CH3)2=CH2,ICH2=CH-CHO,JHOCH2CH2CHO.
,CC(CH3)2=CH2,ICH2=CH-CHO,JHOCH2CH2CHO.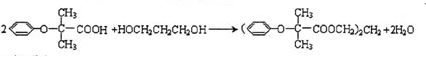 .
.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com