
分析 由方程式可知,反應中Mn元素化合價由+7價降低到+2價,被還原,KMnO4為氧化劑,Cl元素化合價由-1價升高到0價,被氧化,HCl為還原劑,結合化合價的變化以及反應的方程式可計算.
解答 解:(1)反應中Cl元素化合價由-1價升高到0價,HCl為還原劑,反應中生成MnCl2,則濃鹽酸體現出來的性質為還原性和酸性;
故答案為:還原性和酸性;
(2)反應中KMnO4為氧化劑,HCl為還原劑,16molHCl中只有10mol被氧化,則氧化劑與還原劑之比是2:10=1:5;
故答案為:1:5;
(3)Mn元素化合價由+7價降低到+2價,Cl元素化合價由-1價升高到0價,轉移10mol電子生成5mol氯氣,則轉移了0.6mol電子,則產生的氣體為0.3mol,在標準狀況下體積為6.72L;
故答案為:6.72L.
點評 本題考查氧化還原反應,側重于學生的分析能力和計算能力的考查,注意從元素化合價的角度認識氧化還原反應的相關概念和物質的性質,難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 少量的氯水加入到盛有NaBr溶液的試管中 | |
| B. | 取一小片鋁,砂紙除去氧化膜,放入試管中,加入少量2mL水 | |
| C. | 將鋅片與銅片用導線連接,插入盛稀硫酸的燒杯中 | |
| D. | 向盛有過氧化氫水溶液的試管中,加入少量1mol/LFeCl3溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
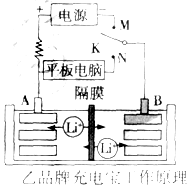 充電寶基本都由聚合物鋰電池作為儲電單元,它本身就是一個聚合物鋰電池的儲電裝置,通過IC芯片進行電壓的調控,再通過連接電源線充電或儲電后將貯存的電量釋放出來.
充電寶基本都由聚合物鋰電池作為儲電單元,它本身就是一個聚合物鋰電池的儲電裝置,通過IC芯片進行電壓的調控,再通過連接電源線充電或儲電后將貯存的電量釋放出來.查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 10 mL 0.1 mol/L AlCl3溶液 | B. | 20 mL 0.1 mol/L CaCl2溶液 | ||
| C. | 30 mL 0.2 mol/L KCl溶液 | D. | 200 mL 2 mol•L-1KClO3溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 3種 | B. | 4種 | C. | 5種 | D. | 6種 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 在容積為1.00L的容器中,通入一定量的N2O4,發生反應N2O4(g)?2NO2(g),隨溫度升高,混合氣體的顏色變深.
在容積為1.00L的容器中,通入一定量的N2O4,發生反應N2O4(g)?2NO2(g),隨溫度升高,混合氣體的顏色變深.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在一定溫度下AgCl水溶液中,Ag+和Cl-濃度的乘積是一個常數 | |
| B. | AgCl的Ksp=1.8×10-10 mol2•L-2,在任何含AgCl固體的溶液中,c(Ag+)=c(Cl-)且Ag+與Cl-濃度的乘積等于1.8×10-10 mol2•L-2 | |
| C. | 溫度一定時,當溶液中Ag+和Cl-濃度的乘積等于Ksp值時,此溶液為AgCl的飽和溶液 | |
| D. | 向2.0mL濃度均為0.1mol•L-1的KCl、KI混合溶液中滴加1~2滴0.01mol•L-1 AgNO3溶液,振蕩,沉淀呈黃色,說明AgCl的Ksp比AgI的Ksp小 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
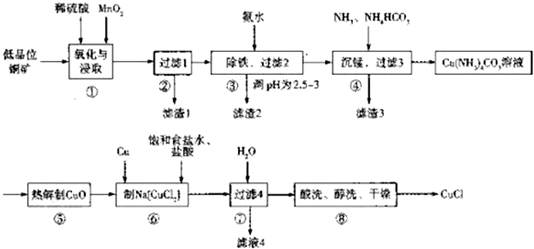
 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com