
| A. | 膠體的本質特征是膠粒直徑在1nm~100nm | |
| B. | 丁達爾現象可以用來區別膠體和溶液 | |
| C. | 煮沸飽和FeCl3溶液可以制得Fe(OH)3膠體 | |
| D. | 溶液和膠體的分散質都能通過濾紙孔隙 |
分析 A.膠體區別于其它分散系的本質是膠體分散質微粒直徑的大小;
B.膠體具有丁達爾現象,而溶液不具有;
C.把飽和FeCl3溶液滴入沸水中加熱到呈紅褐色液體可制得Fe(OH)3膠體;
D.溶液和膠體的分散質粒子直徑較小,均可以通過濾紙.
解答 解:A.膠體區別于其它分散系的本質是膠體分散質微粒直徑的大小,分散質粒子直徑在1nm~100nm之間的分散系屬于膠體,故A正確;
B.膠體具有丁達爾現象,而溶液不具有丁達爾效應,因此丁達爾現象可以用來區別膠體和溶液,故B正確;
C.把飽和FeCl3溶液滴入沸水中加熱到呈紅褐色液體可制得Fe(OH)3膠體,故C錯誤;
D.溶液和膠體的分散質粒子直徑較小,均可以通過濾紙孔隙,故D正確;
故選C.
點評 本題考查了膠體的性質,題目難度不大,注意掌握膠體和溶液的本質區別和鑒別的方法.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 如果容器內壓強不再改變,則證明該反應已達到平衡狀態 | |
| B. | 尋找合適的催化劑是加快反應速率并提高CO2產率的有效措施 | |
| C. | 當反應達到平衡后,保持容器內體積不變,再向其中充入CO和H2O(g)各1 mol,達到新的平衡后CO2的產率會增大 | |
| D. | 如果在某溫度下平衡常數為9.0,則平衡時CO轉化率為75% |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
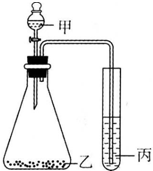
| A. | 甲-鹽酸,乙-石灰石,丙-硅酸鈉溶液,證明酸性:鹽酸>H2CO3>H2SiO3 | |
| B. | 甲-鹽酸,乙-亞硫酸鈉,丙-溴水,證明還原性:HCI>SO2>HBr | |
| C. | 甲-濃鹽酸,乙-高錳酸鉀,丙-溴化鉀,證明氧化性:KMnO4>Cl2>Br2 | |
| D. | 甲-氯化銨飽和溶液,乙-燒堿,丙-氯化鋁,證明堿性:NaOH>NH3•H2O>Al(OH)3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
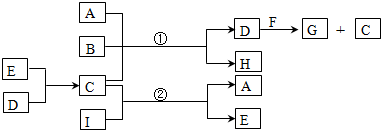
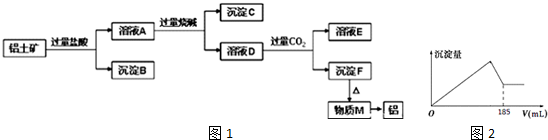
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
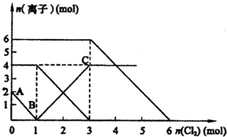 已知:2Fe2++Br2═2Fe3++2Br-、2Fe3++2I-═2Fe2++I2,向FeI2、FeBr2的混合溶液中通入適量氯氣,溶液中某些離子的物質的量變化如圖所示.則下列有關說法中,不正確的是( )
已知:2Fe2++Br2═2Fe3++2Br-、2Fe3++2I-═2Fe2++I2,向FeI2、FeBr2的混合溶液中通入適量氯氣,溶液中某些離子的物質的量變化如圖所示.則下列有關說法中,不正確的是( )| A. | 還原性:Fe2+>I->Br- | |
| B. | 原溶液中:n(Fe2+):n(I-):n(Br-)=2:2:3 | |
| C. | 原混合溶液中FeBr2的物質的量為6 mol | |
| D. | 當通入2molCl2時,溶液中已發生的離子反應可表示為2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | “鈷酞菁”分子既不能透過濾紙,又不能透過半透膜,混有氯化鈉的“鈷酞菁”可用滲析的方法凈化 | |
| B. | “鈷酞菁”與水所形成的分散系具有丁達爾效應 | |
| C. | 此項工作可以用來改變分子的某些物理性質 | |
| D. | 此項工作可廣泛應用于光電器件、生物技術等方面 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | (1)(2)(3) | B. | (1)(3)(4) | C. | (2)(4) | D. | (1)(4) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com