
| A. | 向水中投入一小塊金屬鈉 | B. | 將水加熱煮沸 | ||
| C. | 向水中通入二氧化碳氣體 | D. | 向水中加醋酸鈉晶體 |
分析 酸或堿抑制水電離,含有弱離子的鹽促進水電離,使水電離的離子在溶液中表現為c(OH-)<c(H+),說明該溶液呈酸性,溶液中的溶質為酸、強酸強堿酸式鹽或強酸弱堿鹽,據此分析解答.
解答 解:A.加入金屬鈉,和水電離出的H+反應生成NaOH和氫氣,c(H+)降低,使水的電離向右移動,堿性增強,則c(H+)<c(OH-),故A錯誤;
B.將水加熱煮沸,促進水電離,但溶液中仍然存在c(H+)=c(OH-),溶液呈中性,故B錯誤;
C.向水中通入CO2 后,CO2與水結合產生碳酸,碳酸電離產生H+,使得c(H+)>c(OH-),抑制水電離,故C正確;
D.向水中加入醋酸鈉晶體,CH3COO-與水電離出的H+反應生成CH3COOH,導致水的電離平衡向右移動,堿性增強,c(H+)<c(OH-),故D錯誤;
故選C.
點評 本題考查探究溶液酸堿性判斷及水的電離,為高頻考點,明確水電離影響因素是解本題關鍵,溶液酸堿性要根據溶液中c(H+)、c(OH-)相對大小判斷,題目難度不大.


科目:高中化學 來源: 題型:解答題
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cl2具有很強的氧化性,在化學反應中只能作氧化劑 | |
| B. | Cl-、Cl為不同的核素,有不同的化學性質 | |
| C. | 實驗室制備Cl2,可用排飽和食鹽水集氣法收集 | |
| D. | 電解飽和食鹽水制氯氣時,與電源負極相連的石墨棒上方充滿黃綠色氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 127I與131I互為同素異形體 | B. | 137Cs的核電荷數為137 | ||
| C. | 鈾235的中子數是143 | D. | 銫與水的反應比鈉與水的反應緩慢 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
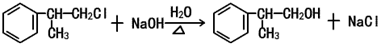
 (X為鹵素原子)
(X為鹵素原子)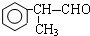 的物質,該物質是一種香料.
的物質,該物質是一種香料.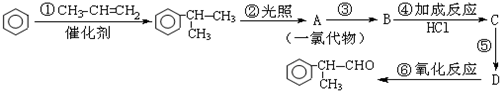
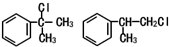 .
.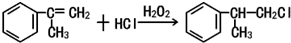 .
. .
.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
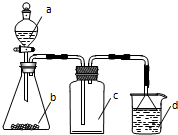 實驗室中某些氣體的制取、收集及尾氣處理裝置如圖所示(省略夾持和凈化裝置).用此裝置和表中提供的物質能完成相關實驗的是( )
實驗室中某些氣體的制取、收集及尾氣處理裝置如圖所示(省略夾持和凈化裝置).用此裝置和表中提供的物質能完成相關實驗的是( )| 選項 | a中物質 | b中物質 | c中的氣體 | d中物質 |
| A | 濃氨水 | CaO | NH3 | H2O |
| B | 稀硝酸 | Cu | NO | H2O |
| C | 硫酸 | Na2CO3 | CO2 | NaOH溶液 |
| D | 濃鹽酸 | MnO2 | Cl2 | NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 離子組 | 分析 |
| A | 含大量Al3+的溶液中:K+、Na+、NO3-、CO32- | 不能大量共存,因有Al2(CO3)3沉淀生成 |
| B | 含大量Fe3+的溶液中:K+、Mg2+、I-、NO3- | 不能大量共存,因2Fe3++2I-=2Fe2++I2 |
| C | 由水電離的c(H+)=1×10-14mol/L的溶液中: Ca2+、NO3-、HCO3-、Cl- | 不能大量共存,因溶液呈酸性,與HCO3-反應產生CO2氣體 |
| D | 使酚酞變紅的溶液中: Na+、K+、SO32-、S2- | 不能大量共存,因SO32-和S2-反應產生淡黃色的S沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| X | ||||
| Z | W |
| A. | X和氫組成的化合物分子中可能含有極性共價鍵和非極性共價鍵 | |
| B. | 工業上用電解Y和W組成的化合物來制備Y | |
| C. | Z、W兩元素的氣態氫化物中,W的氣態氫化物更穩定 | |
| D. | X、Y、Z、W元素最高價氧化物對應的水化物中酸性最強的是HWO4 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com