
| A. | 相同條件下,2 mol SO2(g)和1 mol O2(g)的鍵能之和大于2 mol SO3(g)的鍵能 | |
| B. | 如將一定量的SO2(g)和O2(g)置于某密閉容器中充分反應后放熱Q kJ,則此過程中有2 mol SO2(g)被氧化 | |
| C. | 增大壓強或升高溫度,該平衡都向逆反應方向移動 | |
| D. | 將2 mol SO2(g)和1 mol O2(g)置于一密閉容器中充分反應后,放出熱量為Q kJ |
分析 A.正反應為放熱反應,說明斷裂化學鍵吸收的能量小于生成化學鍵放出的能量;
B.根據熱化學方程式計算;
C.增大壓強,平衡正向移動;
D.反應為可逆反應,不能完全轉化.
解答 解:A.正反應為放熱反應,說明斷裂化學鍵吸收的能量小于生成化學鍵放出的能量,則2 mol SO2(g)和1 mol O2(g)的鍵能之和小于2 mol SO3(g)的鍵能,故A錯誤;
B.由熱化學方程式可知,如將一定量的SO2(g)和O2(g)置于某密閉容器中充分反應后放熱Q kJ,說明此過程中有2 mol SO2(g)被氧化,故B正確;
C.反應物氣體的計量數大于生成物氣體的計量數,增大壓強,平衡正向移動,故C錯誤;
D.反應為可逆反應,不能完全轉化,放出的熱量少于Q kJ,故D錯誤.
故選B.
點評 本題考查了熱化學方程式的應用、化學平衡的影響因素等,關鍵是可逆反應的焓變的意義理解,題目難度不大,側重于考查學生的分析能力和對基礎知識的應用能力.


科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2NO2 (g)?N2O4(g)△H<0 | B. | C(s)+CO2 (g)?2CO(g)△H>0 | ||
| C. | N2(g)+3H2 (g)?2NH3(g)△H<0 | D. | H2S (g)?H2 (g)+S(s)△H>0 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
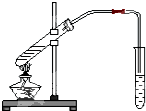 如圖為實驗室制乙酸乙酯的裝置.
如圖為實驗室制乙酸乙酯的裝置.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
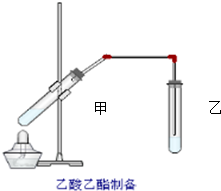 如圖在試管甲中先加入2mL 95%的乙醇,并在搖動下緩緩加入2mL濃硫酸,充分搖勻,冷卻后再加入2克無水乙酸鈉,用玻璃棒充分攪拌后將試管固定在鐵架臺上,在試管乙中加入5ml 飽和的碳酸鈉溶液,按圖連接好裝置,用酒精燈對試管甲小火加熱3~5min后,改用大火加熱,當觀察到左試管中有明顯現象時停止實驗.試回答:
如圖在試管甲中先加入2mL 95%的乙醇,并在搖動下緩緩加入2mL濃硫酸,充分搖勻,冷卻后再加入2克無水乙酸鈉,用玻璃棒充分攪拌后將試管固定在鐵架臺上,在試管乙中加入5ml 飽和的碳酸鈉溶液,按圖連接好裝置,用酒精燈對試管甲小火加熱3~5min后,改用大火加熱,當觀察到左試管中有明顯現象時停止實驗.試回答:查看答案和解析>>
科目:高中化學 來源: 題型:多選題
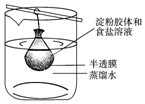 將10mL淀粉膠體和5mL氯化鈉溶液混合后,放入用半透膜制成的袋內,將此袋浸入蒸餾水中(如圖所示)2min后,分別取袋內和燒杯內液體進行實驗.下列說法正確的是( )
將10mL淀粉膠體和5mL氯化鈉溶液混合后,放入用半透膜制成的袋內,將此袋浸入蒸餾水中(如圖所示)2min后,分別取袋內和燒杯內液體進行實驗.下列說法正確的是( )| A. | 燒杯內液體加入硝酸銀溶液后有白色沉淀產生 | |
| B. | 燒杯內液體加入碘水后呈藍色 | |
| C. | 袋內液體加入硝酸銀溶液后不會出現白色沉淀 | |
| D. | 袋內液體加入碘水后不變藍 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 容量瓶用蒸餾水洗凈后,可不經干燥直接用于配制溶液 | |
| B. | 配制一定物質的量濃度的稀鹽酸時,用量筒量取9.82 mL濃鹽酸 | |
| C. | 配制1 L 0.1 mol•L-1的NaCl溶液時用托盤天平稱量5.85 g NaCl固體 | |
| D. | 定容時,為防止液滴飛濺,膠頭滴管緊貼容量瓶內壁 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com