
| A. | 向NH4HCO3溶液中加過量的NaOH溶液并加熱:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| B. | 向NaAlO2溶液中通入少量的CO2的反應為:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- | |
| C. | FeBr2與足量的Cl2反應為:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | |
| D. | 用濃鹽酸酸化的KMnO4溶液與H2O2反應,證明H2O2具有還原性:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O |
分析 A.氫氧化鈉過量,銨根離子、碳酸氫根離子都反應;
B.二氧化碳少量,反應生成氫氧化鋁沉淀和碳酸鈉;
C.氯氣足量二價鐵離子、溴離子全部被氧化;
D.高錳酸鉀能夠氧化氯化氫.
解答 解:A.向NH4HCO3溶液中加過量的NaOH溶液并加熱,離子方程式:HCO3-+NH4++2OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+2H2O+CO32-,故A錯誤;
B.向NaAlO2溶液中通入少量的CO2反應生成氫氧化鋁沉淀和碳酸鈉,反應離子方程式為:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-,故B正確;
C.FeBr2與足量的Cl2反應,離子方程式:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-,故C錯誤;
D.濃鹽酸具有還原性,能夠還原酸性的高錳酸鉀,所以鹽酸酸化會對過氧化氫還原性檢驗造成干擾,故D錯誤;
故選:B.
點評 本題考查離子反應方程式書寫的正誤判斷,為高頻考點,把握發(fā)生的化學反應及離子反應的書寫方法為解答的關(guān)鍵,注意離子反應遵循客觀事實、遵循原子個數(shù)、電荷守恒規(guī)律,題目難度不大.


 津橋教育計算小狀元系列答案
津橋教育計算小狀元系列答案科目:高中化學 來源: 題型:選擇題
| A. | HCl和NaOH反應的中和熱△H=-57.3 kJ•mol-1,則H2SO4和Ca(OH)2反應的中和熱△H=2×(-57.3)kJ•mol-1 | |
| B. | CO(g)的燃燒熱是283.0kJ/mol,則2CO2(g)═2CO(g)+O2(g)反應的△H=+586.0kJ•mol-1 | |
| C. | 需要加熱才能發(fā)生的反應一定是吸熱反應 | |
| D. | 1mol甲烷燃燒生成氣態(tài)水和二氧化碳所放出的熱量是甲烷燃燒熱 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 反應過程中MnO2作催化劑 | B. | 鹽酸未完全反應 | ||
| C. | 參加反應的鹽酸有一半被氧化 | D. | 反應產(chǎn)生2.24L氯氣(標況) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | .常溫常壓下,18 g H2O中含有的電子總數(shù)為10NA | |
| B. | .1 mol•L-1 NaCl溶液含有NA個Na+ | |
| C. | 常溫常壓下,92 g的NO2和N2O4混合氣體含有的原子數(shù)為3 NA | |
| D. | 標準狀況下,2.24LCH4所含中子數(shù)為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 都是有機化合物 | B. | 都能發(fā)生酯化反應 | ||
| C. | 都是純凈物 | D. | 水溶液均呈酸性 |
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省高二上第一次月考化學試卷(解析版) 題型:填空題
將1 mol I2(g) 和2 mol H2置于2L密閉容器中,在一定溫度下發(fā)生反應:I2(g) + H2(g)  2HI(g) △H<0,并達平衡。HI的體積分數(shù)w(HI)隨時間變化如圖曲線(Ⅱ)所示:
2HI(g) △H<0,并達平衡。HI的體積分數(shù)w(HI)隨時間變化如圖曲線(Ⅱ)所示:
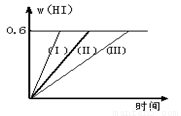
(1)達平衡時,I2(g)的物質(zhì)的量濃度為mol/L 。
(2)若改變反應條件,在甲條件下w(HI)的變化如曲線(Ⅰ) 所示,在乙條件下w(HI)的變化如曲線(Ⅲ) 所示。則甲條件可能是 ,則乙條件可能是 。(填入下列條件的序號)
①恒容條件下,升高溫度;②恒容條件下,降低溫度;③恒溫條件下,縮小反應容器體積;④恒溫條件下,擴大反應容器體積;⑤恒溫恒容條件下,加入正催化劑。
(3)若保持溫度不變,在另一個相同的2L密閉容器中加入2mol I2(g)、4mol H2(g)發(fā)生反應,達平衡時,HI的體積分數(shù)是 0.6(填大于、等于、小于)。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省高二上第一次月考化學試卷(解析版) 題型:選擇題
在25℃時,密閉容器中X、Y、Z三種氣體的初始濃度和平衡濃度如下表:
物質(zhì) | X | Y | Z |
初始濃度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡濃度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列說法錯誤的是( )
A.反應達到平衡時,X的轉(zhuǎn)化率為50%
B.反應可表示為X+3Y 2Z,其平衡常數(shù)為1600
2Z,其平衡常數(shù)為1600
C.改變溫度可以改變此反應的平衡常數(shù)
D.增大壓強使平衡向生成Z的方向移動,平衡常數(shù)增大
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省唐山市高二上10月月考化學試卷 (解析版) 題型:選擇題
如圖所示,a、b、c均為石墨電極,d為鐵電極,通電進行電解。假設在電解過程中產(chǎn)生的氣體全部逸出,下列說法正確的是( )
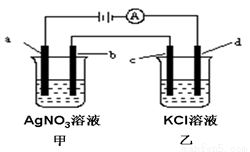
A.乙燒杯中的d電極反應式為Fe-2e-=Fe2+
B.電解一段時間后,將甲、乙兩溶液混合,一定會產(chǎn)生沉淀
C.當b極增重5.4g時,d極產(chǎn)生的氣體為2.24L(標況)
D.甲燒杯中溶液的pH降低
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com