
分析 金屬的電化學腐蝕分為吸氧腐蝕和析氫腐蝕兩種,中性或弱酸性條件下,鋼鐵發生吸氧腐蝕,負極上鐵失電子發生氧化反應,正極上氧氣得電子發生還原反應;酸性環境下,鋼鐵發生析氫腐蝕,負極上鐵失電子發生氧化反應,正極上氫離子得電子發生還原反應.
解答 解:金屬的電化學腐蝕分為吸氧腐蝕和析氫腐蝕兩種,正極上都是氧氣得電子發生還原反應,負極上是金屬失電子發生氧化反應,鋼鐵發生吸氧腐蝕時,鐵作負極,發生失電子的氧化反應,即Fe=Fe2++2e-.
故答案為:吸氧腐蝕;析氫腐蝕;還原;Fe=Fe2++2e-.
點評 本題考查了金屬的電化學腐蝕及電解池原理,明確鋼鐵所處環境的酸堿性即可確定其電化學腐蝕類型,題目難度不大,注意把握電極方程式的書寫方法.


 發散思維新課堂系列答案
發散思維新課堂系列答案科目:高中化學 來源: 題型:解答題
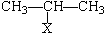 Ⅰ
Ⅰ CH=CH2)與丙烯的共聚物是一種高分子阻燃劑,具有低毒、熱穩定性好等優點.
CH=CH2)與丙烯的共聚物是一種高分子阻燃劑,具有低毒、熱穩定性好等優點. 或
或
 CHBrCH3.
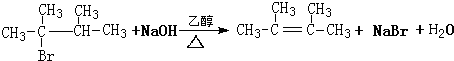
CHBrCH3. CHBrCH3與足量氫氧化鈉溶液共熱得到A,得到A時,苯環上沒有化學鍵的斷裂和生成.
CHBrCH3與足量氫氧化鈉溶液共熱得到A,得到A時,苯環上沒有化學鍵的斷裂和生成.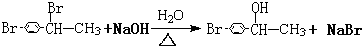 .
.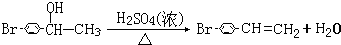 .
.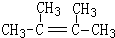 ,1molB完全燃燒時耗氧9mol
,1molB完全燃燒時耗氧9mol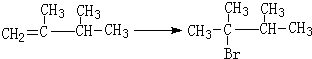
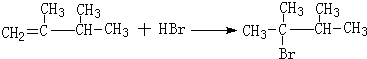
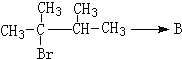
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NH3是氧化劑 | B. | NH3被氧化 | ||
| C. | NO只是還原劑 | D. | 生成60gNO轉移的5mol電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
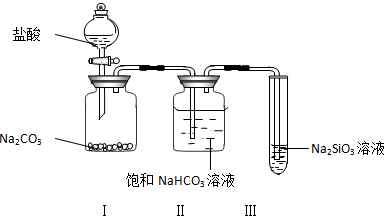
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
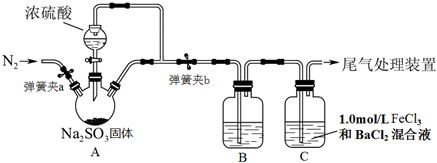
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 常溫下0.1 mol•L-1的下列溶液中:①NH4Al(SO4)2、②NH4Cl、③CH3COONH4,c(NH4+) 由大到小的順序為②>①>③ | |
| B. | 常溫下0.4 mol•L-1CH3COOH溶液和0.2 mol•L-1 NaOH溶液等體積混合后溶液顯酸性,則溶液中粒子濃度由大到小的順序為c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) | |
| C. | 0.1 mol•L-1 Na2CO3溶液與0.2 mol•L-1 NaHCO3溶液等體積混合所得溶液中:c(CO32-)+2c(OH-)=c(HCO3-)+3c(H2CO3)+2c(H+) | |
| D. | 0.1 mol•L-1的氨水與0.05 mol•L-1 H2C2O4溶液等體積混合所得溶液中:c(NH4+)+c(NH3•H2O)=2c(C2O42-)+2c(HC2O4-)+2c(H2C2O4) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③ | B. | ②④ | C. | ②⑤ | D. | ⑤⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氯水中通入一定量的SO2氣體可增強氯水的漂白性 | |
| B. | 因為SO2具有漂白性,所以它能使品紅溶液、酸性高錳酸鉀溶液褪色 | |
| C. | 已知酸性:H2SO4>HClO,則SO2通入漂白粉溶液中可生成次氯酸 | |
| D. | 紫色石蕊試液中通入SO2,溶液變紅后不褪色 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向水中加入NaHCO3溶液會抑制水的電離 | |
| B. | 35℃時純水中c(H+)>c(OH-) | |
| C. | 向水中加入NaHSO4溶液會抑制水的電離 | |
| D. | c(H+)隨著溫度的升高而降低 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com