
五種短周期元素的部分性質數據如下:
元素 | T | X | Y | Z | W |
原子半徑(nm) | 0.037 | 0.075 | 0.099 | 0.102 | 0.143 |
最高或最低化合價 | +1 | +5-3 | +7-1 | +6-2 | +3 |
(1)Z離子的結構示意圖為 。
(2)關于Y、Z兩種元素,下列敘述正確的是 (填序號)。
a.簡單離子的半徑 Y > Z
b.氣態氫化物的穩定性Y比 Z強
c.最高價氧化物對應水化物的酸性Z比Y強
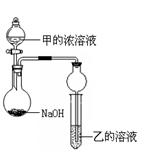
(3)甲是由T、X兩種元素形成的10 e-分子,乙是由Y、W兩種元素形成的化合物。某同學設計了下圖所示裝置(夾持儀器省略)進行實驗,將甲的濃溶液逐滴加入到NaOH固體中,燒瓶中即有甲放出,原因是 。一段時間后,觀察到試管中的現象是 ,發生反應的離子方程式是 。
(4)T、X兩種元素形成XT5固體,它的所有院子的最外層都符合相應稀有氣體原子的最外層結構,則其電子式為_____。
(5)XO2是導致光化學煙霧的“罪魁禍首”之一。它被氫氧化鈉溶液吸收的化學方程式是:2XO2 + 2NaOH = M + NaXO3 + H2O(已配平),產物M中元素X的化合價為 。
(6)常溫下,Z2Y2是一種橙黃色液體,廣泛用于橡膠工業的硫化機,其分子結構與雙氧水分子相似。試寫出其結構式_____。
科目:高中化學 來源:2015-2016學年山東省高二下期中化學試卷(解析版) 題型:推斷題
根據圖示回答下列問題:
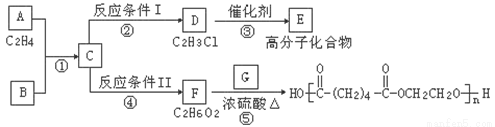
(1)寫出A、E、G的結構簡式:A_______、E_______、G_______。
(2)反應②的化學方程式是_______;反應④的化學方程式是_______。
(3)寫出①、⑤的反應類型:①_______、⑤_______。
(4)反應⑤的化學方程式是_______。
查看答案和解析>>
科目:高中化學 來源:2016屆湖南省等四校高三聯考化學試卷(解析版) 題型:選擇題
下列說法正確的是
A.可使用溴水鑒別植物油和汽油
B.利用二氧化碳制造全降解塑料,可以消除溫室效應
C.“玉兔號”月球車上的太陽能電池的材料是硅
D.實驗室金屬鈉失火時,可使用泡沫滅火器滅火
查看答案和解析>>
科目:高中化學 來源:2015-2016學年天津市高一下期中化學試卷(解析版) 題型:選擇題
為提純下列物質(括號內為雜質)。所選試劑及方法均正確的是
選項 | 物質(括號內為雜質) | 除雜試劑 | 方法 |
A | 溴苯(溴) | CCl4 | 分液 |
B | 硝基苯(NO2) | NaOH | 分液 |
C | 乙烷(乙烯) | 氫氣 | 洗氣 |
D | 乙醇(乙酸) | NaOH | 分液 |
查看答案和解析>>
科目:高中化學 來源:2015-2016學年天津市高一下期中化學試卷(解析版) 題型:選擇題
已知X、Y、Z為三種原子序數相連的元素,最高價氧化物對應水化物的酸性相對強弱是:HXO4>H2YO4>H3ZO4。則下列說法正確的是
A.氣態氫化物的穩定性:HX<H2Y<ZH3
B.非金屬活潑性:Y<X<Z
C.離子半徑:X-<Y2-<Z3-
D.原子序數:Z>Y>X
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山西省高一下期中化學試卷(解析版) 題型:選擇題
短周期元素A、B、C、D、E的原子序數依次增大,A的一中同位素的質量數為1,A和B同主族,C原子的最外層電子數是電子層數的3倍,D的最高正價與最低負價的絕對值相等,E的最高價氧化物的水化物的化學式為HnEO2n+2.下列說法正確的是( )
A.A與D可形成含18e-的離子化合物
B.B單質在C單質中燃燒生成原子個數比為1:1的化合物
C.D的氧化物為酸性氧化物,溶于水可制得D的含氧酸
D.D與E組成的化合物中,各原子最外層均達到8電子結構
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山西省高一下期中化學試卷(解析版) 題型:選擇題
某元素R的最高價氧化物的水化物分子式是HnRO(2n-2),則在氣態氫化物中R元素的化合價是
A.3n-10 B.12-3n C.3n-4 D.3n-12
查看答案和解析>>
科目:高中化學 來源:2015-2016學年寧夏育才中學高一下期中化學試卷(解析版) 題型:實驗題
某探究性學習小組擬通過鋅與鹽酸的反應研究影響反應速率的因素。
該探究性學習小組用相同質量的鋅和相同濃度的足量的稀鹽酸反應得到實驗數據如下表所示:
實驗編號 | 鋅的狀態 | 反應溫度/℃ | 收集100mL氫氣所需時間/s |
Ⅰ | 薄片 | 15 | 200 |
Ⅱ | 薄片 | 25 | 90 |
Ⅲ | 粉末 | 25 | 10 |
(1)該實驗的目的是探究 、 對鋅和稀鹽酸反應速率的影響;
(2)實驗Ⅰ和Ⅱ表明 ,化學反應速率越大;
(3)能表明固體的表面積對反應速率有影響的實驗編號是 和 ,實驗結論是 ;
(4)請設計一個實驗方案證明鹽酸的濃度對該反應的速率的影響:
。
查看答案和解析>>
科目:高中化學 來源:2016屆陜西省高三第六次適應性考試理綜化學試卷(解析版) 題型:填空題
硫酸工業在國民經濟中占有極其重要的地位。
(1)工業制硫酸時所用硫鐵礦的主要成分為FeS2,其中硫元素的化合物為 。
(2)硫酸的最大消費渠道是化肥工業,用硫酸制造的常見化肥有 (任寫一種)。
(3)硫酸生產中,根據化學平衡原理來確定的條件或措施有 (填寫序號)。
A.礦石加入沸騰爐之前先粉碎 B.使用V2O5作催化劑
C.轉化器中使用適宜的溫度 D.凈化后的爐氣中要有過量的空氣
E.催化氧化在常壓下進行 F.吸收塔中用98.3%的濃硫酸吸收SO3
(4)在硫酸工業中,通過下列反應使二氧化硫轉化為三氧化硫:
2SO2(g)+O2(g) 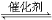 2SO3(g) ΔH=-98.3 kJ·mol-1
2SO3(g) ΔH=-98.3 kJ·mol-1
在實際工業生產中,常采用“二轉二吸法”,即將第一次轉化生成的SO2分離后,將未轉化的SO2進行二次轉化,假若兩次SO2的轉化率均為95%,則最終SO2的轉化率為 。
(5)硫酸的工業制法過程涉及三個主要的化學反應及相應的設備(沸騰爐、轉化器、吸收塔))。
①三個設備分別使反應物之間或冷熱氣體間進行了“對流”。請簡單描述吸收塔中反應物之間是怎樣對流的。____________________________________________________________________。
②工業生產中常用氨—酸法進行尾氣脫硫,以達到消除污染、廢物利用的目的。用化學方程式表示其反應原理。(只寫出2個方程式即可)
______________________________________________________________________
_____________________________________________________________________。
(6)實驗室可利用硫酸廠爐渣(主要成分為鐵的氧化物及少量FeS、SiO2等)制備聚鐵和綠礬(FeSO4•7H2O),聚鐵的化學式為[Fe2(OH)n(SO4)3﹣0.5n]m,制備過程如圖所示,下列說法正確的是 。

A.爐渣中FeS與硫酸和氧氣的反應的離子方程式為:4FeS+3O2+12H+═4Fe3++4S↓+6H2O
B.氣體M的成分是SO2,通入雙氧水得到硫酸,可循環使用
C.向溶液X中加入過量鐵粉,充分反應后過濾得到溶液Y,再將溶液Y蒸發結晶即可得到綠礬
D.溶液Z的pH影響聚鐵中鐵的質量分數,若其pH偏小,將導致聚鐵中鐵的質量分數偏大
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com