
 期末好成績系列答案
期末好成績系列答案 99加1領先期末特訓卷系列答案
99加1領先期末特訓卷系列答案 百強名校期末沖刺100分系列答案
百強名校期末沖刺100分系列答案 好成績1加1期末沖刺100分系列答案
好成績1加1期末沖刺100分系列答案 金狀元績優好卷系列答案
金狀元績優好卷系列答案科目:高中化學 來源: 題型:解答題
 名稱是3,5-二甲基庚烷.
名稱是3,5-二甲基庚烷. 名稱是1,2-二甲苯.
名稱是1,2-二甲苯. 名稱是5,5-二甲基-2-己炔.
名稱是5,5-二甲基-2-己炔. 名稱是4-甲基-1-戊烯.
名稱是4-甲基-1-戊烯.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
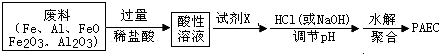
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
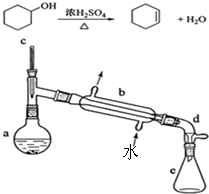 實驗室合成環己烯的反應和實驗裝置(夾持及加熱部分已省略)如圖:
實驗室合成環己烯的反應和實驗裝置(夾持及加熱部分已省略)如圖:| 相對分子數量 | 密度 | 沸點 | 溶解性 | |
| 環乙醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 環乙烯 | 82 | 0.8102 | 83 | 難溶于水 |
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
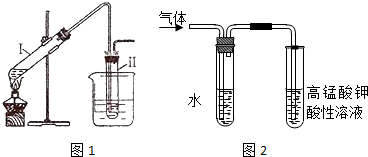
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com