
科目: 來源:河南省周口市西華縣2018屆九年級第一次模擬考試化學試卷 題型:實驗題
設計對比實驗是化學研究常用的方法,下圖是化學小組設計的鐵釘銹蝕條件的探究實驗。
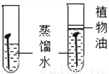
(1)簡要敘述要達到實驗目的還需補充什么實驗?_____________________
(2)寫出用鹽酸除鐵銹(Fe2O3)的化學方程式。_____________________
補充鐵釘在干燥空氣中不(或“是否”)生銹的實驗 Fe2O3 + 6HCl ===2 FeCl 3+ 3H2O 【解析】(1)該實驗中只有鐵只與水接觸、鐵與水和氧氣同時接觸的實驗,因此需要補充鐵釘在干燥的空氣中不生銹的實驗;(2)鹽酸與氧化鐵反應生成氯化鐵和水,化學方程式:Fe2O3 + 6HCl =2FeCl 3+ 3H2O。請用化學方程式表示下列有關反應的原理:
(1) 生活中用天然氣作燃料:_____________________
(2)工業上用純堿和熟石灰反應制燒堿:_____________________
查看答案除去NaCl溶液中CaCl2、MgCl2、Na2SO4雜質的操作有:①溶解;②依次加過量的BaCl2、NaOH、Na2CO3溶液;③過濾;④加適量的鹽酸;⑤蒸發結晶。
(1)過濾后濾液中的溶質有_________種,過濾中玻璃棒的作用是____________。
(2)寫出一個加鹽酸后反應的化學方程式_________________________________。
查看答案已知A、B、C、D是四種不同種類的物質,它們有如圖的轉化關系(部分物質和反應條件略去)。A是年產量最高的金屬,B中氧元素占30%,D的水溶液呈藍色,常用于配制農藥波爾多液。則則A是__________;B→A的化學方程式為_________________;C→D的化學方程式為____________________________________。
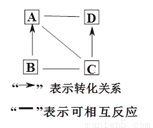
根據下圖甲、乙兩種物質的溶解度曲線回答相關問題:
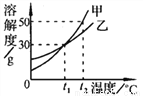
(1)在______℃時,甲、乙的溶解度相同。
(2)t2℃時,若將75 g甲的飽和溶液稀釋成10 %,需加水的質量為________g。
(3)將t2℃時,甲、乙兩種物質的飽和溶液降溫至t1℃(其他條件不變),所得溶液的溶質質量分數的關系是甲_________(填“>”、“<”或“=”)乙。
查看答案下圖是某反應的微觀示意圖,該反應中相對分子質量最小的物質是_________,反應的化學方程式為___________,參加反應的甲和乙的質量最簡整數比為___________。
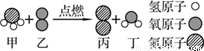
 Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
查看答案和解析>>
科目: 來源:河南省周口市西華縣2018屆九年級第一次模擬考試化學試卷 題型:簡答題
在一定質量Cu(NO3)2、AgNO3和Al(NO3)3的混合溶液中加入過量的Zn,充分反應后,過濾,得到固體和溶液。
(1)請寫出一個有關反應的化學方程式。_____________________
(2)固體中含有的金屬有哪些?_____________________
(3)反應后所得溶液的質量與反應前相比,不能確定是增大、減小還是不變,為什么?_____________________
Zn+2AgNO3=Zn(NO3)2+2Ag[ 或Zn+Cu(NO3)2=Zn(NO3)2+Cu ] Ag 、Cu 、Zn 因為鋅與硝酸銀溶液反應,溶液質量減小;鋅與硝酸銅溶液反應,溶液質量增大。硝酸銀和硝酸銅的質量不確定,故不能確定反應后溶液的質量變化。 【解析】(1)鋅和硝酸銀反應生成硝酸鋅和銀,和硝酸銅反應生成硝酸鋅和銅,反應的化學方程式為:Zn+2AgNO3=Zn(NO3)2+2Ag...設計對比實驗是化學研究常用的方法,下圖是化學小組設計的鐵釘銹蝕條件的探究實驗。

(1)簡要敘述要達到實驗目的還需補充什么實驗?_____________________
(2)寫出用鹽酸除鐵銹(Fe2O3)的化學方程式。_____________________
查看答案請用化學方程式表示下列有關反應的原理:
(1) 生活中用天然氣作燃料:_____________________
(2)工業上用純堿和熟石灰反應制燒堿:_____________________
查看答案除去NaCl溶液中CaCl2、MgCl2、Na2SO4雜質的操作有:①溶解;②依次加過量的BaCl2、NaOH、Na2CO3溶液;③過濾;④加適量的鹽酸;⑤蒸發結晶。
(1)過濾后濾液中的溶質有_________種,過濾中玻璃棒的作用是____________。
(2)寫出一個加鹽酸后反應的化學方程式_________________________________。
查看答案已知A、B、C、D是四種不同種類的物質,它們有如圖的轉化關系(部分物質和反應條件略去)。A是年產量最高的金屬,B中氧元素占30%,D的水溶液呈藍色,常用于配制農藥波爾多液。則則A是__________;B→A的化學方程式為_________________;C→D的化學方程式為____________________________________。

根據下圖甲、乙兩種物質的溶解度曲線回答相關問題:

(1)在______℃時,甲、乙的溶解度相同。
(2)t2℃時,若將75 g甲的飽和溶液稀釋成10 %,需加水的質量為________g。
(3)將t2℃時,甲、乙兩種物質的飽和溶液降溫至t1℃(其他條件不變),所得溶液的溶質質量分數的關系是甲_________(填“>”、“<”或“=”)乙。
查看答案 試題屬性 Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
查看答案和解析>>
科目: 來源:河南省周口市西華縣2018屆九年級第一次模擬考試化學試卷 題型:實驗題
化學小組的同學在收集滿CO2的集氣瓶中放入燃燒的鈉,鈉繼續燃燒,充分反應后生成黑色的碳和一種白色固體。
(1)對于白色固體的成分,有下列猜想:①氧化鈉;②碳酸鈉;③氧化鈉和碳酸鈉的混合物;④氫氧化鈉;⑤碳酸氫鈉。以上猜想中肯定不合理的有_________(填序號)。
(2)請設計實驗方案證明猜想②正確,猜想①、③均不正確。(提示:氧化鈉為白色粉末,溶于水生成氫氧化鈉;碳酸鈉溶液呈堿性。)_____________________
④、⑤ 取白色粉末溶于水,加入足量的CaCl2溶液(或BaCl2溶液),出現白色沉淀,靜置,向上層清液中滴加酚酞溶液,溶液不變紅。可證明猜想②正確,猜想①、③均 不正確。 【解析】(1)以上不合理的猜想是④⑤,這是因為反應物中不含有氫元素,因此不可能生成氫氧化鈉和碳酸氫鈉;(2)實驗方案:取白色粉末溶于水,先加入足量的CaCl2溶液,出現白色沉淀,說明猜想②正確,過濾,向濾液里滴加酚酞...在一定質量Cu(NO3)2、AgNO3和Al(NO3)3的混合溶液中加入過量的Zn,充分反應后,過濾,得到固體和溶液。
(1)請寫出一個有關反應的化學方程式。_____________________
(2)固體中含有的金屬有哪些?_____________________
(3)反應后所得溶液的質量與反應前相比,不能確定是增大、減小還是不變,為什么?_____________________
查看答案設計對比實驗是化學研究常用的方法,下圖是化學小組設計的鐵釘銹蝕條件的探究實驗。

(1)簡要敘述要達到實驗目的還需補充什么實驗?_____________________
(2)寫出用鹽酸除鐵銹(Fe2O3)的化學方程式。_____________________
查看答案請用化學方程式表示下列有關反應的原理:
(1) 生活中用天然氣作燃料:_____________________
(2)工業上用純堿和熟石灰反應制燒堿:_____________________
查看答案除去NaCl溶液中CaCl2、MgCl2、Na2SO4雜質的操作有:①溶解;②依次加過量的BaCl2、NaOH、Na2CO3溶液;③過濾;④加適量的鹽酸;⑤蒸發結晶。
(1)過濾后濾液中的溶質有_________種,過濾中玻璃棒的作用是____________。
(2)寫出一個加鹽酸后反應的化學方程式_________________________________。
查看答案已知A、B、C、D是四種不同種類的物質,它們有如圖的轉化關系(部分物質和反應條件略去)。A是年產量最高的金屬,B中氧元素占30%,D的水溶液呈藍色,常用于配制農藥波爾多液。則則A是__________;B→A的化學方程式為_________________;C→D的化學方程式為____________________________________。

 Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
查看答案和解析>>
科目: 來源:河南省周口市西華縣2018屆九年級第一次模擬考試化學試卷 題型:科學探究題
實驗是科學探究的重要途徑。
(1)①下列實驗儀器不能用于加熱的是_______(填字母代號)。
a.燒杯 b.量筒 c.試管 d.蒸發皿
②做鐵絲在氧氣中燃燒實驗時,集氣瓶中預先加少量水或鋪一層細沙的目的是___________?
③配制質量分數為5%的NaCl溶液,若量取水時仰視量筒讀數(其他操作都正確),所得溶液的質量分數________5%(填“大于”、“小于”或“等于”)。
(2)實驗室選用以下裝置制取純凈、干燥的CO2,并驗證其部分性質。
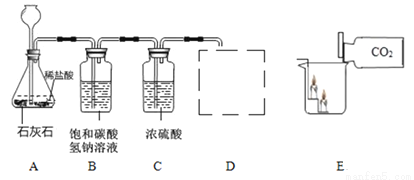
①B裝置中發生反應的化學方程式為______________________________________。
②C裝置中濃硫酸的作用是___________________。
③請在D中簡要補畫出CO2的收集裝置圖。 ________________
④由E可驗證CO2具有哪些性質?________________
(3)取12.5 g石灰石于裝置A中,向其中加入100 g足量的稀鹽酸,充分反應后(雜質不參加反應),A中固液混合物的質量為108.1 g,請計算該石灰石中碳酸鈣的質量分數________________。
b 防止濺落的熔融物炸裂瓶底 小于 NaHCO3+HCl=NaCl+H2O+CO2↑ 干燥氣體 密度比空氣大,不燃燒也不支持燃燒 80% 【解析】(1)①燒杯在加熱時需要墊上石棉網,試管和蒸發皿可直接加熱,量筒不能加熱;②做鐵絲在氧氣中燃燒實驗時,由于鐵燃燒放出了大量的熱,集氣瓶中預先加少量水或鋪一層細沙的目的是:防止濺落的熔化物炸裂瓶底;③量取水時仰視凹液面最低處,會使得量取水的體積偏大,...化學小組的同學在收集滿CO2的集氣瓶中放入燃燒的鈉,鈉繼續燃燒,充分反應后生成黑色的碳和一種白色固體。
(1)對于白色固體的成分,有下列猜想:①氧化鈉;②碳酸鈉;③氧化鈉和碳酸鈉的混合物;④氫氧化鈉;⑤碳酸氫鈉。以上猜想中肯定不合理的有_________(填序號)。
(2)請設計實驗方案證明猜想②正確,猜想①、③均不正確。(提示:氧化鈉為白色粉末,溶于水生成氫氧化鈉;碳酸鈉溶液呈堿性。)_____________________
查看答案在一定質量Cu(NO3)2、AgNO3和Al(NO3)3的混合溶液中加入過量的Zn,充分反應后,過濾,得到固體和溶液。
(1)請寫出一個有關反應的化學方程式。_____________________
(2)固體中含有的金屬有哪些?_____________________
(3)反應后所得溶液的質量與反應前相比,不能確定是增大、減小還是不變,為什么?_____________________
查看答案設計對比實驗是化學研究常用的方法,下圖是化學小組設計的鐵釘銹蝕條件的探究實驗。

(1)簡要敘述要達到實驗目的還需補充什么實驗?_____________________
(2)寫出用鹽酸除鐵銹(Fe2O3)的化學方程式。_____________________
查看答案請用化學方程式表示下列有關反應的原理:
(1) 生活中用天然氣作燃料:_____________________
(2)工業上用純堿和熟石灰反應制燒堿:_____________________
查看答案除去NaCl溶液中CaCl2、MgCl2、Na2SO4雜質的操作有:①溶解;②依次加過量的BaCl2、NaOH、Na2CO3溶液;③過濾;④加適量的鹽酸;⑤蒸發結晶。
(1)過濾后濾液中的溶質有_________種,過濾中玻璃棒的作用是____________。
(2)寫出一個加鹽酸后反應的化學方程式_________________________________。
查看答案 試題屬性 Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
查看答案和解析>>
科目: 來源:北京一零一中學2018屆九年級3月月考化學試卷 題型:單選題
地殼中含量最多的金屬元素是
A. 鋁 B. 硅 C. 氧 D. 鐵
A 【解析】地殼中元素含量前幾位的順序為氧、硅、鋁、鐵,故含量最多的金屬元素是鋁,故選A。化學興趣小組對某品牌牙膏中碳酸鈣含量進行以下探究。該牙膏摩擦劑主要由碳酸鈣、氫氧化鋁組成,其他成分遇到鹽酸時無氣體生成。現利用下圖所示裝置(圖中夾持儀器略去)進行實驗,充分反應后,測定B中生成的BaCO3沉淀質量,以確定碳酸鈣的質量分數。請回答下列問題。(已知:堿石灰固體的主要成分是生石灰和燒堿)
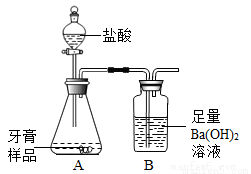
(1)裝置A中牙膏樣品放置在_______(填儀器名稱)中,鹽酸放置在裝置______(填儀器名稱)中,A中至少發生___(填數字)個反應,寫出其中一個反應的化學方程式______
(2)若測定值比實際值小,可能的原因有________________(填字母)
a.裝置A中水蒸氣、HCl等進入裝置B中
b.裝置A中CO2未完全進入裝置B
c.CO2氣流速度太快導致Ba(OH)2未完全吸收
d.鹽酸未滴加過量
(3)為減少誤差,現采取以下一些措施:
①在A、B之間增加一個裝有_____(填化學式)溶液的洗氣瓶,它的作用是___;
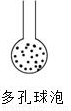
②若將裝置B中的長導管下方增加一個多孔球泡,作用是___;
③若將裝置A的前面再增加一個鼓入氮氣的裝置,目的是_____________;
④若在裝置B的后面再增加一個裝有堿石灰固體的干燥管,目的是___________________
(4)準確稱取三份各16.00g的樣品,進行測定,測得BaCO3質量分別為3.96g、3.92g、3.94g。請計算樣品中碳酸鈣的質量分數。(寫出計算過程)_______
(5)某同學利用上述方法測定牙膏中鈣元素的質量分數。小李同學認為即使即使排除實驗儀器和操作的影響,上述測定的結果仍有可能偏小,理由是:
_______。
查看答案雜鹵石(K2SO4·MgSO4·2 CaSO4·2H2O)屬于“呆礦”,為能充分利用鉀資源,用飽和的Ca(OH)2溶液浸雜鹵石制備硫酸鉀,工藝流程如下:
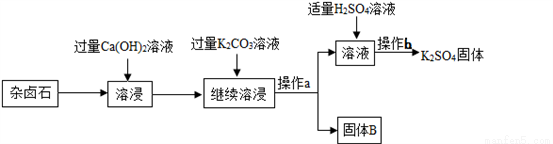
已知:
物質 | CaSO4 | K2SO4 | Mg(OH)2 |
溶解度/g(25℃) | 0.28 | 11.1 | 0.00084 |
(1)操作a的名稱為________,該操作中玻璃棒的作用是___________。
(2)固體B的主要成分有________和________。
(3)操作b的步驟是蒸發濃縮、________、過濾、洗滌。
(4)在實驗流程中加入過量的K2CO3溶液,能除去的物質是______________;
(5)在使用Ca(OH) 2溶液和K2CO3溶液對雜鹵石進行“溶浸”時,為探究獲得較高浸出雜鹵石主要成分的浸取率,某實驗小組用測得浸取液中K+的質量分數來表示浸取率,在相同的時間里,進行了如表實驗組:
實驗 | 溫度/℃ | Ca(OH)2用量/g | K+浸取率/% |
① | 25 | 2.5 | 72.4 |
② | 40 | 2.5 | 86.55 |
③ | 40 | 3 | 90.02 |
④ | 60 | 3 | 91.98 |
⑤ | 60 | 4 | 91.45 |
①上述實驗的數據中,溫度與K+浸取率的關系是_______________
②如表所列出的5組實驗中,若要獲得最佳的K+浸取率,選擇的反應條件是________℃和_____________g 的Ca(OH)2用量
查看答案數十年來,化學工作者對碳的氧化物和氫化物做了廣泛深入的研究并取得了一些重要成果。
(1)工業上常采用將水蒸氣噴到灼熱的炭層上實現煤的氣化(制得CO、H2),該反應的化學方程式是_______,制得的CO是一種有毒氣體,能降低_________的攜氧能力。
(2)上述煤氣化過程中需向炭層交替噴入空氣和水蒸氣,噴入空氣的目的是________;氣化得到的氣體可在加熱和催化劑下合成液體燃料甲醇CH3OH,該反應方程式為
________________________________________。
(3)科學家用氮化鎵材料與銅組裝如圖的人工光合系統,利用該裝置成功地實現了以CO2和H2O合成CH4。
①寫出合成甲烷的化學方程式_________。
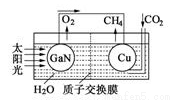
②為提高該人工光合系統的工作效率,可向裝置中加入少量的_______(選填“氫氧化鈉”或“硫酸”)。
查看答案今年,中國網民已將“貴州茅臺”酒列入奢侈品行列,茅臺酒價格一漲再漲,一瓶難求。

①俗話說“酒是陳的香”,聞到香味說明______,將50ml的酒精與50ml的水混合體積小于100ml,這是由于______。
② 釀造需要用到大量的軟水以除去礦物鹽,常用______檢驗軟水和硬水,生活中常用______的辦法將硬水轉化為軟水。
釀造需要用到大量的軟水以除去礦物鹽,常用______檢驗軟水和硬水,生活中常用______的辦法將硬水轉化為軟水。
③目前我國已經開始推廣使用乙醇汽油,乙醇汽油屬于_________ (填“混合物”或“純凈物”) 
 。寫出乙醇(化學式C2H6O)完全燃燒的化學方程式_______________________。
。寫出乙醇(化學式C2H6O)完全燃燒的化學方程式_______________________。
④科學研究發現,過量飲酒有害無益。酒精可以麻痹大腦內的神經,容易出事故。酒后駕駛是一種違法行為。交警通過酒精檢測儀顯示的顏色變化,可快速測出司機是否酒后駕車。其反應原理為:2CrO3(紅色)+3C2H5OH+3H2SO4 = Cr2(SO4)3(綠色)+3CH3CHO+6X,其中X的化學式為____________。
查看答案(1)鋁、鐵、銅是我們生活中常見的金屬.
①下列生活用品中,主要利用金屬具有良好導熱性的是___________ 填序號)
填序號)  。
。
A. 鐵鍋 B.
鐵鍋 B. 鋼導線 C.
鋼導線 C. 鋁制易拉罐
鋁制易拉罐
②鋁具有很好的抗腐蝕性能,原因是_______(用化學方程式表示)。
③在高溫下,利用焦炭與氧氣反應生成的一氧化碳可把鐵從鐵礦石里還原出來。其中焦炭的作用是:提供熱量和____________,高爐煉出來的鐵是生鐵,生鐵的含碳量為________。
④家用鐵鍋未洗凈晾干,放置一段時間后出現紅褐色銹斑,其主要的原因是鐵與________和_________接觸,發生了銹蝕。寫出生活中預防鐵鍋生銹的方法:_________。
(2)秋葵是一種大眾喜愛的食材,含有蛋白質、維生素A、維生素C、纖維素、阿拉伯聚糖和豐富的鐵、鋅、鈣等元素,其中:

①屬于人體所需微量元素的是_________,缺_________易導致骨質疏松。
②屬于糖類的有阿拉伯聚糖、_________,所填物質_________(填“屬于”或“不屬于”)有機高分子化合物。
③蛋白質在人體內最終的水解產物為氨基酸,寫出生活中另一種富含蛋白質的物質________。
查看答案 試題屬性 Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
查看答案和解析>>
科目: 來源:北京一零一中學2018屆九年級3月月考化學試卷 題型:單選題
決定元素種類的是
A. 核外電子數 B. 中子數 C. 質子數 D. 最外層電子數
C 【解析】質子數決定元素是種類,核外電子數決定元素的化學性質,故選C。地殼中含量最多的金屬元素是
A. 鋁 B. 硅 C. 氧 D. 鐵
查看答案化學興趣小組對某品牌牙膏中碳酸鈣含量進行以下探究。該牙膏摩擦劑主要由碳酸鈣、氫氧化鋁組成,其他成分遇到鹽酸時無氣體生成。現利用下圖所示裝置(圖中夾持儀器略去)進行實驗,充分反應后,測定B中生成的BaCO3沉淀質量,以確定碳酸鈣的質量分數。請回答下列問題。(已知:堿石灰固體的主要成分是生石灰和燒堿)


(1)裝置A中牙膏樣品放置在_______(填儀器名稱)中,鹽酸放置在裝置______(填儀器名稱)中,A中至少發生___(填數字)個反應,寫出其中一個反應的化學方程式______
(2)若測定值比實際值小,可能的原因有________________(填字母)
a.裝置A中水蒸氣、HCl等進入裝置B中
b.裝置A中CO2未完全進入裝置B
c.CO2氣流速度太快導致Ba(OH)2未完全吸收
d.鹽酸未滴加過量
(3)為減少誤差,現采取以下一些措施:
①在A、B之間增加一個裝有_____(填化學式)溶液的洗氣瓶,它的作用是___;
②若將裝置B中的長導管下方增加一個多孔球泡,作用是___;
③若將裝置A的前面再增加一個鼓入氮氣的裝置,目的是_____________;
④若在裝置B的后面再增加一個裝有堿石灰固體的干燥管,目的是___________________
(4)準確稱取三份各16.00g的樣品,進行測定,測得BaCO3質量分別為3.96g、3.92g、3.94g。請計算樣品中碳酸鈣的質量分數。(寫出計算過程)_______
(5)某同學利用上述方法測定牙膏中鈣元素的質量分數。小李同學認為即使即使排除實驗儀器和操作的影響,上述測定的結果仍有可能偏小,理由是:
_______。
查看答案雜鹵石(K2SO4·MgSO4·2 CaSO4·2H2O)屬于“呆礦”,為能充分利用鉀資源,用飽和的Ca(OH)2溶液浸雜鹵石制備硫酸鉀,工藝流程如下:

已知:
物質 | CaSO4 | K2SO4 | Mg(OH)2 |
溶解度/g(25℃) | 0.28 | 11.1 | 0.00084 |
(1)操作a的名稱為________,該操作中玻璃棒的作用是___________。
(2)固體B的主要成分有________和________。
(3)操作b的步驟是蒸發濃縮、________、過濾、洗滌。
(4)在實驗流程中加入過量的K2CO3溶液,能除去的物質是______________;
(5)在使用Ca(OH) 2溶液和K2CO3溶液對雜鹵石進行“溶浸”時,為探究獲得較高浸出雜鹵石主要成分的浸取率,某實驗小組用測得浸取液中K+的質量分數來表示浸取率,在相同的時間里,進行了如表實驗組:
實驗 | 溫度/℃ | Ca(OH)2用量/g | K+浸取率/% |
① | 25 | 2.5 | 72.4 |
② | 40 | 2.5 | 86.55 |
③ | 40 | 3 | 90.02 |
④ | 60 | 3 | 91.98 |
⑤ | 60 | 4 | 91.45 |
①上述實驗的數據中,溫度與K+浸取率的關系是_______________
②如表所列出的5組實驗中,若要獲得最佳的K+浸取率,選擇的反應條件是________℃和_____________g 的Ca(OH)2用量
查看答案數十年來,化學工作者對碳的氧化物和氫化物做了廣泛深入的研究并取得了一些重要成果。
(1)工業上常采用將水蒸氣噴到灼熱的炭層上實現煤的氣化(制得CO、H2),該反應的化學方程式是_______,制得的CO是一種有毒氣體,能降低_________的攜氧能力。
(2)上述煤氣化過程中需向炭層交替噴入空氣和水蒸氣,噴入空氣的目的是________;氣化得到的氣體可在加熱和催化劑下合成液體燃料甲醇CH3OH,該反應方程式為
________________________________________。
(3)科學家用氮化鎵材料與銅組裝如圖的人工光合系統,利用該裝置成功地實現了以CO2和H2O合成CH4。
①寫出合成甲烷的化學方程式_________。

②為提高該人工光合系統的工作效率,可向裝置中加入少量的_______(選填“氫氧化鈉”或“硫酸”)。
查看答案今年,中國網民已將“貴州茅臺”酒列入奢侈品行列,茅臺酒價格一漲再漲,一瓶難求。

①俗話說“酒是陳的香”,聞到香味說明______,將50ml的酒精與50ml的水混合體積小于100ml,這是由于______。
② 釀造需要用到大量的軟水以除去礦物鹽,常用______檢驗軟水和硬水,生活中常用______的辦法將硬水轉化為軟水。
釀造需要用到大量的軟水以除去礦物鹽,常用______檢驗軟水和硬水,生活中常用______的辦法將硬水轉化為軟水。
③目前我國已經開始推廣使用乙醇汽油,乙醇汽油屬于_________ (填“混合物”或“純凈物”) 
 。寫出乙醇(化學式C2H6O)完全燃燒的化學方程式_______________________。
。寫出乙醇(化學式C2H6O)完全燃燒的化學方程式_______________________。
④科學研究發現,過量飲酒有害無益。酒精可以麻痹大腦內的神經,容易出事故。酒后駕駛是一種違法行為。交警通過酒精檢測儀顯示的顏色變化,可快速測出司機是否酒后駕車。其反應原理為:2CrO3(紅色)+3C2H5OH+3H2SO4 = Cr2(SO4)3(綠色)+3CH3CHO+6X,其中X的化學式為____________。
查看答案 試題屬性 Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
查看答案和解析>>
科目: 來源:北京一零一中學2018屆九年級3月月考化學試卷 題型:單選題
銅絲常用于制作電線,主要是因為銅具有
A. 導熱性 B. 導電性 C. 密度較大 D. 抗腐蝕性
B 【解析】銅具有導電性,故銅可以做導線,故選B。決定元素種類的是
A. 核外電子數 B. 中子數 C. 質子數 D. 最外層電子數
查看答案地殼中含量最多的金屬元素是
A. 鋁 B. 硅 C. 氧 D. 鐵
查看答案化學興趣小組對某品牌牙膏中碳酸鈣含量進行以下探究。該牙膏摩擦劑主要由碳酸鈣、氫氧化鋁組成,其他成分遇到鹽酸時無氣體生成。現利用下圖所示裝置(圖中夾持儀器略去)進行實驗,充分反應后,測定B中生成的BaCO3沉淀質量,以確定碳酸鈣的質量分數。請回答下列問題。(已知:堿石灰固體的主要成分是生石灰和燒堿)


(1)裝置A中牙膏樣品放置在_______(填儀器名稱)中,鹽酸放置在裝置______(填儀器名稱)中,A中至少發生___(填數字)個反應,寫出其中一個反應的化學方程式______
(2)若測定值比實際值小,可能的原因有________________(填字母)
a.裝置A中水蒸氣、HCl等進入裝置B中
b.裝置A中CO2未完全進入裝置B
c.CO2氣流速度太快導致Ba(OH)2未完全吸收
d.鹽酸未滴加過量
(3)為減少誤差,現采取以下一些措施:
①在A、B之間增加一個裝有_____(填化學式)溶液的洗氣瓶,它的作用是___;
②若將裝置B中的長導管下方增加一個多孔球泡,作用是___;
③若將裝置A的前面再增加一個鼓入氮氣的裝置,目的是_____________;
④若在裝置B的后面再增加一個裝有堿石灰固體的干燥管,目的是___________________
(4)準確稱取三份各16.00g的樣品,進行測定,測得BaCO3質量分別為3.96g、3.92g、3.94g。請計算樣品中碳酸鈣的質量分數。(寫出計算過程)_______
(5)某同學利用上述方法測定牙膏中鈣元素的質量分數。小李同學認為即使即使排除實驗儀器和操作的影響,上述測定的結果仍有可能偏小,理由是:
_______。
查看答案雜鹵石(K2SO4·MgSO4·2 CaSO4·2H2O)屬于“呆礦”,為能充分利用鉀資源,用飽和的Ca(OH)2溶液浸雜鹵石制備硫酸鉀,工藝流程如下:

已知:
物質 | CaSO4 | K2SO4 | Mg(OH)2 |
溶解度/g(25℃) | 0.28 | 11.1 | 0.00084 |
(1)操作a的名稱為________,該操作中玻璃棒的作用是___________。
(2)固體B的主要成分有________和________。
(3)操作b的步驟是蒸發濃縮、________、過濾、洗滌。
(4)在實驗流程中加入過量的K2CO3溶液,能除去的物質是______________;
(5)在使用Ca(OH) 2溶液和K2CO3溶液對雜鹵石進行“溶浸”時,為探究獲得較高浸出雜鹵石主要成分的浸取率,某實驗小組用測得浸取液中K+的質量分數來表示浸取率,在相同的時間里,進行了如表實驗組:
實驗 | 溫度/℃ | Ca(OH)2用量/g | K+浸取率/% |
① | 25 | 2.5 | 72.4 |
② | 40 | 2.5 | 86.55 |
③ | 40 | 3 | 90.02 |
④ | 60 | 3 | 91.98 |
⑤ | 60 | 4 | 91.45 |
①上述實驗的數據中,溫度與K+浸取率的關系是_______________
②如表所列出的5組實驗中,若要獲得最佳的K+浸取率,選擇的反應條件是________℃和_____________g 的Ca(OH)2用量
查看答案數十年來,化學工作者對碳的氧化物和氫化物做了廣泛深入的研究并取得了一些重要成果。
(1)工業上常采用將水蒸氣噴到灼熱的炭層上實現煤的氣化(制得CO、H2),該反應的化學方程式是_______,制得的CO是一種有毒氣體,能降低_________的攜氧能力。
(2)上述煤氣化過程中需向炭層交替噴入空氣和水蒸氣,噴入空氣的目的是________;氣化得到的氣體可在加熱和催化劑下合成液體燃料甲醇CH3OH,該反應方程式為
________________________________________。
(3)科學家用氮化鎵材料與銅組裝如圖的人工光合系統,利用該裝置成功地實現了以CO2和H2O合成CH4。
①寫出合成甲烷的化學方程式_________。

②為提高該人工光合系統的工作效率,可向裝置中加入少量的_______(選填“氫氧化鈉”或“硫酸”)。
查看答案 試題屬性 Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
查看答案和解析>>
科目: 來源:北京一零一中學2018屆九年級3月月考化學試卷 題型:單選題
下列操作合理的是
A. 用完酒精燈后,用嘴立即吹滅
B. 加熱后的試管,立即用冷水沖洗干凈
C. 加熱時試管內液體體積不超過試管容積的1/3
D. 使用試管加熱任何試劑,試管口都應略向下傾斜
C 【解析】A、酒精燈應該用燈帽蓋滅,不能用嘴吹滅,錯誤; B、加熱后的試管,不能立即用冷水沖洗,否則會引起試管炸裂,錯誤; C、加熱時試管內液體體積不超過試管容積的1/3,正確; D、加熱液體時試管口向上傾斜,錯誤。故選C。銅絲常用于制作電線,主要是因為銅具有
A. 導熱性 B. 導電性 C. 密度較大 D. 抗腐蝕性
查看答案決定元素種類的是
A. 核外電子數 B. 中子數 C. 質子數 D. 最外層電子數
查看答案地殼中含量最多的金屬元素是
A. 鋁 B. 硅 C. 氧 D. 鐵
查看答案化學興趣小組對某品牌牙膏中碳酸鈣含量進行以下探究。該牙膏摩擦劑主要由碳酸鈣、氫氧化鋁組成,其他成分遇到鹽酸時無氣體生成。現利用下圖所示裝置(圖中夾持儀器略去)進行實驗,充分反應后,測定B中生成的BaCO3沉淀質量,以確定碳酸鈣的質量分數。請回答下列問題。(已知:堿石灰固體的主要成分是生石灰和燒堿)


(1)裝置A中牙膏樣品放置在_______(填儀器名稱)中,鹽酸放置在裝置______(填儀器名稱)中,A中至少發生___(填數字)個反應,寫出其中一個反應的化學方程式______
(2)若測定值比實際值小,可能的原因有________________(填字母)
a.裝置A中水蒸氣、HCl等進入裝置B中
b.裝置A中CO2未完全進入裝置B
c.CO2氣流速度太快導致Ba(OH)2未完全吸收
d.鹽酸未滴加過量
(3)為減少誤差,現采取以下一些措施:
①在A、B之間增加一個裝有_____(填化學式)溶液的洗氣瓶,它的作用是___;
②若將裝置B中的長導管下方增加一個多孔球泡,作用是___;
③若將裝置A的前面再增加一個鼓入氮氣的裝置,目的是_____________;
④若在裝置B的后面再增加一個裝有堿石灰固體的干燥管,目的是___________________
(4)準確稱取三份各16.00g的樣品,進行測定,測得BaCO3質量分別為3.96g、3.92g、3.94g。請計算樣品中碳酸鈣的質量分數。(寫出計算過程)_______
(5)某同學利用上述方法測定牙膏中鈣元素的質量分數。小李同學認為即使即使排除實驗儀器和操作的影響,上述測定的結果仍有可能偏小,理由是:
_______。
查看答案雜鹵石(K2SO4·MgSO4·2 CaSO4·2H2O)屬于“呆礦”,為能充分利用鉀資源,用飽和的Ca(OH)2溶液浸雜鹵石制備硫酸鉀,工藝流程如下:

已知:
物質 | CaSO4 | K2SO4 | Mg(OH)2 |
溶解度/g(25℃) | 0.28 | 11.1 | 0.00084 |
(1)操作a的名稱為________,該操作中玻璃棒的作用是___________。
(2)固體B的主要成分有________和________。
(3)操作b的步驟是蒸發濃縮、________、過濾、洗滌。
(4)在實驗流程中加入過量的K2CO3溶液,能除去的物質是______________;
(5)在使用Ca(OH) 2溶液和K2CO3溶液對雜鹵石進行“溶浸”時,為探究獲得較高浸出雜鹵石主要成分的浸取率,某實驗小組用測得浸取液中K+的質量分數來表示浸取率,在相同的時間里,進行了如表實驗組:
實驗 | 溫度/℃ | Ca(OH)2用量/g | K+浸取率/% |
① | 25 | 2.5 | 72.4 |
② | 40 | 2.5 | 86.55 |
③ | 40 | 3 | 90.02 |
④ | 60 | 3 | 91.98 |
⑤ | 60 | 4 | 91.45 |
①上述實驗的數據中,溫度與K+浸取率的關系是_______________
②如表所列出的5組實驗中,若要獲得最佳的K+浸取率,選擇的反應條件是________℃和_____________g 的Ca(OH)2用量
查看答案 試題屬性 Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
查看答案和解析>>
科目: 來源:北京一零一中學2018屆九年級3月月考化學試卷 題型:單選題
下列物質的用途中,主要利用了其物理性質的是
A.氧氣用于切割金屬 B.干冰用于制冷劑
C.酒精可用作燃料 D.焦炭可用于煉鐵
B 【解析】 試題分析:氧氣用于切割金屬,是利用氧氣具有助燃性的性質;干冰用于制冷劑是因為干冰升華要吸收大量的熱;酒精可用作燃料是因為酒精具有可燃性;焦炭可用于煉鐵是因為它具有還原性。故選B。 考點:物質的性質下列操作合理的是
A. 用完酒精燈后,用嘴立即吹滅
B. 加熱后的試管,立即用冷水沖洗干凈
C. 加熱時試管內液體體積不超過試管容積的1/3
D. 使用試管加熱任何試劑,試管口都應略向下傾斜
查看答案銅絲常用于制作電線,主要是因為銅具有
A. 導熱性 B. 導電性 C. 密度較大 D. 抗腐蝕性
查看答案決定元素種類的是
A. 核外電子數 B. 中子數 C. 質子數 D. 最外層電子數
查看答案地殼中含量最多的金屬元素是
A. 鋁 B. 硅 C. 氧 D. 鐵
查看答案化學興趣小組對某品牌牙膏中碳酸鈣含量進行以下探究。該牙膏摩擦劑主要由碳酸鈣、氫氧化鋁組成,其他成分遇到鹽酸時無氣體生成。現利用下圖所示裝置(圖中夾持儀器略去)進行實驗,充分反應后,測定B中生成的BaCO3沉淀質量,以確定碳酸鈣的質量分數。請回答下列問題。(已知:堿石灰固體的主要成分是生石灰和燒堿)


(1)裝置A中牙膏樣品放置在_______(填儀器名稱)中,鹽酸放置在裝置______(填儀器名稱)中,A中至少發生___(填數字)個反應,寫出其中一個反應的化學方程式______
(2)若測定值比實際值小,可能的原因有________________(填字母)
a.裝置A中水蒸氣、HCl等進入裝置B中
b.裝置A中CO2未完全進入裝置B
c.CO2氣流速度太快導致Ba(OH)2未完全吸收
d.鹽酸未滴加過量
(3)為減少誤差,現采取以下一些措施:
①在A、B之間增加一個裝有_____(填化學式)溶液的洗氣瓶,它的作用是___;
②若將裝置B中的長導管下方增加一個多孔球泡,作用是___;
③若將裝置A的前面再增加一個鼓入氮氣的裝置,目的是_____________;
④若在裝置B的后面再增加一個裝有堿石灰固體的干燥管,目的是___________________
(4)準確稱取三份各16.00g的樣品,進行測定,測得BaCO3質量分別為3.96g、3.92g、3.94g。請計算樣品中碳酸鈣的質量分數。(寫出計算過程)_______
(5)某同學利用上述方法測定牙膏中鈣元素的質量分數。小李同學認為即使即使排除實驗儀器和操作的影響,上述測定的結果仍有可能偏小,理由是:
_______。
查看答案 試題屬性 Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
查看答案和解析>>
科目: 來源:北京一零一中學2018屆九年級3月月考化學試卷 題型:單選題
亞硝酸鈉(NaNO2)是一種工業原料,人若誤食會引起中毒。亞硝酸鈉中氮元素化合價是
A. +3 B. -3 C. +1 D. -1
A 【解析】NaNO2中鈉元素的化合價為+1價,氧元素的化合價為-2價,根據化合價的代數和為哦可求得氮元素的化合價為+3價,故選A。下列物質的用途中,主要利用了其物理性質的是
A.氧氣用于切割金屬 B.干冰用于制冷劑
C.酒精可用作燃料 D.焦炭可用于煉鐵
查看答案下列操作合理的是
A. 用完酒精燈后,用嘴立即吹滅
B. 加熱后的試管,立即用冷水沖洗干凈
C. 加熱時試管內液體體積不超過試管容積的1/3
D. 使用試管加熱任何試劑,試管口都應略向下傾斜
查看答案銅絲常用于制作電線,主要是因為銅具有
A. 導熱性 B. 導電性 C. 密度較大 D. 抗腐蝕性
查看答案決定元素種類的是
A. 核外電子數 B. 中子數 C. 質子數 D. 最外層電子數
查看答案地殼中含量最多的金屬元素是
A. 鋁 B. 硅 C. 氧 D. 鐵
查看答案 試題屬性 Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
Copyright @ 2008-2013 滿分5 學習網 ManFen5.COM. All Rights Reserved.答案無憂
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com