
分析 (1)鐵絲與氧氣在點燃的條件下生成四氧化三鐵,據(jù)此寫出反應的化學方程式;
(2)鐵銹主要成分是氧化鐵,放入稀鹽酸后首先是鐵銹反應,鐵銹完全反應后鐵和稀鹽酸反應產(chǎn)生氣泡,據(jù)此分析解答即可;
(3)根據(jù)在煉鐵爐中碳的作用分析;
(4)根據(jù)三種金屬活動性強弱關系鐵>銅>銀,對將鐵粉和銅粉的混合物放入硝酸銀溶液中可能出現(xiàn)的變化進行分析,判斷反應結束后剩余固體成分.
解答 解:(1)鐵絲與氧氣在點燃的條件下生成四氧化三鐵,方程式是:3Fe+2O2$\frac{\underline{\;點燃\;}}{\;}$Fe3O4;
(2)生銹的鐵釘放入稀鹽酸中,先是表面的鐵銹的主要成分氧化鐵與鹽酸反應生成氯化鐵與水,當鐵銹完全反應后鐵與稀鹽酸發(fā)生反應,生成氯化亞鐵與氫氣,反應的化學方程式為:Fe+2HCl═FeCl2+H2↑;由題意可知,鐵能與氯化鐵反應生成氯化亞鐵,由于鐵有剩余,溶液中不含有鐵離子,子溶液中含有的氧離子時亞鐵離子,符號為:Fe2+;
(3)在煉鐵爐中焦炭的作用一是燃燒放出熱量,二是產(chǎn)生一氧化碳做還原劑,反應的方程式是:C+O2$\frac{\underline{\;點燃\;}}{\;}$CO2、CO2+C$\frac{\underline{\;高溫\;}}{\;}$2CO;
(4)A、根據(jù)三種金屬活動性強弱關系鐵>銅>銀,將鐵粉和銅粉的混合物放入硝酸銀溶液中,鐵粉、銅粉都能與硝酸銀發(fā)生反應得到銀,因此剩余固體中一定含有銀,故A對;
B、因未說明混合物的用量,因此對于固體混合物是否出現(xiàn)剩余則無法準確判斷,因此肯定有銀、可能有銅,故B錯;
C、因為鐵的質量無法確定,無法準確判斷是否把銅銀全部從其溶液中全部置換出來,所以反應后溶液中可能含有Ag+和Cu2+.故C錯;
D、多種金屬與一種金屬鹽溶液反應時最活潑的金屬先反應,鐵首先與硝酸銀反應生成硝酸亞鐵和銀,與硝酸銀完全反應后再與硝酸銅反應生成硝酸亞鐵和銅,故濾液中一定含有生成的硝酸亞鐵,此時無法判斷濾液中是否含有硝酸銅,故D錯.
故答為:(1)3Fe+2O2$\frac{\underline{\;點燃\;}}{\;}$Fe3O4;(2)Fe+2HCl═FeCl2+H2;Fe2+;(3)C+O2$\frac{\underline{\;點燃\;}}{\;}$CO2、CO2+C$\frac{\underline{\;高溫\;}}{\;}$2CO;(4)A.
點評 本題難度不大,考查學生根據(jù)金屬活動順序表,活動性強的金屬能將活動性弱的金屬從其鹽溶液中置換出來的有關知識.


 階梯計算系列答案
階梯計算系列答案科目:初中化學 來源: 題型:選擇題
| A. | +1 | B. | +3 | C. | +5 | D. | -1 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
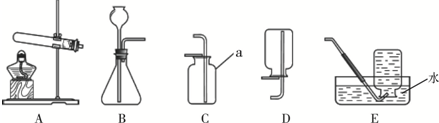
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 兩個N原子均為-3 | B. | 第一個N原子為+1 | C. | 第二個N原子為+3 | D. | 第二個N原子為+5 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
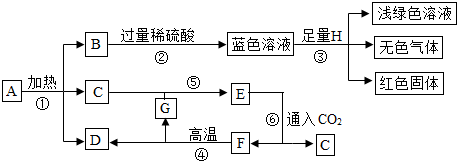
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 蒸發(fā)掉一半溶劑(恒溫) | B. | 蒸發(fā)掉25克溶劑(恒溫) | ||
| C. | 加入50克a%的該溶液 | D. | 加入0.5a克該溶質 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 硫酸鋇 | B. | 碳酸鋇 | C. | 碳酸銨 | D. | 硝酸銀 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com