
分析 (1)摩爾質量是指單位物質的量的物質所具有的質量,摩爾質量的單位為g/mol,在數值上等于該物質的相對原子質量或相對分子質量.1mol任何物質中含有6.02×1023個分子.
(2)①氫氧化鈉與硫酸銅溶液反應生成氫氧化銅沉淀和硫酸鈉,寫出反應的化學方程式即可.
②由參加反應的氫氧化鈉的物質的量,根據反應的化學方程式計算出生成氫氧化銅的物質的量即可.
解答 解:(1)摩爾質量是指單位物質的量的物質所具有的質量,氫氧化鈉的相對分子質量是23+16+1=40,故氫氧化鈉的摩爾質量是40g/mol.
1mol任何物質中含有6.02×1023個分子,一個氫氧化鈉分子含有1個氧原子,故3molNaOH中約含有中有3mol×1×6.02×1023個=1.806×1024個氧原子.
(2)①氫氧化鈉與硫酸銅溶液反應生成氫氧化銅沉淀和硫酸鈉,反應的化學方程式為:2NaOH+CuSO4═Na2SO4+Cu(OH)2↓.
②設生成的氫氧化銅的物質的量為x
2NaOH+CuSO4═Na2SO4+Cu(OH)2↓
2 1
0.1mol x
$\frac{2}{1}=\frac{0.1mol}{x}$ x=0.05mol
質量為0.05mol×98g/mol=4.9g.
故答案為:(1)40g/mol;1.806×1024;(2)①2NaOH+CuSO4═Na2SO4+Cu(OH)2↓;②0.05;4.9.
點評 本題難度不大,掌握根據化學方程式的計算、化學式的有關計算是正確解答本題的關鍵.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:初中化學 來源: 題型:選擇題
| A. | KOH | B. | Mg(OH)2 | C. | CuSO4 | D. | Ca(OH)2 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| 選項 | 物質 | 所含雜質 | 除去雜質的方法 |
| A | H2 | HCl | 將氣體通過NaOH溶液,干燥 |
| B | FeCl2 | CuCl2 | 加入過量的鐵粉,過濾 |
| C | MnO2 | KCl | 加足量水溶解,過濾、洗滌,干燥 |
| D | CaO | CaCO3 | 加足量水溶解,過濾、蒸發、結晶 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
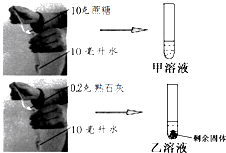 小明同學為探究物質的溶解性進行如圖實驗,圖中環境溫度為20℃,從圖中數據分析可知:
小明同學為探究物質的溶解性進行如圖實驗,圖中環境溫度為20℃,從圖中數據分析可知:查看答案和解析>>
科目:初中化學 來源: 題型:解答題
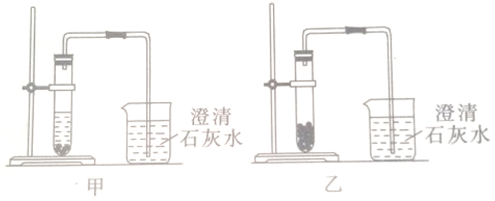
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 濾液中一定含有ZnSO4 | B. | 濾渣中一定沒有鐵粉 | ||
| C. | 濾液中可能含有FeSO4 | D. | 濾渣中一定有鋅粉 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
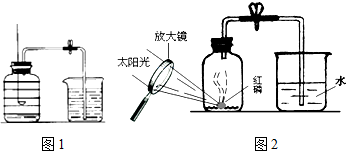
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com