
| 實驗 | 1 | 2 | 3 | 4 |
| 加入礦石的質量/g | 5 | 10 | 15 | 20 |
| 生成CO2的質量/g | 1.76 | 3.52 | 4.4 | m |
分析 (1)觀察并對比表格中的數據可知:第2次實驗中的數據均為第一次實驗的兩倍,而第3次少,說明此時鹽酸已完全反應,故3、4次實驗中碳酸鈣有剩余,且生成二氧化碳的質量相等,即m=4.4;碳酸鈣的質量分數可根據第1次或第2次實驗中二氧化碳的質量求出.根據化學方程式得出各物質之間的質量比,列出比例式,即可求出參加反應的CaCO3的質量,然后再根據質量分數公式進行計算即可.
解答 解:(1)由表格中的數據可知,第3次反應已是完全反應,故第3、4次反應中的碳酸鈣的質量有剩余.
(2)因為第3次反應已是完全反應,不再有氣體產生,故第四次反應生成的氣體質量的第三次的一樣多,即m=4.4.
(3)設第1次實驗中樣品中的碳酸鈣的質量為x,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 1.76g
$\frac{100}{44}=\frac{x}{1.76g}$ 解之得:x=4g,
石灰石中碳酸鈣的質量分數為:$\frac{4g}{5g}×100%$=80%.
故答為:(1)3、4;(2)4.4;(3)石灰石中碳酸鈣的質量分數為80%.
點評 本題主要考查學生對完全反應的概念的認識,以及運用化學方程式和質量分數公式進行計算的能力.


科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
| 實驗操作 | 實驗現象 | 實驗結論 |
| (1)取少量固體于試管中,加適量水振蕩后靜置,再滴幾滴無色酚酞試液 | 溶液變紅 | 說明固體成分中一定含有 氧化鈣 |
| (2)再取少量固體于另一試管中滴加過量稀鹽酸 | 有氣泡生成 | 說明固體成分中一定含有碳酸鈣 |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
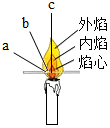 為了探究蠟燭燃燒的現象,做了表中的實驗,請你幫忙完成實驗報告的內容:
為了探究蠟燭燃燒的現象,做了表中的實驗,請你幫忙完成實驗報告的內容:| 實驗步驟 | 實驗現象 | 結論 |
| 點燃蠟燭,將一根火柴橫在火焰上方片刻; | 火柴梗的a(填“a”、“b”或“c”)處最先碳化. | 蠟燭火焰的外焰溫度最高. |
| 將一只干冷的燒杯罩在火焰上方; | 燒杯內壁出現水霧. | 說明蠟燭燃燒生成了水. |
| 將一只內壁附有澄清石灰水的燒杯罩在火焰上方. | 燒杯內壁有白色固體生成 | 說明蠟燭燃燒還生成二氧化碳. 蠟燭燃燒的文字表達式為:石蠟+氧氣$\stackrel{點燃}{→}$水+二氧化碳. |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
| 實驗步驟 | 實驗現象 | 結論 |
| ①取樣,加入過量的CaCl2溶液,過濾 | 產生白色沉淀 | 猜想3 成立 |
| ②向上述濾液中滴加幾滴無色酚酞溶液 | 酚酞溶液變紅 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
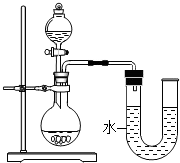 化學反應中通常伴隨有能量的變化,可借助反應前后的溫度變化來判斷反應的發生.將7.3%的鹽酸和8%的NaOH溶液各10mL混合,用溫度計測量發現混合后溫度比混合前升高了,從而證明氫氧化鈉溶液與稀鹽酸發生了反應.
化學反應中通常伴隨有能量的變化,可借助反應前后的溫度變化來判斷反應的發生.將7.3%的鹽酸和8%的NaOH溶液各10mL混合,用溫度計測量發現混合后溫度比混合前升高了,從而證明氫氧化鈉溶液與稀鹽酸發生了反應.查看答案和解析>>
科目:初中化學 來源: 題型:解答題
 以化合價為縱坐標,物質的類別為橫坐標所繪制的圖象叫價類圖.如圖為硫的價類圖,請分析該圖后填空:
以化合價為縱坐標,物質的類別為橫坐標所繪制的圖象叫價類圖.如圖為硫的價類圖,請分析該圖后填空:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com