
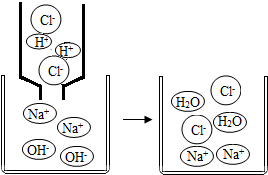
 初中化學中,我們學習了酸和堿發生中和反應的實質是H++OH-═H2O.如圖,像這種用實際參加反應的離子符號來表示反應的式子叫離子方程式.離子方程式的書寫一般按以下步驟:(以Na2SO4與BaCl2反應為例)
初中化學中,我們學習了酸和堿發生中和反應的實質是H++OH-═H2O.如圖,像這種用實際參加反應的離子符號來表示反應的式子叫離子方程式.離子方程式的書寫一般按以下步驟:(以Na2SO4與BaCl2反應為例)分析 根據反應原理寫出反應的化學方程式;
(1)離子之間不反應生成氣體、沉淀、弱電解質或絡合物或發生氧化還原反應、雙水解反應的就能共存,據此分析解答.
(2)反應生成氯化鈣、水、二氧化碳,水、二氧化碳、碳酸鈣在離子反應中保留化學式;
(2)反應生成KCl和碘,氯氣、碘在離子反應中保留化學式.
(3)非氧化性的強酸如稀硫酸、稀鹽酸與金屬鎂的反應.
(4)復分解反應實質上就是兩種化合物在溶液中相互交換離子的反應,生成物中有氣體或沉淀或水;反應就能發生.
解答 解:Na2SO4與BaCl2反應的化學方程式:Na2SO4+BaCl2=BaSO4↓+2NaCl;
(1)A.這幾種離子之間不反應,所以能大量共存,故正確;
B、H+ 和OH- 反應生水,故錯誤;
C、這幾種離子之間不反應,所以能大量共存,故正確;
D.H+ 和 CO32- 反應生成二氧化碳和水,故錯誤;
(2)石灰石和鹽酸反應的離子反應為:CaCO3+2H+=Ca2++H2O+CO2↑;故填:CaCO3+2H+=Ca2++H2O+CO2↑;
(3)與離子方程式Mg+2H+=Mg2++H2↑相對應的化學方程式:Mg+H2SO4=MgSO4+H2↑或Mg+2HCl=MgCl2+H2↑;故填:Mg+H2SO4=MgSO4+H2↑或Mg+2HCl=MgCl2+H2↑.
(4)復分解反應實質上就是兩種化合物在溶液中相互交換離子的反應,生成物中有氣體或沉淀或水;反應就能發生.故填:水.
答案:Na2SO4+BaCl2=BaSO4↓+2NaCl
(1)AC;
(2)CaCO3+2H+=Ca2++H2O+CO2↑;
(3)Mg+H2SO4=MgSO4+H2↑或Mg+2HCl=MgCl2+H2↑.
(4)水.
點評 本題考查的是復分解反應的條件和復分解反應的實質,完成此題,可以依據已有的知識進行.


科目:初中化學 來源: 題型:實驗探究題
 我國古代將爐甘石(主要成分:ZnCO3)、赤銅礦(主要成分:Cu2O)和木炭粉為原料值得來黃銅(銅和鋅的合金,外觀似黃金),其生產流程如下:
我國古代將爐甘石(主要成分:ZnCO3)、赤銅礦(主要成分:Cu2O)和木炭粉為原料值得來黃銅(銅和鋅的合金,外觀似黃金),其生產流程如下:查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
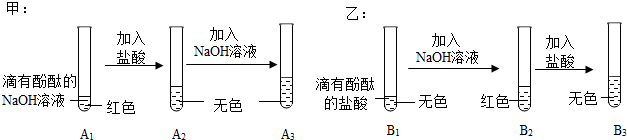
| 探究 環節 | 甲同學的探究 | 乙同學的探究 |
| 提出 問題 | A3溶液為什么不變紅? | B3溶液中溶質成分是什么?(酚酞不計) |
| 做出 猜想 | 實驗過程中,酚酞變質了? | 猜想一:NaCl 猜想二:NaCl HCl |
實驗 驗證 | (1)取少量A3溶液于另一試管中,向其中滴加NaOH溶液,溶液變紅,說明甲同學的猜想不成立(填“成立”或“不成立”) (2)你認為在常溫下A2溶液測出的pH <(填“>”、“=”或“<”)7 | 取少量B3溶液加入盛有少量鐵粉的試管中,觀察到有無色氣泡產生,固體逐漸減少,溶液由無色變淺綠色,你認為乙同學的猜想二.(填“一”或“二”)成立 |
交流 反思 | (1)甲、乙同學的實驗中,反應均涉及到的化學方程式是NaOH+HCl=NaCl+H2O. (2)A3溶液未變紅,你認為原因是A2溶液中鹽酸較多,加入的NaOH溶液未將其完全中和. (3)甲、乙同學經過實驗對比探究,認為做化學實驗時應注意藥品用量的控制. | |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題

查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
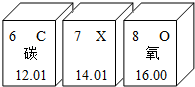 如圖為元素周期表的一部分(x元素信息不全).下列說法正確的是( )
如圖為元素周期表的一部分(x元素信息不全).下列說法正確的是( )| A. | 碳的化學性質活潑 | B. | X表示N2 | ||
| C. | 氧原子的質子數是8 | D. | 三種元素原子的核外電子數相同 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
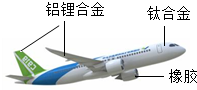 2015年11月,我國首架大型客機C919(如圖)正式下線,實現了我國航空領域的新突破.回答下列問題:
2015年11月,我國首架大型客機C919(如圖)正式下線,實現了我國航空領域的新突破.回答下列問題:查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 鎂條在空氣中劇烈燃燒,發出耀眼白光,生成黑色固體 | |
| B. | 鐵銹在稀鹽酸里浸泡一段時間后,鐵銹消失,溶液變為淺綠色 | |
| C. | 向淀粉溶液中滴加碘水,溶液變為藍色 | |
| D. | 向硫酸銅溶液中滴加氫氧化鈉溶液,生成白色沉淀 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
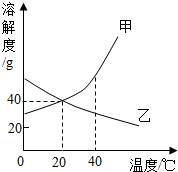 甲、乙兩種固體物質的溶解度曲線如圖所示,下列說法正確的是( )
甲、乙兩種固體物質的溶解度曲線如圖所示,下列說法正確的是( )| A. | 20℃時,甲物質的溶解度是40 | |
| B. | 升溫可使乙物質的飽和溶液析出固體 | |
| C. | 甲物質的溶解度大于乙物質的溶解度 | |
| D. | 40℃時,將甲、乙兩物質飽和溶液分別降溫到20℃,二者都變為不飽和溶液 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com