
分析 (1)考慮如果含有硫酸銅,銅離子在溶液中,溶液應為藍色;考慮碳酸根離子與酸反應生成氣體;
(2)考慮Ba(NO3)2+MgSO4=BaSO4↓+Mg(NO3)2,進行分析;
(3)根據生成的氯化銀沉淀的質量,結合反應的化學方程式可計算出原固體混合物中的氯化鈉的質量和硝酸銀溶液中的硝酸銀的質量,進而計算出原混合物中硫酸鎂、氯化鈉的質量即可.
解答 解:
有一白色粉末,其中只可能含有硫酸鎂、碳酸鈉、硫酸銅、氯化鈉、氯化鎂中的一種或幾種.根據以下實驗回答:(1)取樣,加水溶解得無色溶液A,向A中加入足量稀硝酸,無現象,得無色溶液B.因為如果含有硫酸銅,銅離子在溶液中,溶液應為藍色;而碳酸根離子與酸反應生成氣體,則該粉末中一定沒有硫酸銅、碳酸鈉.
(2)根據(1)推測,溶液B中成分可能為稀硝酸、硫酸鎂、氯化鈉、氯化鎂,其中加入足量硝酸鋇溶液,得到23.3g白色沉淀和無色溶液C,根據Ba(NO3)2+MgSO4=BaSO4↓+Mg(NO3)2,則原白色粉末中含有硫酸鎂.
(3)根據(2)推測,無色溶液C可能為稀硝酸、Mg(NO3)2、氯化鈉、氯化鎂,為確定是否含有另外兩種物質“氯化鈉、氯化鎂”,將C溶液平均分成兩份,向一份中加入足量的硝酸銀得到14.35g白色沉淀,則可知一定有氯離子;
根據Ba(NO3)2+MgSO4=BaSO4↓+Mg(NO3)2,
233 148,因為23.3g白色沉淀BaSO4,則可知Mg(NO3)2的質量為14.8g,
根據2NaOH+Mg(NO3)2=2NaNO3+Mg(OH)2↓,
148 58,因為14.8gMg(NO3)2,則可知生成沉淀Mg(OH)2的質量為5.8g,故可知:則原白色粉末中還一定含有氯化鈉,一定沒有氯化鎂.
故答案為:
(1)硫酸銅、碳酸鈉;(2)硫酸鎂(3)氯化鈉,氯化鎂.
點評 本考點屬于物質的鑒別題,是通過對實驗方法和過程的探究,在比較鑒別的基礎上,得出了正確的實驗結論.本考點是中考的重要內容之一,主要出現在填空題和實驗題中.


科目:初中化學 來源: 題型:解答題
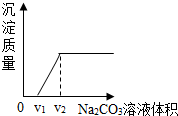 某學習小組探究氫氧化鈣溶液的化學性質,并作了延伸探究.
某學習小組探究氫氧化鈣溶液的化學性質,并作了延伸探究.| 方案 | (1) | (2) | (3) |
| 實驗操作 | 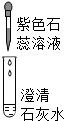 | 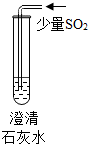 |  |
| 現象 | 溶液變為藍色 | 澄清石灰水變渾濁 | 紅色褪為無色 |
| 結論或解釋 | 氫氧化鈣溶液能使石蕊等酸堿指示劑變色 | 氫氧化鈣溶液能與某些非金屬氧化物反應生成鹽和水.二氧化硫與澄清石灰水反應的化學方程式是 SO2+Ca(OH)2═CaSO3↓+H2O | 氫氧化鈣溶液能與酸發生中和反應 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
 在實驗室里用濃度為98%的濃硫酸和蒸餾水配制稀硫酸.
在實驗室里用濃度為98%的濃硫酸和蒸餾水配制稀硫酸.查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 銅片插入稀硫酸:Cu+H2SO4═CuSO4+H2↑ | |
| B. | 工業煉鐵:FexOy+yCO$\frac{\underline{\;高溫\;}}{\;}$xFe+yCO2 | |
| C. | 氫氧化鈉溶液吸收二氧化硫:2NaOH+SO2═Na2SO4+H2O | |
| D. | 二氧化碳通入氯化鈣溶液:CO2+CaCl2+H2O═CaCO3↓+2HCl |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
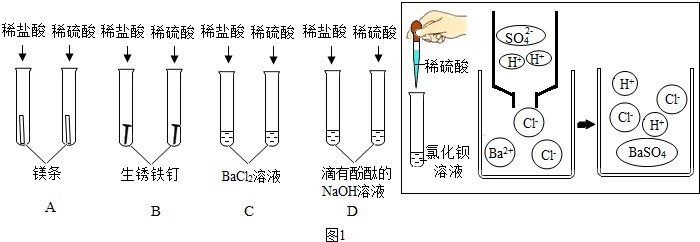
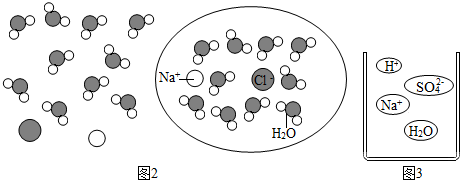
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
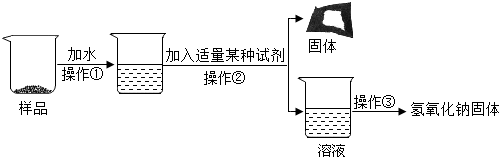
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com