
分析 方法一,因為反應后減少的是二氧化碳,鈣元素全部轉化為CaO中的鈣,則只要計算出所有CaO中的鈣元素即可求出;
方法二,利用生成的二氧化碳(120-84=36g)來計算參加反應的碳酸鈣質量,同時也計算出混合物中氧化鈣的質量,再分別計算這兩種物質中含有鈣元素的質量就能求出.
解答 解:(法一)
84gCaO含鈣元素的質量=84g×$\frac{40}{56}$×100%=60g,反應前混合物中鈣元素的質量也為60g,
則原固體混合物中鈣元素的質量分數=$\frac{60g}{120g}$×100%=50%
答:原固體混合物中鈣元素的質量分數為50%.
(法二)
生成的二氧化碳的質量=120g-84g=36g
設原混合物中碳酸鈣的質量為x
CaCO3$\frac{\underline{\;高溫\;}}{\;}$CaO+CO2↑
100 44
x 36g
100:44=x:36g 解之得 x≈81.8g
則原混合物中氧化鈣的質量=120g-81.8g=38.2g
原混合物中鈣元素的質量=81.8g×$\frac{40}{100}$×100%+38.2g×$\frac{40}{56}$×100%=60g
則原固體混合物中鈣元素的質量分數=$\frac{60g}{120g}$×100%=50%
答:原固體混合物中鈣元素的質量分數為50%.
點評 兩種解法中,解法一很簡單且數據較容易處理;解法二的過程較多,數據處理時稍不注意就會出現較大的誤差.


科目:初中化學 來源: 題型:填空題
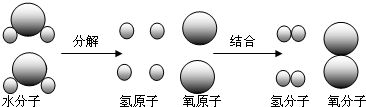
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 氮氣 性質穩定 保護氣 | B. | 酒精 可燃性 消毒劑 | ||
| C. | 食醋 酸性 除水垢 | D. | 干冰 升華吸熱 人工降雨 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
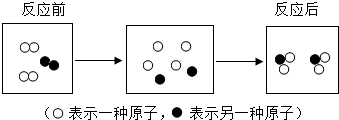
| A. | 分子由原子構成 | B. | 分子間存在一定的空隙 | ||
| C. | 化學反應中分子可分為原子 | D. | 反應前后分子變大了 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:填空題

查看答案和解析>>
科目:初中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com