
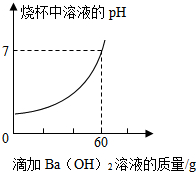
 某品牌潔廁靈的成分是硫酸與鹽酸的混合溶液.某同學想測定該潔廁靈中HCl的質量分數.取20g該品牌的潔廁靈溶液于燒杯中,不斷滴加氫氧化鋇溶液,反應過程燒杯中產生沉淀質量和燒杯中溶液pH變化的部分數據如圖表所示:(已知BaCl2溶液的pH=7)
某品牌潔廁靈的成分是硫酸與鹽酸的混合溶液.某同學想測定該潔廁靈中HCl的質量分數.取20g該品牌的潔廁靈溶液于燒杯中,不斷滴加氫氧化鋇溶液,反應過程燒杯中產生沉淀質量和燒杯中溶液pH變化的部分數據如圖表所示:(已知BaCl2溶液的pH=7)| 滴加氫氧化鋇溶液的質量/g | 5 | 10 | 25 | 30 |
| 燒杯中產生沉淀的質量/g | 1.165 | 2.33 | 4.66 | 4.66 |
分析 氫氧化鋇和稀硫酸反應生成白色沉淀硫酸鋇和水,和稀鹽酸反應生成氯化鋇和水,根據反應的化學方程式和提供的數據、信息等可以進行相關方面的判斷和計算.
解答 解:(1)由圖象可知,當潔廁靈中的硫酸恰好反應完時,溶液的pH=7,消耗氫氧化鋇溶液的質量為 60g;
(2)當氫氧化鋇溶液滴加到10g時,產生2.33g沉淀,產生4.66g沉淀時消耗20g氫氧化鋇溶液,當氫氧化鋇溶液的質量再增加時生成沉淀的質量不再增加,說明了當氫氧化鋇溶液滴加到20g時,硫酸反應完全,與鹽酸反應的氫氧化鋇的溶液的質量是60g-20g=40g.
設20g氫氧化鋇溶液中溶質的質量為x,
Ba(OH)2+H2SO4═BaSO4↓+2H2O,
171 233
x 4.66g
$\frac{171}{233}=\frac{x}{4.66g}$ 解得:x=3.42g
氫氧化鋇溶液中溶質的質量分數為:$\frac{3.42g}{20g}×100%$=17.1%
(3)設該潔廁靈溶液中HCl的質量為y
Ba(OH)2+2HCl═BaCl2+2H2O
171 73
40g×17.1% y
$\frac{171}{73}=\frac{40g×17.1%}{y}$ 解得:y=2.92g
該潔廁靈溶液中HCl的質量分數為:$\frac{2.92g}{20g}×100%$=14.6%
故答為:(1)60;(2)氫氧化鋇溶液中溶質的質量分數為17.1%;(3)計算:該潔廁靈溶液中HCl的質量分數為14.6%
點評 本題難度不大,掌握根據化學方程式的計算即可正確解答本題,細致地分析圖表信息,根據找出生成硫酸鋇沉淀的質量是正確解答本題的前提和關鍵.


科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
| 營養成分 | 水分 | 蛋白質 | 脂肪 | 糖類 | X | 鈣、磷、鐵、鋅 |
| 質量 | 92.5g | 0.7g | 0.2g | 6.1g | 6.8mg | 17.1mg |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題

查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
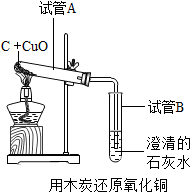 對于化學反應,我們不但要考慮加入的試劑,還要考慮環境中的其他物質對化學反應的影響.教材中“木炭還原氧化銅”的實驗(見圖).
對于化學反應,我們不但要考慮加入的試劑,還要考慮環境中的其他物質對化學反應的影響.教材中“木炭還原氧化銅”的實驗(見圖).查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 中和反應生成鹽和水,所以生成鹽和水的反應一定是中和反應 | |
| B. | 堿能跟某些非金屬氧化物反應,所以堿溶液能吸收一氧化碳氣體 | |
| C. | 酸能使紫色石蕊溶液變紅,通入二氧化碳后的紫色石蕊溶液變紅,所以二氧化碳是酸 | |
| D. | 堿性物質的溶液能使無色酚酞溶液變紅,所以能使無色酚酞溶液變紅的物質一定顯堿性 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com