
溶液在生產、生活中起著十分重要的作用。
(1)可作為溶質的是_______。
A.只有固體 B. 只有液體
C.只有氣體 D. 氣體、液體、固體都可以
(2)物質加入足量水中,能形成無色透明溶液的是_______。
A.汽油 B. 面粉 C. 純堿 D. 硫酸銅
(3)物質加入水中形成溶液過程中,溫度會升高的是_______。
A.燒堿 B. 氯化鈉 D. 氧化鈣 D. 碳酸鈣
(4)下表是NaCl和KNO3在不同溫度時的溶解度,回答問題。
溫度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度g/100g水 | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 |
①兩種物質中,溶解度受溫度影響變化較大的是__________。
②NaCl和KNO3溶解度相等的溫度范圍是__________。
③KNO3晶體中含有少量NaCl,提純KNO3晶體的方法是__________。
④60℃時,按圖示操作:
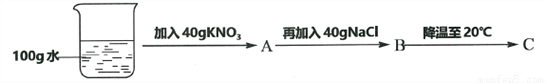
A中溶液是__________(填“飽和”或“不飽和”)溶液,C中溶液的總質量是__________g。
⑤50℃時,將兩種物質的飽和溶液各100g,分別加熱蒸發10g水后,再恢復到50℃,剩余溶液的質量:NaCl溶液__________(填“大于”“等于”或“小于”)KNO3溶液。
D C AC KNO3 20℃ 每日10分鐘口算心算速算天天練系列答案
每日10分鐘口算心算速算天天練系列答案科目:初中化學 來源:四川省2018年初中畢業生學業綜合測試化學試卷 題型:單選題
“碳捕捉技術”是指通過一定的方法,將工業生產中產生的CO2分離出來進行儲存和利用。常利用NaOH溶液來“捕捉”CO2,過程如下圖所示(部分條件及物質未標出)。下列說法正確的是 ( )

A. 該方法的優點是沒有能耗
B. “反應、分離”中,分離物質的基本操作是蒸發、結晶
C. 整個過程中,只有一種物質可以循環利用
D. 該方法可減少碳排放
D 【解析】A、該反應在高溫爐中進行,是高耗能反應,故錯誤; B、“反應、分離”中,分離物質發生的是化學變化,故錯誤; C、反應中氧化該和氫氧化鈉都可以循環利用,故錯誤; D、該方法可以減少二氧化碳的排放量,故正確。故選D。查看答案和解析>>
科目:初中化學 來源:山東省2018年中考化學一輪復習綜合測試卷 題型:實驗題
某小組在學習“二氧化碳與氫氧化鈉溶液反應”時,進行了如下探究,
【提出問題】二氧化碳與氫氧化鈉反應,還是溶解在水中?
【查閱資料】
 、101KPa時,二氧化碳的溶解度如下:
、101KPa時,二氧化碳的溶解度如下:
溶劑 | 水 | 酒精 |
溶解度 |
|
|
 時,在酒精中氫氧化鈉易溶、碳酸鈉微溶.
時,在酒精中氫氧化鈉易溶、碳酸鈉微溶.
 通常情況下,稀溶液的體積約等于溶劑的體積.
通常情況下,稀溶液的體積約等于溶劑的體積.
【實驗設計】在 、101KPa時,制取二氧化碳并用于實驗甲、實驗乙.
、101KPa時,制取二氧化碳并用于實驗甲、實驗乙.

【分析與表達】
 如果二氧化碳與氫氧化鈉反應,化學方程式是______ ,那么氫氧化鈉應______ 保存.
如果二氧化碳與氫氧化鈉反應,化學方程式是______ ,那么氫氧化鈉應______ 保存.
 實驗前,兩套裝置都進行氣密性檢查,實驗甲裝置氣密性檢查的方法是______
實驗前,兩套裝置都進行氣密性檢查,實驗甲裝置氣密性檢查的方法是______
 實驗甲中,同時滴入等體積的水和氫氧化鈉溶液后的現象是______
實驗甲中,同時滴入等體積的水和氫氧化鈉溶液后的現象是______
 實驗乙中,將氫氧化鈉完全滴入錐形瓶中,注射器會自動向內移動并將酒精推入錐形瓶,活塞的移動速度是______
實驗乙中,將氫氧化鈉完全滴入錐形瓶中,注射器會自動向內移動并將酒精推入錐形瓶,活塞的移動速度是______  填答案字母
填答案字母
A.先慢后快  先快后慢
先快后慢  先慢后快,再變慢
先慢后快,再變慢
實驗乙中,還可能觀察到的現象是______ .
 實驗乙中,120mL酒精______
實驗乙中,120mL酒精______  填“能”或“不能”
填“能”或“不能” 換成水,原因是______ .
換成水,原因是______ .
 實驗乙結束時,注射器中酒精燈體積為20mL,則與氫氧化鈉反應的二氧化碳體積至少是______ mL.
實驗乙結束時,注射器中酒精燈體積為20mL,則與氫氧化鈉反應的二氧化碳體積至少是______ mL.
 由以上探究可知,二氧化碳能溶于水,也能氫氧化鈉反應,但實驗乙的數據還不夠準確,造成實驗乙誤差的原因可能有______
由以上探究可知,二氧化碳能溶于水,也能氫氧化鈉反應,但實驗乙的數據還不夠準確,造成實驗乙誤差的原因可能有______  寫一條
寫一條
查看答案和解析>>
科目:初中化學 來源:山東省2018年中考化學一輪復習綜合測試卷 題型:單選題
下圖是甲、乙、丙三種物質的溶解度曲線,下列說法中正確的是( )

A. t1℃時,甲物質的飽和溶液中溶質和溶劑的質量比為1:4
B. P點表示甲、丙兩種物質的飽和溶液質量相等
C. t1℃時,乙物質的飽和溶液,升溫至t2℃時仍是飽和溶液
D. 將三種物質的溶液從t2℃降至t1℃,析出晶體最多的是甲物質
A 【解析】試題分析:A、t1℃時,甲物質的溶解度是25g,所以甲物質的飽和溶液中溶質和溶劑的質量比為25g:100g=1:4,故A正確;B、P點表示甲、丙兩種物質的飽和溶液質量的質量分數相等,故B錯誤;C、乙物質的溶解度隨溫度的升高而增大,所以t1℃時,乙物質的飽和溶液,升溫至t2℃時不是飽和溶液,故C錯誤;D、三種物質飽和溶液的質量不能確定,所以將三種物質的溶液從t2℃降至t1℃,析出晶...查看答案和解析>>
科目:初中化學 來源:上海市楊浦區2018屆初三二模化學試卷 題型:科學探究題
某興趣小組同學稱取10g氧化銅和碳粉,通過下列實驗對其中炭粉含量進行探究。實驗前進行知識準備:2Cu + O2  2CuO
2CuO

(1)關閉彈簧夾,打開分液漏斗活塞。寫出A中的化學反應方程式________________________________。
(2)點燃酒精燈,將尖嘴管對著火焰,以提高溫度,其原因是________________________________。玻璃管中發生的反應為 木炭還原氧化銅:C+ 2CuO → 2Cu + CO2↑,該反應條件是__________。
(3)反應一段時間,裝置B中一定會觀察到_____________________。裝置D中澄清石灰水不變渾濁,說明__________________________________________。
(4)再打開彈簧夾,繼續加熱裝置B,裝置C中觀察到的現象是____________________。
直至固體顏色不再變化后停止加熱,稱量裝置C,質量比反應前增重4.4g,增重質量就是____________質量。通過計算可知裝置B中含碳元素質量為____________g。本實驗還可以通過稱量____________________,也能計算出原混合物中碳的質量分數。
2H2O2O2↑+ 2H2O 氧氣具有助燃性(或氧氣使酒精燃燒更充分) 高溫 黑色固體變成紅色 CO2被NaOH完全吸收 有氣泡冒出 生成的CO2 1.2 B中玻璃管及其中固體在反應前后的總質量 【解析】(1)過氧化氫在二氧化錳作催化劑的條件下反應生成水和氧氣,反應方程式為2H2O2O2↑+ 2H2O (2)尖嘴管中放出的是氧氣,氧氣具有助燃性(或氧氣使酒精燃燒更充分),提供更高的溫度...查看答案和解析>>
科目:初中化學 來源:上海市楊浦區2018屆初三二模化學試卷 題型:單選題
下列各組溶液,不外加試劑就能鑒別出來的是
A. NaOH、Ba(NO3)2、NaCl、MgSO4 B. NaOH、FeCl3、HCl、HNO3
C. Na2CO3、NaCl、Na2SO4、Ba(OH)2 D. Na2CO3、HCl、BaCl2、NaCl
D 【解析】A、組內四種物質兩兩混合,硫酸鎂與氫氧化鈉和硝酸鋇溶液反應均能產生白色沉淀,但是其余兩種物質混合均為明顯現象,故不加其他試劑無法鑒別,錯誤; B、FeCl3是黃色溶液,首先可以鑒別,氯化鐵與氫氧化鈉反應由紅色沉淀生成,可以確定氫氧化鈉,稀鹽酸和硝酸無法鑒別,錯誤; C、氫氧化鋇可以與碳酸鈉和硫酸鈉反應生成表示沉淀,可以確定氫氧化鋇,碳酸鈉和硫酸鈉、氯化鈉無法鑒別,錯誤...查看答案和解析>>
科目:初中化學 來源:上海市楊浦區2018屆初三二模化學試卷 題型:單選題
可燃冰主要含甲烷水合物,用作燃料時反應的微觀示意圖如圖,下列說法正確的是

A. 可燃冰中只有甲烷
B. 反應前后分子總數不變
C. 反應的化學方程式為CH4 + O2  CO2 + H2O
CO2 + H2O
D. 反應前后的物質均由原子構成
B 【解析】A、可燃冰主要含甲烷水合物,是混合物,錯誤; B、由微觀示意圖可知,反應前后分子的個數不變,正確; C、該反應沒有配平,錯誤; D、反應前后的物質由分子構成,錯誤。故選B。查看答案和解析>>
科目:初中化學 來源:湖北省恩施州利川市蘇馬蕩教育集團2018屆九年級中考模擬(一)化學試卷 題型:簡答題
A、B、C三種物質的溶解度曲線如圖所示,請回答下列問題:

(1)N點對應的是物質A在t2℃的__________(“飽和”或“不飽和”)溶液。
(2)加熱C的飽和溶液,出現渾濁現象,其原因是___________。
(3)除去A中少量的B,步驟是:加水溶解,蒸發濃縮,__________,過濾,洗滌,干燥。
(4)t1℃時,將A、B、C各8 g分別加入盛有50g水的燒杯中, 充分溶解,測得三種溶液中溶質的質量分數分別為w(A) 、w(B) 、w(C),則三者之間的大小關系是______。
不飽和 C的溶解度隨溫度的升高而減小 降溫結晶(冷卻結晶) w(A)= w(B)>w(C) 【解析】本題考查了固體的溶解度曲線所表示的意義,及根據固體的溶解度曲線來解決相關的問題。(1)N點在A物質的溶解度曲線的下方,所以N點對應的是物質A在t2℃的不飽和溶液; (2)C物質的溶解度隨溫度的升高而減小,所以加熱C的飽和溶液,出現渾濁現象; (3)A物質的溶解度受溫度變化影響較大,...查看答案和解析>>
科目:初中化學 來源:山東省德州市德城區2018屆九年級第一次練兵考試化學試卷 題型:簡答題
水是生命之源,請回答有關水的下列問題:
(1)電解水實驗如圖所示。①中所得氣體是______,①與②中所得氣體的體積比約為______。該反應的微觀示意圖如下,請在方框內補全相應微粒的示意圖。

 _________________
_________________
(2)“生命吸管”是一種便攜式戶外凈水器。其凈水原理如下圖:

①通過濾網可去除______(填“可溶性”或“難溶性”)雜質。
②抗菌活性復合濾料中有活性炭、離子交換樹脂等。活性炭的主要作用是______。
③離子交換樹脂能去除原水中的鈣離子,鈣離子的符號是______。
O2 1∶2 難溶性 吸附 Ca2+ 【解析】本題考查了水的電解實驗和水的凈化。 (1)①中所得氣體是電源的正極產生的氣體是氧氣(O2),②中所得氣體為氫氣,①與②中所得氣體的體積比約為 1:2; ②由質量守恒定律反應前后原子的中種類及數目不變可知,在方框內補全相應一個氧分子,如右圖; ②①過濾可以把不溶于水的物質除去,通過濾網可去除難溶性雜質; ②活性炭具有吸附作用...查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com