
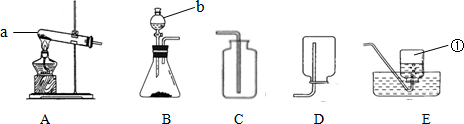
分析 (1)根據實驗室常用儀器解答;
(2)如果用高錳酸鉀或氯酸鉀制氧氣就需要加熱.氧氣的密度比空氣的密度大,不易溶于水,因此能用向上排空氣法和排水法收集,向上排空氣法收集的氣體比較干燥,排水法收集的氣體比較純凈;氧氣的驗滿方法是:將帶火星的木條平放在集氣瓶口,木條復燃,證明氧氣滿了.
(3)如果用雙氧水和二氧化錳制氧氣就不需要加熱;
(4)根據實驗室制取CO2,是在常溫下,用碳酸鈣和鹽酸互相交換成分生成氯化鈣和水和二氧化碳,因此不需要加熱.二氧化碳能溶于水,密度比空氣的密度大,因此只能用向上排空氣法收集.若裝置B中反應劇烈,從實驗安全角度考慮,從實驗安全角度考慮,不宜采取的措施有:用容積較小的錐形瓶;加熱反應物等.
解答 解:
(1)根據實驗室常用儀器可知:b分液漏斗;
(2)如果用高錳酸鉀制氧氣就需要加熱,高錳酸鉀受熱分解生成錳酸鉀和二氧化錳和氧氣,要注意配平,反應的化學方程式為:2KMnO4 $\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;氧氣的密度比空氣的密度大,不易溶于水,因此能用向上排空氣法和排水法收集,向上排空氣法收集的氣體比較干燥,排水法收集的氣體比較純凈;氧氣的驗滿方法是:將帶火星的木條平放在集氣瓶口,木條復燃,證明氧氣滿了;故答案為:2KMnO4 $\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;A; D;集氣瓶口; E
(3)如果用雙氧水和二氧化錳制氧氣就不需要加熱,注射器可以控制反應的速度,故答案為:B;
(4)實驗室制取CO2,是在常溫下,用碳酸鈣和鹽酸互相交換成分生成氯化鈣和水和二氧化碳,反應的化學方程式為:CaCO3+2HCl=CaCl2+H2O+CO2↑;因此不需要加熱;若裝置B中反應劇烈,從實驗安全角度考慮,從實驗安全角度考慮,不宜采取的措施有:用容積較小的錐形瓶;加熱反應物等;
答案:
(1)分液漏斗;
(2)2KMnO4 $\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;A; C;集氣瓶口; E;
(3)B;
(4)CaCO3+2HCl=CaCl2+H2O+CO2↑;①③.
點評 本題為常用氣體的原理、裝置、檢驗及驗滿方法的考查,應熟練掌握典型氣體的實驗室制取原理、反應的化學方程式書寫及檢驗驗方法.


科目:初中化學 來源: 題型:實驗探究題


查看答案和解析>>
科目:初中化學 來源: 題型:解答題
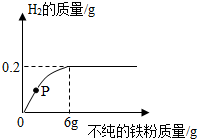 向一定量的稀鹽酸中逐漸加入某種不純的鐵粉,加入鐵粉的量與生成H2的關系如圖所示,請回答有關問題:
向一定量的稀鹽酸中逐漸加入某種不純的鐵粉,加入鐵粉的量與生成H2的關系如圖所示,請回答有關問題:查看答案和解析>>
科目:初中化學 來源: 題型:推斷題
 如圖表示某些物質間轉化關系.A、B為組成元素相同的無色液體,D是大理石的主要成分,C、F、H為氣體,且H有刺激性氣味.
如圖表示某些物質間轉化關系.A、B為組成元素相同的無色液體,D是大理石的主要成分,C、F、H為氣體,且H有刺激性氣味.查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
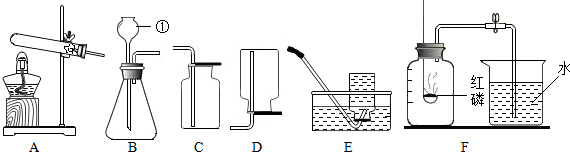
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | NaCl(Na2CO3) | B. | C(CaCO3) | C. | KNO3(KCl) | D. | Cu(Fe) |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | ②③ | B. | ③⑤ | C. | ②⑤ | D. | ①④ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com