3.化學興趣小組根據老師提供的實驗裝置(如圖1)進行如下實驗探究.
(試劑足量,反應均完全,裝置可重復使用,部分夾持裝置已省略,裝置氣密性良好.)
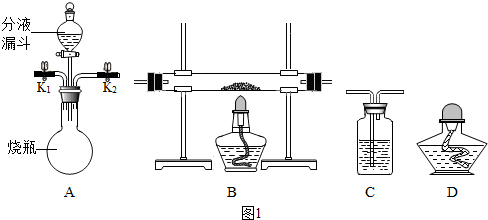
(1)甲組同學利用A裝置中產生的氧氣驗證B中的黑色粉末是炭粉.
①A裝置中反應的化學方程式為2H
2O
2$\frac{\underline{\;MnO_2\;}}{\;}$2H
2O+O
2↑.
②為完成此實驗,除用A、B裝置外,還需要補充C、D裝置,C瓶中試劑為石灰水主要作用是證明有二氧化碳生成,反應化學方程式為Ca(OH)
2+CO
2═CaCO
3↓+H
2O;
D裝置的主要作用是提供熱量.
(2)乙組同學要驗證A中燒瓶內裝的氣體可能是CO、CO
2、CH
4中的一種或幾種,為確定燒瓶內氣體的成分,乙組同學進行如下實驗(忽略B、C裝置中空氣的影響):
【資料】甲烷和氧化銅反應的化學方程式為:CH
4+4CuO$\frac{\underline{\;\;△\;\;}}{\;}$4Cu+CO
2+2H
2O
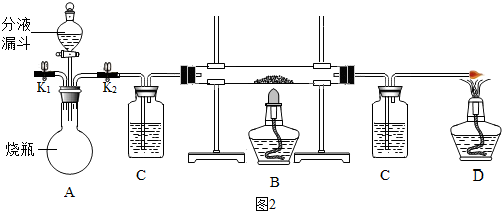
【操作步驟】
Ⅰ.按A→C→B→C→D的順序連接裝置如圖2,實驗時打開K
2與分液漏斗,將3.0g的濃氫氧化鈉溶液滴入燒瓶中;加熱B中足量的氧化銅固體,點燃D中酒精燈.
Ⅱ.打開K
1,通入氮氣;待B中固體顏色不再發生改變,停止加熱,繼續通氮氣.
Ⅲ.反應結束后,測得燒瓶中溶液的質量為3.1g,B中固體的質量減少了0.32g,
第二個C裝置的質量增加了0.18g.
①在Ⅱ中打開K
1,通入氮氣目的是排出燒瓶中的氣體;停止加熱,繼續通氮氣目的是防止C中的液體倒吸入玻璃管中.
②兩個C裝置中試劑相同均為濃硫酸,則參加反應的氧化銅質量是1.6g.
③燒瓶中氣體的成分為二氧化碳和甲烷.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案
