
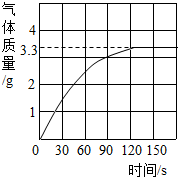
 長期使用的熱水壺底部有一層水垢,水垢的主要成分是碳酸鈣和氫氧化鎂.他們為了測定水垢中碳酸鈣的含量,將足量質量分數為10%的鹽酸加入到10.0g水垢后,產生CO2氣體的情況如圖所示.
長期使用的熱水壺底部有一層水垢,水垢的主要成分是碳酸鈣和氫氧化鎂.他們為了測定水垢中碳酸鈣的含量,將足量質量分數為10%的鹽酸加入到10.0g水垢后,產生CO2氣體的情況如圖所示.分析 (1)碳酸鈣與稀鹽酸反應生成氯化鈣、水和二氧化碳,氫氧化鎂與稀鹽酸反應生成氯化鎂和水;由產生CO2氣體的情況圖,最終測試3.3g二氧化碳氣體,由反應的化學方程式列式計算出參加反應的碳酸鈣的質量、參加反應的稀鹽酸中溶質的質量,進而計算出水垢中碳酸鈣的質量分數.
(2)由水垢中氫氧化鎂的質量,由反應的化學方程式列式計算出參加反應的稀鹽酸中溶質的質量,進而計算出所需稀鹽酸的質量.
(3)根據溶液稀釋前后溶質的質量不變,結合題意進行分析解答.
解答 解:(1)設參加反應的碳酸鈣的質量為x,與碳酸鈣反應消耗的稀鹽酸中溶質的質量為y
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
x y 3.3g
$\frac{100}{44}=\frac{x}{3.3g}$ x=7.5g
$\frac{73}{44}=\frac{y}{3.3g}$ y=5.475g
水垢中碳酸鈣的質量分數是$\frac{7.5g}{10g}$×100%=75%.
(2)水垢中氫氧化鎂的質量為10g-7.5g=2.5g.
設氫氧化鎂完全反應消耗HCl的質量為z
2HCl+Mg(OH)2═MgCl2+2H2O
73 58
z 2.5g
$\frac{73}{58}=\frac{z}{2.5g}$ z≈3.147g
至少需要質量分數為10%的鹽酸的質量為(5.475g+3.147g)÷10%≈86.2g.
(3)設需用38%的濃鹽酸(密度為1.19g/cm3)的體積是x
1.19g/cm3×x×38%=113.0g×10.0% x≈25cm3(25mL)
答:(1)水垢中碳酸鈣的質量分數是75%;(2)至少需要質量分數為10%的鹽酸的質量為86.2g;(3)需用38%的濃鹽酸(密度為1.19g/cm3)的體積是25mL.
點評 本題難度不大,掌握利用化學方程式與溶質質量分數的綜合計算即可正確解答本題,解題時要注意解題的規范性.


科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
 有A,B兩種金屬放入等質量分數的稀硫酸中,生成氫氣的質量與反應時間的關系如圖所示,下列結論合理的是( )
有A,B兩種金屬放入等質量分數的稀硫酸中,生成氫氣的質量與反應時間的關系如圖所示,下列結論合理的是( )| A. | 金屬活動性A>B | B. | 生成氫氣的質量A>B | ||
| C. | 反應的硫酸質量A<B | D. | 反應的金屬質量A<B |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | ①②④ | B. | ②④⑥ | C. | ①③⑤ | D. | ③⑤⑥ |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 配制溶液時,只能用水作溶劑 | |
| B. | 配制硝酸銨溶液的過程中,溶液的溫度會下降 | |
| C. | 用濃硫酸配制稀硫酸時,應將水緩緩注入濃硫酸中 | |
| D. | 將10g氯化鈉溶于100g水中,得到質量分數為10%的氯化鈉溶液 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 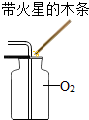 收集氧氣時,氧氣的驗滿 | B. | 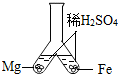 比較鎂與鐵的金屬活動性 | ||
| C. | 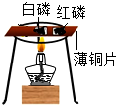 驗證白磷的著火點低于紅磷 | D. | 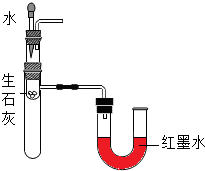 驗證生石灰與水反應放熱 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 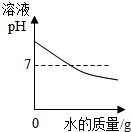 向氫氧化鈉溶液中加水 | |
| B. |  向一定質量的稀鹽酸中持續加入碳酸鈉溶液 | |
| C. |  向氯化鈉飽和溶液中加入氯化鈉固體 | |
| D. | 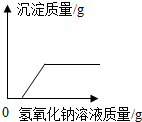 向硫酸銅溶液中加入氫氧化鈉溶液 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com