

| 編號 | 鹽酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | x |
| 3 | 7.30% | 8.00% | 14 |
分析 方案一:(1)根據用pH試紙測定溶液的pH的方法進行分析;
(2)根據用鹽酸滴定氫氧化鈉溶液時,如果鹽酸過量,則使溶液的pH小于7進行分析;
方案二:(1)根據氧氣不易溶于水,所以空氣中的氧氣有一少部分會溶于水,加熱可把水中的氧氣除去;植物油浮在水面上,能防止氧氣進入溶液進行分析;
(2)根據碳酸鈉溶液顯堿性進行分析;
(3)根據用稀釋濃氫氧化鈉溶液的方法檢驗濃氫氧化鈉能使變紅的酚酞試液的紅色消失進行分析;
方案三:(1)根據表中的數據第一組與第三組的數據進行分析判斷解答即可;
(2)根據中和反應是放熱反應使燒瓶中的氣體膨脹,壓強變大的角度進行分析;
(3)①根據膠頭滴管的用途進行分析;
②根據玻璃棒的作用進行分析;
③根據碳酸鈉與鹽酸反應的現象進行分析;
④根據氫氧化鈉與二氧化碳的反應情況進行分析;
(4)根據該題中所發生的化學反應,可以知道是碳酸鈉和鹽酸的反應,然后依據二氧化碳氣體的質量來求出碳酸鈉的質量,然后判斷是否有氫氧化鈉進而解答該題.
解答 解:方案一:(1)用pH試紙測定溶液的pH時,正確的操作是:將pH試紙放在表面皿上,用玻璃棒蘸取少量待測液滴在試紙上,將試紙顏色與比色卡對照讀出pH值;
(2)向NaOH溶液中再滴加鹽酸,如果鹽酸過量,這時溶液呈酸性,溶液的pH小于7;
方案二:(1)由于水中溶有少量的氧氣,加熱是為了除去溶液中的氧氣,滴加植物油是為了防止空氣中的氧氣進入;
(2)碳酸鈉雖然是鹽,但它的水溶液顯堿性;
(3)可以采用向濃氫氧化鈉溶液中加水稀釋的方法來證明,所以①實驗方法:向氫氧化鈉溶液中滴幾滴酚酞試液,可觀察到溶液先變紅色,過一會紅色消失,再向溶液中加入水進行稀釋,觀察現象,②觀察到的現象:溶液又變成紅色;
方案三:(1)第三組中氫氧化鈉和鹽酸的濃度都是第一組的2倍,濃度疊加就是第一組的4倍,溫度的變化是第一組的4倍;第二組與第一組比較,鹽酸的質量分數不變,而氫氧化鈉的濃度是第一組的2倍,所以溫度的改變也是第一組的2倍,所以X的值是7;
(2)氫氧化鈉和鹽酸發生中和反應,溶液的溫度會升高,導致燒瓶內的壓強增大,使U形管的液面出現高度差,所以U形管中的液面左低右高;
(3)①在鹽酸和氫氧化鈉反應時,如果加入鹽酸的速度稍快可能會使加入的鹽酸過量,如使用膠頭滴管加入鹽酸,可以防止稀鹽酸過量;
②用玻璃棒攪拌能夠使鹽酸和氫氧化鈉充分反應;
③若出現氣泡則說明可能是氫氧化鈉變質,氫氧化鈉溶液中含有碳酸鈉;
④氫氧化鈉若變質則產生碳酸鈉,由于反應的情況不能確定,所以可以得出固體成分可能是碳酸鈉,碳酸鈉和氫氧化鈉等猜想;
(4)設固體樣品中碳酸鈉的質量為x,跟碳酸鈉反應的鹽酸的質量為y
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 44
x y×10% 2.2g
$\frac{106}{x}$=$\frac{73}{y×10%}$=$\frac{44}{2.2g}$
x=5.3g
y=36.5g
NaOH的質量為:13.3g-5.3g=8g
設和氫氧化鈉反應的鹽酸的質量為z
NaOH+HCl═NaCl+H2O
40 36.5
8g z×10%
$\frac{40}{8g}$=$\frac{36.5}{z×10%}$
z=73g
(3)在圖中畫出以縱坐標表示二氧化碳質量,橫坐標表示鹽酸的質量的關系圖: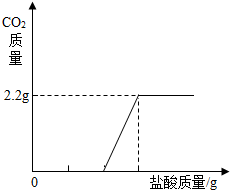 .
.
故答案為:方案一:(1)將pH試紙放在表面皿上,用玻璃棒蘸取少量待測液滴在試紙上,將試紙顏色與比色卡對照讀出pH值;
(2)鹽酸過量,溶液呈酸性,溶液的pH小于7;
方案二:(1)除去氧氣和隔絕氧氣;
(2)堿;
(3)取上述溶液加水稀釋后,再滴加無色酚酞;溶液呈紅色不消失;
方案三:(1)7;
(2)U型管中液面左低右高;
(3)①防止稀鹽酸過量;
②使反應充分;
③氫氧化鈉溶液中含有碳酸鈉;
④Na2CO3,NaOH與Na2CO3的混合物;
(4)(1)樣品中氫氧化鈉的質量為8g;
(2)和氫氧化鈉反應的鹽酸的質量為73g;
(3) .
.
點評 本題主要考查了酸堿中和反應以及酸堿性溶液與酸堿指示劑相互作用的情況,可以依據已有的知識進行,要求同學們加強對物質性質的識記,以便靈活應用.


 口算小狀元口算速算天天練系列答案
口算小狀元口算速算天天練系列答案 天天練口算系列答案
天天練口算系列答案科目:初中化學 來源: 題型:實驗探究題

查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 青蒿素是一種有機物 | |
| B. | 在一個青蒿素分子中,C、H、O三種元素的原子個數比是15:22:5 | |
| C. | 青蒿素不屬于氧化物 | |
| D. | 青蒿素分子中氧元素的化合價為-2價,則在生成該分子時,氧元素失去了兩個電子 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | Na2CO3 純堿 堿 | B. | CaO 生石灰 氧化物 | ||
| C. | O2 臭氧 單質 | D. | NaHCO3 蘇打 鹽 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com