
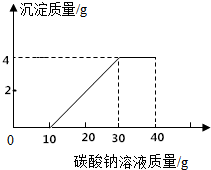
 實驗室制取二氧化碳后,對回收的鹽酸和氧化鈣混合溶液(不考慮其他雜質)進行了以下實驗:取100g該溶液于燒杯中,滴入40g溶質質量分數為21.2%的碳酸鈉溶液,充分反應后過濾,滴入碳酸鈉溶液質量與生成沉淀質量的關系如圖所示.求:
實驗室制取二氧化碳后,對回收的鹽酸和氧化鈣混合溶液(不考慮其他雜質)進行了以下實驗:取100g該溶液于燒杯中,滴入40g溶質質量分數為21.2%的碳酸鈉溶液,充分反應后過濾,滴入碳酸鈉溶液質量與生成沉淀質量的關系如圖所示.求:分析 (1)由圖示可知,開始滴入10g碳酸鈉溶液時沒有沉淀生成,說明是與鹽酸發生反應.故與鹽酸發生反應的碳酸鈉的質量為10g×21.2%=2.12g,然后根據化學方程式,得出各物質之間的質量比,列出比例式,就可計算出混合溶液中氯化氫的質量和生成氯化鈉的質量的質量.然后根據溶質質量分數公式就可計算出混合溶液中氯化氫的質量分數;
(2)由題意可知,將過濾所得的溶液蒸干,得到固體的質量即生成的NaCl的質量與未反應完的碳酸鈉的質量.根據圖示可知,與氯化鈣反應的碳酸鈉溶液的質量為20g,根據溶液的溶質質量分數計算出碳酸鈉的質量.然后根據化學方程式,得出各物質之間的質量比,列出比例式,就可計算出生成氯化鈉的質量.根據溶液的溶質質量分數就可計算出未反應完的碳酸鈉的質量.
解答 解:(1)根據圖示可知,與鹽酸反應的碳酸鈉的質量為:10g×21.2%=2.12g.
設100g混合溶液中氯化氫的質量為x,生成氯化鈉的質量為y,
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73 117
2.12g x y
∴$\frac{106}{2.12g}=\frac{73}{x}=\frac{117}{y}$
解之得:x=1.46g,y=2.34g,
混合溶液中氯化氫的質量分數為:$\frac{1.46g}{100g}$×100%=1.46%.
(2)根據圖示與氯化鈣反應的碳酸鈉的質量為:20g×21.2%=4.24g,
設生成氯化鈉的質量為z.
Na2CO3+CaCl2=2NaCl+CaCO3↓
106 117
4.24g z
∴$\frac{106}{4.24g}=\frac{117}{z}$
解之得:z=4.68g,
根據圖示未反應的碳酸鈉的質量為:10g×21.2%=2.12g.
實驗結束后,將過濾所得的溶液蒸干,得到固體的質量為:2.34g+4.68g+2.12g=9.14g.
答:實驗結束后,將過濾所得的溶液蒸干,得到固體的質量為9.14g.
點評 本題主要考查學生運用化學方程式和溶質質量分數公式進行計算的能力.


科目:初中化學 來源: 題型:選擇題
| A. | 水倒流 | B. | 溫度過高 | C. | 炸裂反應容器 | D. | 反應過慢 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 濾液M中可能存在Fe2+ | |
| B. | 濾液M中一定含有兩種金屬陽離子 | |
| C. | 濾渣N中一定沒有單質鎂 | |
| D. | 濾渣N的質量一定大于加入鐵粉的質量 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | CO2(CO):通過的灼熱的氧化銅 | B. | N2(O2):通過灼熱銅網 | ||
| C. | CaCl2(CaCO3):溶解、過濾、蒸發 | D. | H2(CO2):通過濃氫氧化鈉溶液 |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
 取24.8gCaCO3和Ca(OH)2固體混合物于燒杯中,向燒杯中不斷加入質量分數為7.3%的稀鹽酸.反應過程中測得生成氣體的質量與所加稀鹽酸質量的關系如圖所示.
取24.8gCaCO3和Ca(OH)2固體混合物于燒杯中,向燒杯中不斷加入質量分數為7.3%的稀鹽酸.反應過程中測得生成氣體的質量與所加稀鹽酸質量的關系如圖所示.查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
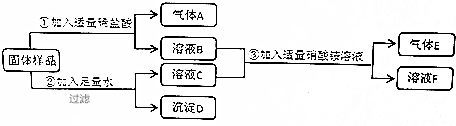
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 用水區分燒堿和硝酸銨兩種固體 | |
| B. | 用硝酸銀溶液區分氯化鈉和氯化鈣溶液 | |
| C. | 除去氧化銅中含有的銅粉:在空氣中加熱 | |
| D. | 除去二氧化碳中含有的水蒸氣,將氣體通過濃硫酸 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 氯酸鉀中氯元素的化合價:K$\stackrel{+3}{Cl}$O3 | |
| B. | 鎂離子的結構示意圖: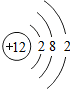 | |
| C. | 兩個乙醇分子:2C2H5OH | |
| D. | 工業上煉鐵的主要反應原理:3C+2Fe2O3$\frac{\underline{\;高溫\;}}{\;}$4Fe+3CO2↑ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com