
分析 (1)①根據貝殼的成分來分析;
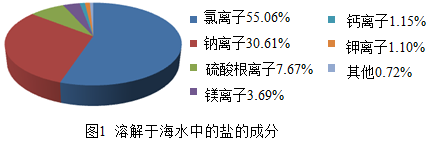
②根據提供的元素和物質的類別來確定物質的化學式;根據溶質的質量=溶液的質量×溶液中溶質的質量分數來分析;
③從入海的河水含鹽量較低的原因來分析;
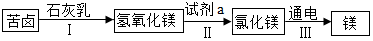
(2)加入過量的氯化鋇溶液可以除去硫酸鈉,加入過量的氫氧化鈉溶液可以除去氯化鎂,加入過量的碳酸鈉溶液可以除去氯化鈣和過量的氯化鋇;根據氯化鎂的生產流程,要將氫氧化鎂沉淀轉化為氯化鎂,應加入的試劑是稀鹽酸;海水中的氯化鎂能和氫氧化鈣反應生成氫氧化鎂沉淀,化學方程式為:MgCl2+Ca(OH)2=CaCl2+Mg(OH)2↓;
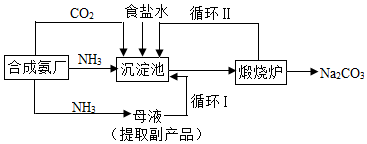
(3)根據NH3+H2O+CO2+NaCl═NH4Cl+NaHCO3↓及流程圖知,母液中溶質為氯化銨,向母液中通氨氣加入細小食鹽顆粒,冷卻析出副產品,循環Ⅰ中的氯化鈉有又返回到沉淀池.
解答 解:(1)①貝殼的主要成分是碳酸鈣;故填:CaCO3;
②鉀元素顯+1價,硫酸根顯-2價,故硫酸鉀的化學式為K2SO4;Wg海水中含有鉀離子的質量為:Wg×3.8%×1.10%,那么氯化鉀的質量為:$\frac{Wg×3.8%×1.10%×74.5}{39}$;故填:K2SO4;$\frac{Wg×3.8%×1.10%×74.5}{39}$;
③在河流的入海口處,有大量的河水注入海洋,相對于海水來講,注入海洋的河流屬于淡水.所以注入海洋的河水,等于是增加了入海口處海水中的水(溶劑),造成該處海水鹽的濃度降低;故填:河水中的淡水將海水中的鹽分稀釋;
(2)加入過量碳酸鈉溶液的目的是除去溶液中的鈣離子和鋇離子,故填:除去溶液中的鈣離子和鋇離子;
由氯化鎂的生產流程,要將氫氧化鎂沉淀轉化為氯化鎂,應加入的試劑a是稀鹽酸;海水中的氯化鎂能和氫氧化鈣反應生成氫氧化鎂沉淀,化學方程式為:MgCl2+Ca(OH)2=CaCl2+Mg(OH)2↓;故填:鹽酸;MgCl2+Ca(OH)2=CaCl2+Mg(OH)2↓;
(3)根據NH3+H2O+CO2+NaCl═NH4Cl+NaHCO3↓及流程圖知,母液中溶質為氯化銨,向母液中通氨氣加入細小食鹽顆粒,冷卻析出副產品,循環Ⅰ是將未反應的氯化鈉返回沉淀池中,煅燒碳酸氫鈉時生成二氧化碳、二氧化碳能循環利用,從固液混合物中分離出固體的方法為過濾.沉淀池中發生的反應是氨氣、水、二氧化碳和氯化鈉反應生成氯化銨和碳酸氫鈉;
故答案為:①侯德榜.②過濾;食品發酵粉等.③Ⅰ.④NH3+H2O+CO2+NaCl═NH4Cl+NaHCO3
點評 本題考查了實驗方案的設計,明確物質的性質是解本題關鍵,了解制備原理,知道常見陰陽離子的檢驗方法、物質分離的方法,難度中等.


科目:初中化學 來源: 題型:選擇題
| A. | 沒有規定用量時,液體取1-2ml | |
| B. | 酒精燈內的酒精不能超過酒精燈容積的四分之三 | |
| C. | 加熱液體時,液體體積不能超過試管容積的三分之一 | |
| D. | 量筒量取的液體體積通常應該稍小于或等于所要量取的量程 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題

| A. | 堿能使酚酞溶液變紅 | |
| B. | 氨分子是不斷運動的 | |
| C. | 空氣不能使酚酞溶液變紅 | |
| D. | 氨分子溶于水,形成的氨水使酚酞溶液變紅 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 木炭在空氣中燃燒,生成二氧化碳 | |
| B. | 硫在氧氣中燃燒,產生大量白煙 | |
| C. | 氫氣在空氣中燃燒,發出淡藍色火焰 | |
| D. | 紅磷在空氣中燃燒,產生大量白霧 |
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
 在某公共場所張貼有以下廣告請回答下列問題:
在某公共場所張貼有以下廣告請回答下列問題:查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 氟乙酸甲脂由4個元素組成 | |
| B. | 氟乙酸甲脂由3個碳原子、3個氫原子、1個氟原子和2個氧原子構成 | |
| C. | 氟乙酸甲脂中碳、氫、氟、氧元素的質量比為3:3:1:2 | |
| D. | 氟乙酸甲脂中碳元素的質量分數最大 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 500 mL容量瓶 | B. | 膠頭滴管 | C. | 試管 | D. | 托盤天平 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com