
分析 (1)鐵與硫酸反應生成氫氣,所以反應后燒杯中固體和液體的總質量減少的質量為氫氣的質量.
(2)由生成氣體的質量根據(jù)化學方程式可以計算出樣品中鐵的質量,進而計算出雜質的質量.
(3)由樣品質量和雜質質量可以計算出樣品中鐵的質量分數(shù),再結合生鐵的質量100t可以計算出生鐵中鐵元素的質量,由于化學反應中元素質量守恒,根據(jù)氧化鐵的化學式可以計算出氧化鐵的質量,最后再結合赤鐵礦中氧化鐵的質量分數(shù),就可以計算出赤鐵礦的質量.
解答 解:(1)反應后生成氫氣的質量為0.34g.
(2)設生鐵樣品中純鐵的質量為x.
Fe+H2SO4=FeSO4+H2↑
56 2
x 0.34g
$\frac{56}{x}=\frac{2}{0.34g}$,
x=9.52g
(3)設需要赤鐵礦的質量為y.
所得生鐵的含鐵質量分數(shù)為$\frac{9.52g}{10.0g}$×100%=95.2%
Fe2O3+3CO$\frac{\underline{\;高溫\;}}{\;}$2Fe+3CO2
160 112
y×80% 100t×95.2%
$\frac{160}{y×80%}=\frac{112}{100t×95.2%}$
解得y=170t
答:(1)反應后生成氫氣的質量為0.34g.
(2)樣品中純鐵的質量為9.52g,
(2)需要赤鐵礦170t.
點評 本題主要考查含雜質的物質的化學方程式計算,難度較大.


科目:初中化學 來源: 題型:選擇題
| A. | 好酒不怕巷子深一一分子是不斷運動的 | |
| B. | 熱脹冷縮一一分子間隔的大小隨溫度的改變而改變 | |
| C. | 電解水生成氫氣和氧氣一一分子可分成原子,原子重新組合成新分子 | |
| D. | 水可以分解為氫氣同種物質組成的混合物 |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題

查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | NH4Cl(含氮約26%) | B. | (NH4)2SO4(含氮約21%) | ||
| C. | NH4HCO3(含氮約17.7%) | D. | CO(NH2)2(含氮約46.7%) |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
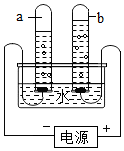 實驗是化學學習的一種重要手段,如利用電解水實驗可探究水的組成.請根據(jù)電解水實驗回答下列問題:通電后電極上出現(xiàn)氣泡,并匯集到試管上端.負極產(chǎn)生的氣體與正極產(chǎn)生的氣體的體積比為2:1,經(jīng)檢驗,負極產(chǎn)生的氣體是H2(填化學式),正極產(chǎn)生的氣體是O2(填化學式).從而證明了水是氫元素和氧元素組成的,寫出電解水的化學反應文字表達式水$\stackrel{通電}{→}$氫氣+氧氣.
實驗是化學學習的一種重要手段,如利用電解水實驗可探究水的組成.請根據(jù)電解水實驗回答下列問題:通電后電極上出現(xiàn)氣泡,并匯集到試管上端.負極產(chǎn)生的氣體與正極產(chǎn)生的氣體的體積比為2:1,經(jīng)檢驗,負極產(chǎn)生的氣體是H2(填化學式),正極產(chǎn)生的氣體是O2(填化學式).從而證明了水是氫元素和氧元素組成的,寫出電解水的化學反應文字表達式水$\stackrel{通電}{→}$氫氣+氧氣.查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題

查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com