
向20g赤鐵礦樣品中(樣品中雜質不溶于水,也不和酸反應)不斷加入稀鹽酸至固體量不再減少為止,共消耗稀鹽酸184g,測得剩余固體的質量為4g。請計算:
(1)赤鐵礦樣品中,氧化鐵的質量分數
(2)最后所得溶液中溶質的質量分數
【答案】(1)樣品中氧化鐵的質量是20g -4 g= 16 g ……………………………… 1分
樣品中,氧化鐵的質量分數為 ×100%= 80%…………………… 1分
×100%= 80%…………………… 1分
(2)解:設所得溶液中溶質的質量為x。
Fe2 O3 + 6HCl===2 FeCl3 + 3H2O ……………………………………… 1分
160 325
16g X
 160 325
160 325
16g X
X == 32.5g …………………………………………………… 1分
所得溶液的質量為:184 g + 20 g - 4 g=200 g …………………………… 1分
所得溶液中溶質的質量分數為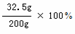 =16.25% …………………………1分
=16.25% …………………………1分
答:略。(單位和百分號都不在扣分范圍內)
【解析】(1)由題意可知,剩余的4g固體為礦石中雜質的質量,則可知20g赤鐵礦石中含氧化鐵的質量為20g-4g=16g,赤鐵礦中氧化鐵的質量分數= ×100%= 80%。
×100%= 80%。
(2)由發生的反應可知,反應后所得溶液為生成的氯化鐵的溶液,即本題要求反應后所得的氯化鐵溶液的溶質質量分數。要想求解本題,需知道反應后溶液的質量和溶液中的溶質FeCl3的質量。溶液質量可根據質量守恒定律求得,即所得溶液質量為參加反應的氧化鐵的質量與加入的稀鹽酸的質量之和:20g-4g+184g=200g。而FeCl3的質量需根據化學方程式計算進行求解,計算時的已知量是參加反應的氧化鐵的質量,設生成的氯化鐵質量為x,據此根據化學方程式中各物質的質量比關系,列出比例式并求出x,最后根據溶質質量分數計算公式解答本題。


 世紀百通期末金卷系列答案
世紀百通期末金卷系列答案科目:初中化學 來源: 題型:
工業上采用離子交換膜電解槽電解飽和食鹽水,可以得到高濃度的燒堿溶液(含NaOH35%~48%)。某學習小組為了驗證附近氯堿化工廠產生的NaOH溶液是否達到高濃度標準,進行了如下操作,請你參與計算:
(1)到工廠采集了電解槽中的NaOH溶液100g。NaOH中氧元素的質量分數是 。
(2)在實驗室用如右圖所示濃硫酸配制200g24.5%的稀硫酸,計算所取濃硫酸的體積 (計算結果取整數)。

(3)進行中和測定,向采集到的溶液中逐滴加入所配制的稀硫酸,并不斷測定溶液的pH值,當pH=7時,消耗稀硫酸160g。通過計算判斷此時電解槽中NaOH溶液是否達到高濃度標準。
查看答案和解析>>
科目:初中化學 來源: 題型:
某廠排放的廢水中含有碳酸鈉,未經處理,會造成污染.化學興趣小組的同學對廢水處理設計了如圖所示的實驗方案.

試計算:
(1)反應生成CO2氣體的質量是 2.2 g.
(2)反應后所得溶液中溶質的質量分數?
(溫馨提示:Na2CO3+2HC1═2NaC1+H2O+CO2↑)
查看答案和解析>>
科目:初中化學 來源: 題型:
重鉻酸鉀(K2Cr2O7,Mr=294。鉻元素為+6價,Mr表示相對分子質量)是一種重要的化工原料,在皮革工業、有機反應中都有廣泛應用。但+6價鉻有很強的毒性易污染環境,使用后,須用綠礬(FeSO4·7H2O,Mr=278)將其變成低毒性+3價鉻才能做后續處理.
反應原理:6FeSO4·7H2O+ K2Cr2O7+7H2SO4=3Fe2(SO4)3+Cr2(SO4)3+K2SO4+49H2O
現有1.0噸重鉻酸鉀需要處理,計算需要綠礬多少噸?(寫出計算過程,結果精確小數點后1位)
查看答案和解析>>
科目:初中化學 來源: 題型:
常溫下,氨氣為無色有刺激性惡臭氣味的氣體,密度比空氣小,易溶于水。氨氣溶于水顯弱堿性,實驗室可用氯化銨固體和氫氧化鈣固體混合加熱制取。則下列說法正確的是( )
A.可用向下排空氣法收集到氨氣 B.氨水能使紫色石蕊試液變紅色
C.多余的氨氣可排放到大氣中 D.實驗室制氨氣的發生裝置與雙氧水制氧氣相同
查看答案和解析>>
科目:初中化學 來源: 題型:
(1)請用化學用語表示或寫出符號的意義:
①氫氧根離子________;②二氧化硫中硫元素的化合價________;
③3H2O________。
(2)下列食物:①米飯;②雞蛋;③大豆油;④西紅柿。能提供大量蛋白質的是__________(填序號),蛋白質屬于______(填“無機物”或“有機物”)。
(3)香煙煙霧中含有多種有害物質,毒副作用大的有________、尼古丁和焦油,不吸煙的人能聞到煙味的原因是________;隨手丟棄的煙頭還容易引發火災,原因是(填字母)________(A.提供可燃物 B.提供氧氣 C.使可燃物的溫度達到著火點)。一旦發生火災,消防隊員通常用水來滅火,該方法的化學原理是
______________________________________________________。
查看答案和解析>>
科目:初中化學 來源: 題型:
20℃時,取甲、乙、丙、丁四種純凈物各20g,分別加入到四個各盛有50g水的燒杯中,充分溶解,其溶解情況如表:
| 物質 | 甲 | 乙 | 丙 | 丁 |
| 未溶解固體的質量/g | 4.2 | 2 | 0 | 9.2 |
下列說法正確的是( )
A.所得四杯溶液都是飽和溶液
B.丁溶液的溶質質量分數最大
C.20℃時四種物質溶解度的關系為:丙>乙>甲>丁
D.四杯溶液中溶劑的質量大小為:丙溶液>乙溶液>甲溶液>丁溶液
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com