
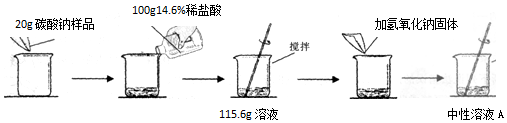
分析 碳酸鈉和稀鹽酸反應生成氯化鈉、水和二氧化碳,根據反應的化學方程式及其提供的數據可以進行相關方面的計算和判斷;
稀釋溶液時,溶質質量不變.
解答 解:(1)需要36.5%的濃鹽酸的質量為:100g×14.6%÷36.5%=40g,
則需要水的質量為:100g-40g=60g,
故填:60g.
(2)樣品中碳酸鈉和稀鹽酸反應生成氯化鈉、水和二氧化碳,反應的化學方程式為:Na2CO3+2HCl=2NaCl+H2O+CO2↑.
故填:Na2CO3+2HCl=2NaCl+H2O+CO2↑.
(3)設碳酸鈉質量為X,反應的氯化氫質量為Y,生成氯化鈉質量為Z,
反應生成二氧化碳質量為:20g+100g-115.6g=4.4g,
Na2CO3+2HCl=2NaCl+H2O+CO2↑,
106 73 117 44
X Y Z 4.4g
$\frac{106}{X}$=$\frac{73}{Y}$=$\frac{117}{Z}$=$\frac{44}{4.4g}$,
X=10.6g,Y=7.3g,Z=11.7g,
故填:$\frac{106}{X}$=$\frac{44}{4.4g}$.
(4)該樣品中碳酸鈉的質量分數為:$\frac{10.6g}{20g}$×1005=53%,
故填:53%.
(5)設氫氧化鈉質量為x,生成氯化鈉質量為y,
和氫氧化鈉反應的氯化氫質量為:100g×14.6%-7.3g=7.3g
NaOH+HCl═NaCl+H2O,
40 36.5 58.5
x 7.3g y
$\frac{40}{x}$=$\frac{36.5}{7.3g}$=$\frac{58.5}{y}$,
x=8g,y=11.7g,
中性溶液A中氯化鈉質量為:20g-10.6g+11.7g+11.7g=32.8g,
向中性溶液A中加入76.4g水,最終得到溶液質量為:115.6g+8g+76.4g=200g,
溶質質量分數是:$\frac{32.8g}{200g}$×100%=16.4%,
故填:16.4%.
(6)20t樣品中碳酸鈉質量為:20t×$\frac{10.6g}{20g}$×100%=10.6t,
設轉化成氫氧化鈉的質量為z,
Na2CO3~2NaOH,
106 80
10.6t z
$\frac{106}{10.6t}$=$\frac{80}{z}$,
z=8t,
若將20t樣品中的純堿轉化為燒堿,則制得含雜質的燒堿質量為:20t-10.6t+8t=17.4t,
答:若將20t樣品中的純堿轉化為燒堿,則制得含雜質的燒堿質量為17.4t.
點評 本題主要考查學生運用假設法和化學方程式進行計算和推斷的能力,計算時要注意規范性和準確性.


 教材全解字詞句篇系列答案
教材全解字詞句篇系列答案科目:初中化學 來源: 題型:推斷題
 如圖表示的是初中幾種常見物質的轉化關系(部分反應物、生成物及反應條件省略),已知C為生活中不可缺少的調味品,F為大理石的主要成分,D、E、H是同種類別的物質,請回答以下問題:
如圖表示的是初中幾種常見物質的轉化關系(部分反應物、生成物及反應條件省略),已知C為生活中不可缺少的調味品,F為大理石的主要成分,D、E、H是同種類別的物質,請回答以下問題:查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 6.4g | B. | 8g | C. | 10.5 g | D. | 12.8g |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
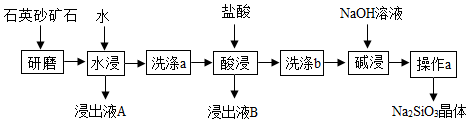
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| 20℃ | 40℃ | |
| 水 | 109g | 129g |
| 酒精 | 17.3g | 40g |
| A. | 溫度和溶劑種類對NaOH的溶解度都有影響 | |
| B. | NaOH易溶于水,也易溶于酒精 | |
| C. | 40℃,40gNaOH溶解在l00g酒精中達到飽和 | |
| D. | 將等質量40℃的飽和NaOH水溶液和飽和NaOH酒精溶液降溫至20℃,析出的晶體前者比后者多 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | NaOH | B. | NaHCO3 | C. | H2SO4 | D. | K2SO4 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com