
分析 因反應中只有二氧化碳是氣體,則根據反應前后溶液的質量差來計算二氧化碳的質量,將二氧化碳的量代入化學反應方程式來計算稀硫酸中溶質的質量及碳酸鈉的質量.
解答 解:根據質量守恒定律,二氧化碳的質量為20g+100g+50g-165.6g=4.4g
設碳酸鈉的質量為x,滴加的稀硫酸中溶質的質量為y
則Na2CO3+H2SO4=Na2SO4+CO2↑+H2O
106 98 44
x y 4.4g
$\frac{106}{x}=\frac{98}{y}=\frac{44}{4.4g}$
x=10.6g
y=9.8g
(1)滴加的稀硫酸中溶質的質量分數=$\frac{9.8g}{50g}$×100%=19.6%
(2)該樣品中Na2CO3的質量分數=$\frac{10.6g}{20g}×$100%=53%
答案:
(1)滴加的稀硫酸中溶質的質量分數為19.6%;
(2)該樣品中Na2CO3的質量分數為53%.
點評 本題考查學生利用化學反應方程式的計算,利用物質的狀態及質量守恒來計算二氧化碳的質量是解答本題的關鍵.


 閱讀快車系列答案
閱讀快車系列答案科目:初中化學 來源: 題型:選擇題
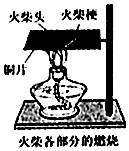
| A. | 有可燃物 | B. | 有助燃劑 | ||
| C. | 溫度達到可燃物的著火點 | D. | 可燃物與火焰直接接觸 |
查看答案和解析>>
科目:初中化學 來源: 題型:多選題
| A. | Na2CO3 H2SO4 HCl Ba(NO3)2 | B. | NaOH NaCl HCl FeCl3 | ||
| C. | Na2SO4 BaCl2 HCl K2CO3 | D. | NaOH NaCl KNO3 MgCl2 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 將25mL水慢慢倒入盛有5.4mL濃硫酸的量筒中,并用玻璃棒不斷攪拌 | |
| B. | 將10g98%的濃硫酸沿燒杯壁慢慢注入盛有25mL水的燒杯中,并用玻璃棒不斷攪拌 | |
| C. | 若其他操作正確,量取25mL水時俯視,則所配稀硫酸中溶質的質量分數小于28% | |
| D. | 配制該溶液時,若有濃硫酸沾到手上應立即用氫氧化鈉溶液中和 |
查看答案和解析>>
科目:初中化學 來源: 題型:推斷題
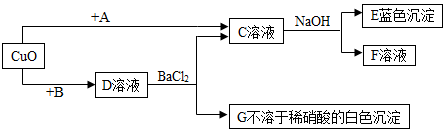
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題

查看答案和解析>>
科目:初中化學 來源: 題型:填空題
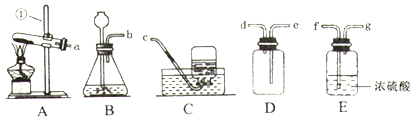
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
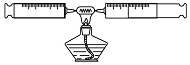 在由兩個注射器組成的密閉系統內共有50mL空氣,如下圖.然后給裝有紅磷的玻璃管加熱.同時交替推動兩個注射器的活塞,至玻璃管內的紅磷變成白煙,且較長時間內無進一步變化時停止.停止加熱后,待冷卻至室溫將氣體全部推至一個注射器內.
在由兩個注射器組成的密閉系統內共有50mL空氣,如下圖.然后給裝有紅磷的玻璃管加熱.同時交替推動兩個注射器的活塞,至玻璃管內的紅磷變成白煙,且較長時間內無進一步變化時停止.停止加熱后,待冷卻至室溫將氣體全部推至一個注射器內.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com