
分析 根據鋅和硫酸反應生成硫酸鋅和氫氣,利用生成硫酸鋅的質量參加反應的稀硫酸中H2SO4的質量以及合金中鋅的質量,進而求出合金中銅的質量分數即可.
解答 解:(1)設參加反應的稀硫酸中H2SO4的質量為y,黃銅樣品中鋅的質量為z,
Zn+H2SO4=ZnSO4 +H2↑
65 98 161
z y 100g×16.1%
$\frac{65}{x}$=$\frac{98}{y}$=$\frac{161}{100g×16.1%}$
y=9.8g
z=6.5g
稀硫酸中H2SO4的質量是9.8g;
(2)合金中銅的質量分數為:$\frac{10g-6.5g}{10g}$×100%=35%.
故答案為:(1)9.8g;
(2)合金中銅的質量分數是35%.
點評 本題難度不大,掌握化學方程式與溶質質量分數的綜合計算即可正確解答本題,解題時要注意解題的規范性.


科目:初中化學 來源: 題型:選擇題
 硝酸鉀與氯化鉀的溶解度曲線如圖所示.下列說法錯誤的是( )
硝酸鉀與氯化鉀的溶解度曲線如圖所示.下列說法錯誤的是( )| A. | 硝酸鉀和氯化鉀的溶解度都是隨溫度升高而增大 | |
| B. | 20℃時,硝酸鉀和氯化鉀的溶解度相等 | |
| C. | 40℃時,硝酸鉀溶液的溶質質量分數比氯化鉀大 | |
| D. | 60℃時,55克硝酸鉀溶于50水中,恰好形成飽和溶液 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
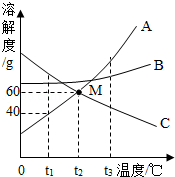 如圖是常見固體物質的溶解度曲線,根據圖示回答:
如圖是常見固體物質的溶解度曲線,根據圖示回答:查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
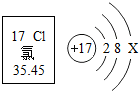 根據如圖的信息判斷,下列說法中,錯誤的是( )
根據如圖的信息判斷,下列說法中,錯誤的是( )| A. | 氯原子的質子數是17 | B. | 氯原子核外有3個電子層 | ||
| C. | 當X=8時,該微粒是陰離子 | D. | 在化學變化中,氯原子易失電子 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
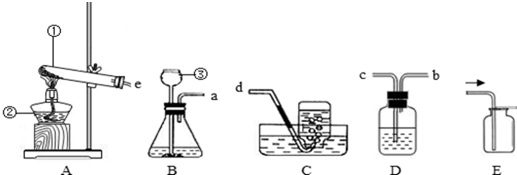
| 物質 | 制取氣體的藥品 | 制取氣體的反應條件 | 氣體的物理性質 |
| 氯氣 | MnO2固體和濃鹽酸 | 需要加熱 | 可溶于水,密度比空氣大 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com