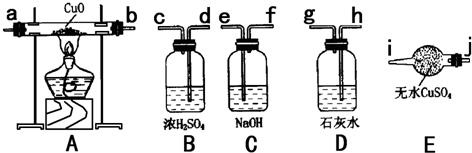
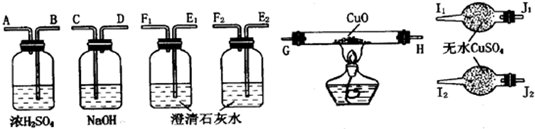
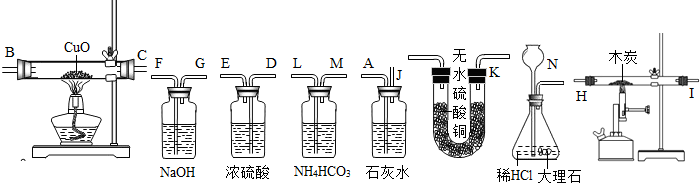
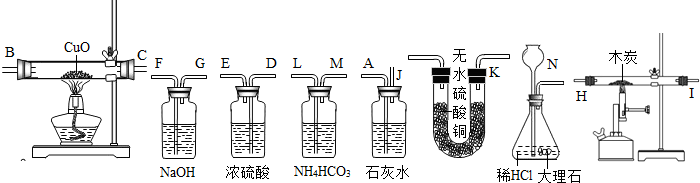
解:①由該實驗可知,應選擇制取二氧化碳裝置→除雜裝置→干燥裝置→一氧化碳的制取裝置→吸收二氧化碳的裝置→還原實驗裝置→驗證實驗產物的裝置來選擇接口,且除雜時導管長進短出,故答案為:N→L M→J K→H I→F G→D E→B C→A;
②因鹽酸容易揮發,則二氧化碳中混有HCl,則NaHCO
3溶液的作用是吸收HCl氣體,故答案為:吸收HCl氣體;
③因濃硫酸和無水硫酸銅都具有吸收性,則起干燥作用的物質為濃硫酸和無水硫酸銅,故答案為:濃硫酸和無水硫酸銅;
①因氫氧化鈉在還原實驗裝置之前,為排除對還原實驗產生檢驗的影響,應將一氧化碳中混有的二氧化碳除去,則氫氧化鈉可吸收二氧化碳,氫氧化鈣溶液在還原實驗裝置之后,則可利用二氧化碳使澄清石灰水變渾濁來檢驗二氧化碳,故答案為:吸收CO
2氣體;證明氧化產物是CO
2;
②因實驗中碳與二氧化碳反應生成二氧化碳,反應條件為高溫,則反應為C+CO
2
2CO,故答案為:C+CO
2
2CO.
分析:(1)根據實驗的目的可知要檢驗一氧化碳的還原性可知,則應選擇制取二氧化碳裝置→除雜裝置→干燥裝置→一氧化碳的制取裝置→吸收二氧化碳的裝置→還原實驗裝置→驗證實驗產物的裝置來選擇接口,除雜時導管長進短出;
(2)利用氣體的成分及物質之間的反應來分析溶液的作用;
(3)根據物質的性質來分析起干燥作用的物質;
(4)根據裝置的位置及通過裝置的氣體的成分來分析溶液的作用;
(5)根據生成CO的裝置中的反應物來書寫化學反應方程式.
點評:本題考查學生選擇實驗裝置,并制取氣體并驗證氣體的還原性,學生應注意氣體之間的相互影響,注意除雜及利用物質的性質來檢驗物質,考查很全面.

 2CO,故答案為:C+CO2
2CO,故答案為:C+CO2 2CO.
2CO.

 智能訓練練測考系列答案
智能訓練練測考系列答案