
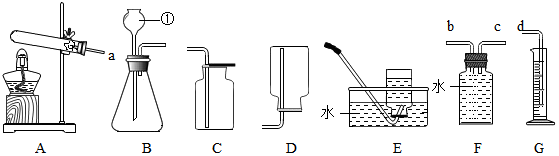
分析 (1)根據常用儀器的名稱和用途判斷;
(2)根據制取二氧化碳的反應物狀態和反應的條件選擇發生裝置;根據二氧化碳的密度和溶解性選擇收集裝置;根據碳酸鈣和稀鹽酸反應生成氯化鈣、水和二氧化碳書寫化學方程式;根據一氧化碳的密度和空氣接近,并且有毒,不溶于水進行分析;
(3)若各裝置的連接順序是:a→b→c→d,F裝置內導管,c管延長,有利于排水;
(4)根據化學方程式:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑可知,二氧化錳在反應前后固體混合物中的質量分數的變化;
(5)根據燃燒的條件進行解答.
解答 解:(1)據圖可以知道,①是試管,②是集氣瓶,故填:試管,集氣瓶;
(2)實驗室制取二氧化碳使用的是碳酸鈣固體和稀鹽酸在常溫下反應,故發生裝置選擇B;二氧化碳的密度比空氣大,能溶于水,故選擇C收集裝置;碳酸鈣和稀鹽酸反應生成氯化鈣、水和二氧化碳,反應的化學方程式為:CaCO3+2HCl=CaCl2+H2O+CO2↑;一氧化碳的密度和空氣接近,并且有毒,不溶于水,不能用排氣法收集,只能用排水法收集,故選擇E收集裝置;
(3)若各裝置的連接順序是:a→b→c→d,F裝置內導管,c管延長,有利于排水,從而通過測量水的體積測量氧氣的體積,故如圖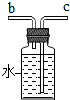 ;
;
(4)根據化學方程式:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑可知,二氧化錳在反應前后固體混合物中的質量分數的變化為變大;
(5)燃燒的條件是可燃物、氧氣、達到物質的著火點,前2項已具備,所以棉花未燃燒是因為未達到其著火點.
故答案為:(1)長頸漏斗;(2)BC;CaCO3+2HCl═CaCl2+H2O+CO2↑; E (3)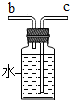 ;(4)變大;(5)溫度沒有達到著火點.
;(4)變大;(5)溫度沒有達到著火點.
點評 本題考查了常見氣體的實驗室制取裝置和收集方法,完成此題,可以依據已有的知識進行.解題時明確依據反應物的狀態和條件選擇發生裝置,根據氣體的密度和溶解性選擇收集裝置及方程式的書寫.


科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 呼出氣體中的水蒸氣含量大于空氣中水蒸氣含量 | |
| B. | 硫酸銅溶液和氫氧化鈉溶液反應后,藍色固體減少至消失,形成藍色溶液 | |
| C. | 試管中的水沸騰時,看見試管口產生白霧 | |
| D. | 大理石和稀鹽酸反應時,可以看到固體表面有二氧化碳氣體冒出 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com