某集團是一家以生產電纜類產品為主的國家大型企業.在電纜生產過程中,不可避免地會產生一定量的含銅廢料(如:零碎電纜).某化學興趣小組的四位同學得知這一情況后,圍繞“從含銅廢料中回收銅”提出了各自的看法.
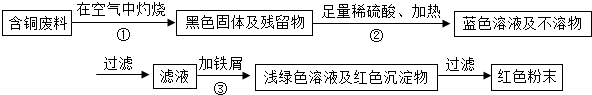
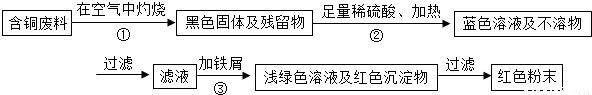
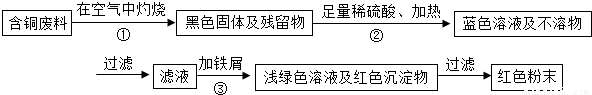
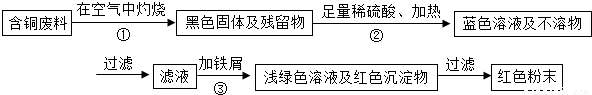
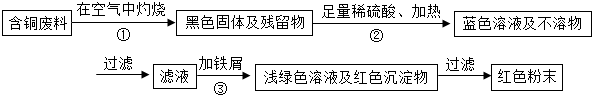
甲同學根據已學知識,提出了一套回收方案:
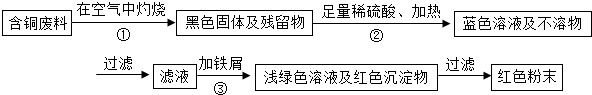
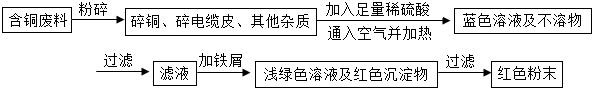
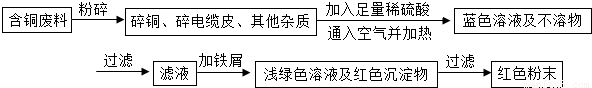
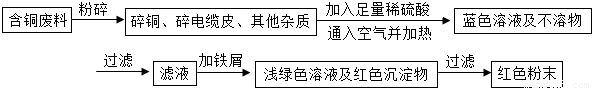
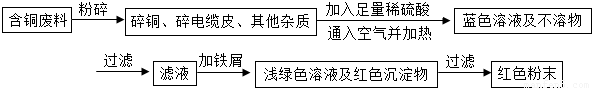
乙同學在查閱資料后得知:在通入空氣并加熱的條件下,銅可與稀硫酸在溶液中發生反應(方程式為:2Cu+2H
2SO
4+O
2?2CuSO
4+2H
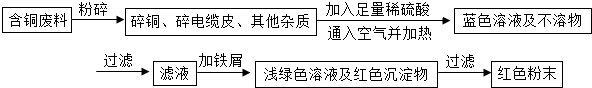
2O),于是他提出了另一套方案:
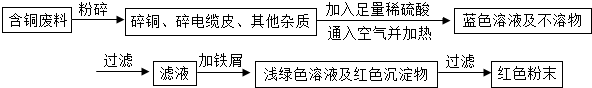
(1)甲方案的①②③三個步驟中,與銅或銅的化合物有關的化學反應方程式分別是:
①
;②
;③
.
(2)從環保角度對兩套方案的不同部分進行比較,你認為
(填“甲”或“乙”)的方案更合理.理由是:
.
(3)丙認為,無論是甲還是乙的方案,在“加鐵屑”這一步時,應該加入略過量的鐵屑.你認為丙這么說的道理是:
.
丁又提出了疑問:“如果鐵過量,剩余的鐵會混在紅色粉末中,該怎么處理呢?”.請提出你的想法:
.
(4)最后,老師肯定了同學們的積極思考,但同時指出:方案最后一步所得淺綠色濾液結晶后,會得到一種俗稱“綠礬”的工業產品,可增加經濟效益.請寫出使“綠礬”結晶的兩種可能方法:
、
(“綠礬”溶解度隨溫度升高而增大).如果直接排放掉濾液,不僅造成了浪費,還會
.
(5)若上述方案所用的稀硫酸溶質質量分數為36.8%,問每1000mL98%的濃硫酸(密度為1.84g/mL)能配制出這種稀硫酸
g,需水
mL(水的密度為1.0g/mL).在實驗室中稀釋濃硫酸時,是如何操作的:
.
(6)根據乙同學查出的方程式(2Cu+2H
2SO
4+O
2?2CuSO
4+2H
2O)計算:如果1000mL98%的濃硫酸(密度為1.84g/mL)稀釋后全部參加了反應(假設硫酸不和碎電纜皮、其他雜質反應),所能處理的廢料中含純銅多少克?(請寫出計算過程,結果精確到0.1克)

 2CuO,Fe+CuSO4═FeSO4+Cu;
2CuO,Fe+CuSO4═FeSO4+Cu;

 浙江名校名師金卷系列答案
浙江名校名師金卷系列答案